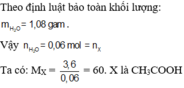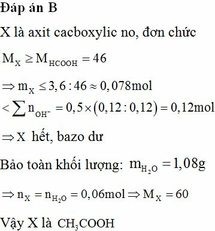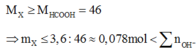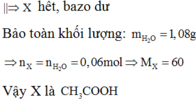Hãy tính pH của dung dịch A gồm KCN 0,12M; NH3 0,15M và KOH 0,005M. Cho biết pKa của HCN là 9,35 của \(NH^+_4\) là 9,24
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) \(n_{H^+}=n_{HCl}+2n_{H_2SO_4}=0,1\cdot0,12+0,1\cdot0,04=0,016\)
\(C_M=\dfrac{0,016}{0,2}=0,08M\)
\(\Rightarrow pH=-log\left(0,08\right)=1,1\)
b) \(n_{OH^-}=n_{KOH}+2n_{Ba\left(OH\right)_2}=0,012+2\cdot0,004=0,02\)
\(C_M=\dfrac{0,02}{0,2}=0,1\)
\(\Rightarrow pH=-log\left(\dfrac{10^{-14}}{0,1}\right)=13\)

\(n_{NaOH}=0,006\left(mol\right)\\ \Rightarrow n_{Na^+}=0,006\left(mol\right);n_{OH^-}=0,006\left(mol\right)\\ n_{H_2SO_4}=0,005\left(mol\right)\\ \Rightarrow n_{H^+}=0,01\left(mol\right);n_{SO_4^{2-}}=0,005\left(mol\right)\\ H^++OH^-\rightarrow H_2O\\ LTL:\dfrac{0,01}{1}>\dfrac{0,006}{1}\Rightarrow H^+dư\\ \left[H^+_{dư}\right]=\dfrac{0,01-0,006}{0,1}=0,04M\\ \left[Na^+\right]=\dfrac{0,006}{0,1}=0,06M\\ \left[SO_4^{2-}\right]=\dfrac{0,005}{0,1}=0,05M\)

CTTQ : CnH2n+1COOH
Gọi CT chung của NaOH và KOH là MOH
CnH2n+1COOH + MOH --> CnH2n+1COOM +H2O
BTKL ta có :
mH2O=1,08(g) => nH2O =0,06(mol)
Ta thấy : naxit = nH2O = 0,06(mol)
=> Maxit = 60(g/mol)
=> CTPT :CH3COOH

nNaOH = 0,06; nKOH =0,06
Có RCOOH + MOH ⟶ RCOOM + H2O
Theo định luật bảo toàn khối lượng ta có:
mX +mNaOH + mKOH = mrắn khan + m H 2 O
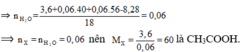
Đáp án D

Đáp án B
Hướng dẫn nKOH = 0,06 mol; nNaOH = 0,06 mol
Bảo toàn khối lượng: mX + mNaOH + mKOH = mrắn khan + mH2O
=> mH2O = 1,08 gam => nH2O = 0,06 mol
Vì X là axit đơn chức => nX = nROH = nH2O = 0,06 mol
=> MX = 3,6 / 0,06 = 60
=> X là CH3COOH