Điện phân 500ml dung dịch NaCl 1M có màng ngăn hiệu suất phản ứng điện phân đạt 80%. Cho khí Cl2 sinh ra tác dụng với 11,2 gam Fe. tính khối lượng muối tạo thành
Giúp với nha!!
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

2NaCl + 2H2O điện phân dd có màng ngăn --> 2NaOH + Cl2 + H2
nCl2 =\(\dfrac{8,96}{22,4}\)= 0,4 mol . Hiệu suất phản ứng = 80% => nNaCl = \(\dfrac{0,4.2}{80\%}\)=1 mol
=> mNaCl = 1.58,5 = 58,5 gam

Chọn C.
Ta có: ne = 0,12 mol ® Tại anot có khí Cl2 (x mol) và O2 (y mol) và tại catot có Cu (0,06 mol).
mà mdd giảm = 71x + 32y + 0,06.64 = 6,45 và 2x + 4y = 0,12 Þ x = 0,03 ; y = 0,015.
Dung dịch Y có chứa H2SO4 (0,015.2 = 0,03 mol) ; Na2SO4 (0,03 mol).
Khi cho 0,05 mol Fe(NO3)2 vào Y thì:
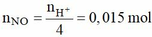
Dung dịch Z chứa Fen+ (0,05), Na+ (0,06), SO42- (0,06), NO3- (0,1 – 0,015 = 0,085) Þ m = 15,21 (g)
nNaCl = 1.0,5=0,5(mol)
Ta có PT:
2NaCl + 2H2O ---> 2NaOH + Cl2 + H2
....0,5........0,5...............0,5.......0,25..0,25
Vì hiệu suất pư xảy ra là 80%
=> n\(Cl_2\) thu được =0,25.80%=0,2(mol)
Ta có PT
2Fe + 3Cl2 ---> 2FeCl3
nFe=\(\frac{11,2}{56}\)=0,2(mol)
Ta có: \(\frac{0,2}{2}\)>\(\frac{0,2}{3}\)=> Fe dư
=> n\(FeCl_3\)=\(\frac{2}{3}\)n\(Cl_2\)=\(\frac{2}{3}\).0.2=0,1333(mol)
m\(FeCl_3\)=0,1333.162,5=21,66(g)