Hòa tan hỗn CaO và CaCO3 bằng dung dịch H2SO4 loãng thu được dung dịch A, khí B. Cô cạn dung dịch A thu được 3,44 gam thạch cao (CaSO4.2H2O) , hấp thụ khí B bằng 100 ml dung dịch NaOH 0,16 M. Sau đó them BaCl2 dư vào thấy tạo ra 1,182 gam kết tủa. Tính khối lượng mỗi chất có trong hỗn hợp ban đầu.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án B
Vì H2SO4 đặc nóng dư nên khí A sinh ra là SO2.
Muối khan thu được là
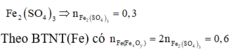
Vì dung dịch NaOH dư nên khỉ dẫn SO2 vào đung dịch NaOH chỉ xảy ra một phản ứng:
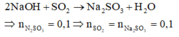
Coi oxit FexOy ban đầu là hỗn hợp của Fe và O.
Gọi nO = a.
Áp dụng định luật bảo toàn moi electron, ta có:


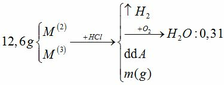
Đồng nhất dữ kiện để thuận lợi cho tính toán, bằng cách nhân đôi khối lượng H2O.
a.
BTNT H: nH2 = nH2O = 0,31 mol
=> nHCl = 0,62mol
BTKL: m kim loại + mHCl = mA + mB => 12,6 + 36,5 . 0,62 = m + 2 . 0,31 => m = 34,61g
b.
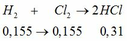
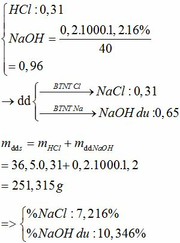

Đáp án : D
Giả sử kim loại M có hóa trị x
=> muối có dạng M2(SO4)x
=> m S O 4 p ư = mmuối – mKL = 49,4592g
=> n S O 4 p ư = 0,5152 mol
=> M = 20x (g)
Nếu x = 2 => M = 40g => Ca







Ta có:
nCaCO3 + nCaO = nCaSO4 = 0,02 mol
nNaOH = 0,016 mol, nBaCO3 = 0,006 mol
*TH1 : NaOH dư (Chỉ tạo Na2CO3)
Bảo toàn C : nCaCO3 = nCO2 = nBaCO3 = 0,006 mol ⇒ nCaO = 0,02 – 0,006 = 0,014 mol
mCaCO3 = 0,6g và mCaO = 0,784g (1)
*TH2 : CO2 và NaOH đều hết (Tạo hh 2 muối).
CO2 + NaOH\(\rightarrow\) NaHCO3
u_______u ________________mol
CO2 + 2NaOH \(\rightarrow\) Na2CO3 + H2O
v _____2v_________ v______________mol
nNa2CO3 = nBaCO3 = 0,006 mol = v
⇒ u = 0,016 – 2v = 0,004 mol
nCO2 = 0,01 mol
nCaCO3 = nCO2 = 0,01 ⇒ nCaO = 0,02 – 0,01 = 0,01 mol
mCaCO3 = 1g và mCaO = 0,56g (2)
– Từ (1),(2) ⇒ Khối lượng CaCO3 và CaO lần lượt là (0,6 ; 0,784) hoặc (1 ; 0,56).