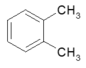
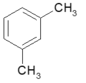
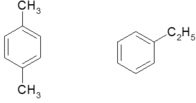
Đốt cháy hoàn toàn 5,8 gam chất X thu được 2,65 gam Na2CO3; 2,25 gam H2O và 13,2 gam CO2. Công thức phân tử của X là A
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Lời giải:
nNa2CO3 = 0,025 ⇒ nNa = 0,05
nH2O = 0,125
nCO2 = 0,275
⇒ nC/X = 0,275 + 0,025 = 0,3
Có mX = mH + mC + mNa + mO ⇒ mO = 5,8 – 0,3.12 – 0,05.23 – 0,125.2 = 0,8
⇒ nO = 0,05
⇒ Trong X có C : H : O : Na = 6 : 5 : 1 : 1
⇒ X là C6H5ONa
C6H5ONa + CO2 + H2O → C6H5OH + NaHCO3
⇒ Y là C6H5OH
Đáp án D.

Đáp án B
Khi 0,1 mol Y phản ứng với 0,2 mol Na => Y có tổng số nhóm OH và COOH trong phân tử là 2
Mà X hidro hóa tạo Y => X có 2 nhóm CHO ( Vì X thuần chức )
. => nX = ¼ nAg = 0,1 mol
=> MX = 58g => X là (CHO)2
Khi đốt cháy X thì nCO2 = 2nH2O

Đáp án B
, Khi 0,1 mol Y phản ứng với 0,2 mol Na => Y có tổng số nhóm OH và COOH trong phân tử là 2
Mà X hidro hóa tạo Y => X có 2 nhóm CHO ( Vì X thuần chức )
. => nX = ¼ nAg = 0,1 mol
=> MX = 58g => X là (CHO)2
Khi đốt cháy X thì nCO2 = 2nH2O

ĐÁP ÁN B
Xét chất Y : , nNa = 0,2 mol = 2nancol => Y có 2 nhóm OH => Y có tối đa 2 nhóm CHO
Xét chất X :
, nAg = 0,4 mol.
+) TH1 : Nếu là HCHO -> nHCHO = 0,193 mol => ¼ nAg (Loại)
+) TH2 : Nếu là RCHO -> nRCHO = ½ nAg = 0,2 mol => MRCHO = 29(Loại)
+) TH3 : Nếu là R(CHO)2 -> nR(CHO)2 = ¼ nAg = 0,1 mol => M = 58 => (CHO)2

Đáp án D
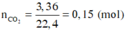
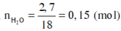
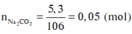
mX = mC + mH + mO + mNa = 12 ( n N a 2 C O 3 + n C O 2 ) + 2 n H 2 O + 23.2. n N a 2 C O 3 + m O
Þ 12.(0,15 + 0,05) + 2.0,15 + 46.0,05 + mO = 8,2
Þ mO = 3,2 gam

Đáp án : A
Áp dụng định luật bảo toàn khối lượng ta có:
mhh X = mC4H10 = 5,8 (g)
=> Đốt cháy hỗn hợp X cũng giống như đốt cháy C4H10
Ta có: nC4H10 = 5,8/58 = 0,1 mol
C4H10 => 4CO2 + 5H2O
0,1 0,5
=> mH2O = 0,5.18 = 9 (g)