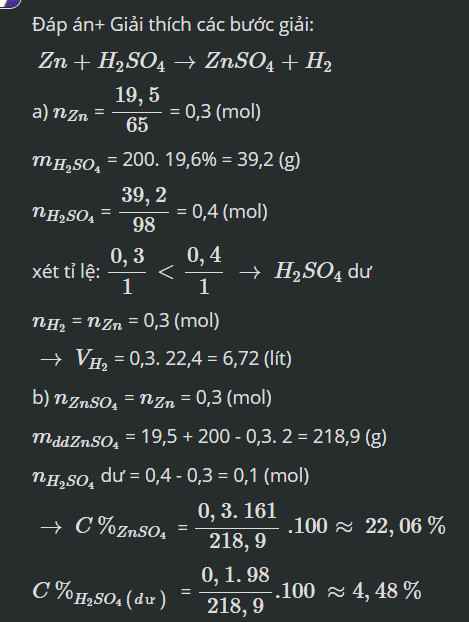Trộn 300 gam dung dịch H2SO4 19,6 % với 200 gam dung dịch NaOH 4% . Tính C% các chất tan có trong dung dịch ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{H_2SO_4}=\dfrac{200.19,6}{100.98}=0,4mol\\ CuO+H_2SO_4\rightarrow CuSO_4+H_2O\\ n_{CuSO_4\left(A\right)}=n_{CuO}=n_{H_2SO_4}=0,4mol\\ n_{Cu\left(OH\right)_2}=\dfrac{29,4}{98}=0,3mol\\ CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\\\Rightarrow\dfrac{0,4}{1}>\dfrac{0,3}{1}\Rightarrow CuSO_4.pư.không.hết\)
\(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
0,3mol 0,6mol 0,3mol
\(m_{ddB}=0,4.80+200+0,6.40-29,4=226,6g\\ C_{\%Na_2SO_4\left(B\right)}=\dfrac{0,3.142}{226,6}\cdot100=18,8\%\)

Ta có: \(n_{H_2SO_4}=\dfrac{200.19,6\%}{98}=0,4\left(mol\right)\)
\(n_{Cu\left(OH\right)_2}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
PT: \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
Dung dịch A gồm: CuSO4 và H2SO4 dư
\(H_2SO_4+2NaOH\rightarrow Na_2SO_4+2H_2O\)
\(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
Đề có cho dữ kiện gì liên quan đến dd NaOH không bạn nhỉ?

\(\begin{cases} m_{H_2SO_4}=\dfrac{100.19,6\%}{100\%}=19,6(g)\\ m_{BaCl_2}=\dfrac{300.20,8\%}{100\%}=62,4(g) \end{cases} \Rightarrow \begin{cases} n_{H_2SO_4}=\dfrac{19,6}{98}=0,2(mol)\\ n_{BaCl_2}=\dfrac{62,4}{208}=0,3(mol) \end{cases}\\ a,PTHH:BaCl_2+H_2SO_4\to BaSO_4\downarrow +2HCl\)
Vì \(\dfrac{n_{H_2SO_4}}{1}<\dfrac{n_{BaCl_2}}{1}\) nên \(BaCl_2\) dư
\(\Rightarrow n_{BaSO_4}=0,2(mol)\\ \Rightarrow m_{BaSO_4}=0,2.233=46,6(g)\)
\(b,n_{HCl}=n_{BaSO_4}=0,2(mol)\\ \Rightarrow m_{CT_{HCl}}=0,2.36,5=7,3(g)\\ m_{dd_{HCl}}=100+300-46,6=353,4(g)\\ \Rightarrow C\%_{HCl}=\dfrac{7,3}{353,4}.100\%\approx 2,07\%\)

a, \(BaCl_2+H_2SO_4\rightarrow2HCl+BaSO_{4\downarrow}\)
b, \(m_{BaCl_2}=200.2,08\%=4,16\left(g\right)\Rightarrow n_{BaCl_2}=\dfrac{4,16}{208}=0,02\left(mol\right)\)
\(m_{H_2SO_4}=300.9,8\%=29,4\left(g\right)\Rightarrow n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,02}{1}< \dfrac{0,3}{1}\), ta được H2SO4 dư.
Theo PT: \(\left\{{}\begin{matrix}n_{BaSO_4}=n_{H_2SO_4\left(pư\right)}=n_{BaCl_2}=0,02\left(mol\right)\\n_{HCl}=2n_{BaCl_2}=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=0,3-0,02=0,28\left(mol\right)\)
Ta có: m dd sau pư = m dd BaCl2 + m dd H2SO4 - mBaSO4 = 200 + 300 - 0,02.233 = 495,34 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{HCl}=\dfrac{0,04.36,5}{495,34}.100\%\approx0,295\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{0,28.98}{495,34}.100\%\approx5,54\%\end{matrix}\right.\)

\(n_{HCl}=\dfrac{300.7,3\%}{36,5}=0,6\left(mol\right)\\ n_{NaOH}=\dfrac{200.4\%}{40}=0,2\left(mol\right)\\ a.NaOH+HCl\rightarrow NaCl+H_2O\\ Vì:\dfrac{0,6}{1}>\dfrac{0,2}{1}\\ \Rightarrow HCldư\\ b.n_{HCl\left(p.ứ\right)}=n_{NaCl}=n_{NaOH}=0,2\left(mol\right)\\ n_{HCl\left(dư\right)}=0,6-0,2=0,4\left(mol\right)\\ m_{ddsau}=300+200=500\left(g\right)\\ C\%_{ddHCl\left(dư\right)}=\dfrac{0,4.36,5}{500}.100=2,92\%\\ C\%_{ddNaOH}=\dfrac{0,2.58,5}{500}.100=2,34\%\)
c. Vì dư HCl => Qùy tím sẽ hóa đỏ.

Bài 19 :
\(a) n_{Al} = \dfrac{10,8}{27} = 0,4(mol)\\ 2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ n_{H_2} = \dfrac{3}{2}n_{Al} = 0,6(mol)\\ V_{H_2} = 0,6.22,4 = 13,44(lít)\\ b) \text{Chất tan : }Al_2(SO_4)_3\\ n_{Al_2(SO_4)_3} = \dfrac{1}{2}n_{Al} = 0,2(mol)\\ m_{Al_2(SO_4)_3} = 0,2.342 = 68,4(gam)\)
Bài 18 :
\(a) n_{HCl} = \dfrac{250.7,3\%}{36,5 } = 0,5(mol)\\ Zn + 2HCl \to ZnCl_2 + H_2\\ n_{H_2} = \dfrac{1}{2}n_{HCl} = 0,25(mol) \Rightarrow V_{H_2} = 0,25.22,4 = 5,6(lít)\\ b) \text{Chất tan : } ZnCl_2\\ n_{ZnCl_2} = n_{H_2} = 0,25(mol)\\ m_{ZnCl_2} = 0,25.136 = 34(gam)\)

\(a,n_{Zn}=\dfrac{19,5}{65}=0,3\left(mol\right)\\ m_{H_2SO_4}=200.19,6\%=39,2\left(g\right)\\ \rightarrow n_{H_2SO_4}=\dfrac{39,2}{98}=0,4\left(mol\right)\)
PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
bđ 0,3 0,4
pư 0,3 0,3
spư 0 0,1 0,3 0,3
\(\rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
\(b,m_{dd}=19,5+200-0,3.2=218,9\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}C\%_{ZnSO_4}=\dfrac{0,3.161}{218,9}.100\%=22,06\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{0,1.98}{218,9}.100\%=4,48\%\end{matrix}\right.\)

Khối lượng chất tan có trong 200gam dung dịch H2SO4 19,6%:
\(m_{H_2SO_4}=\dfrac{200.19,6}{100}=39,2\left(g\right)\\ \)
Khối lượng chất tan có trong 150gam dung dịch H2SO4 9,8%:
\(m_{H_2SO_4}=\dfrac{150.9,8}{100}=14,7\left(g\right)\)
Nồng độ phần trăm của dd A:
\(C\%_{ddA}=\dfrac{39,2+14,7}{200+150}.100=15,4\%\)
áp dụng sơ đồ đường chéo ta có :
200g dd H2SO4 19,6%------------------------- x-9,8 ( %)
--------------------------------- x ( % )
150g dd H2SO4 9,8 %-------------------------19,6-x ( %)
trong đó x là nồng độ % của dung dịch A thu được
=> \(\dfrac{200}{150}=\dfrac{x-9,8}{19,6-x}\)
Giải phương trình trên ta được x = 15,4
vậy nồng độ % của dung dịch A thu được là 15,4%