Cho 4,48 lít CO2 (đktc) vào 400ml dung dịch hỗn hợp KOH 0,25M và K2CO3 0,4M được dung dịch X. Cho dung dịch BaCl2 dư vào dung dịch X thu được kết tủa, lọc lấy kết tủa đem nung đến khối lượng không đổi thu được m gam chất rắn. Giá trị của m là ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nHCl = 0,4.0,5 = 0,2 mol; nH2SO4 = 0,08.0,5 = 0,04 mol
nH+ = nHCl + 2nH2SO4 = 0,28 mol
Đặt số mol của Zn và Mg trong hỗn hợp ban đầu là x và y (mol)
Ta có: 65x + 24y = 5,34 (1)
Zn + 2H+ → Zn2+ + H2
x → 2x → x (mol)
Mg + 2H+ → Mg2+ + H2
y → 2y → y (mol)
Dung dịch Y gồm có:
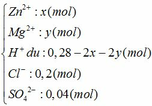
Ta thấy: nH+ + 2nZn2+ + 2nMg2+ (= 0,28 mol) < nNaOH (= 0,3 mol)
=> NaOH dư, Zn(OH)2 bị tan một phần
=> nNaOH hòa tan kết tủa = 0,3 – 0,28 = 0,02 mol
H+ + OH- → H2O
0,28-2x-2y → 0,28-2x-2y (mol)
Zn2+ + 2OH- → Zn(OH)2
x → 2x → x (mol)
Mg2+ + 2OH- → Mg(OH)2
y → 2y → y (mol)
Zn(OH)2 + 2OH- → ZnO22- + H2O
0,01 ← 0,02 (mol)
Khối lượng kết tủa thu được sau phản ứng: m kết tủa = mMg(OH)2 + mZn(OH)2
=> 99(x-0,01) + 58y = 8,43 <=> 99x + 58y = 9,42 (2)
Từ (1) và (2) ta có:

Ta có: nKOH : nBa(OH)2 = 0,4:0,05 = 8
Giả sử số mol của KOH và Ba(OH)2 lần lượt là 8a và a (mol)
=> nBa2+ = a (mol); nOH- = nKOH + 2nBa(OH)2 = 10a (mol)
- Khi kết tủa Mg(OH)2 và Zn(OH)2 đạt giá trị lớn nhất: nOH- = nH+ dư + 2nZn2+ + 2nMg2+
=> 10a = 0,04 + 2.0,06 + 2.0,06 => a = 0,028 mol
Ta thấy a < nSO42- => BaSO4 chưa đạt cực đại
- Giả sử sau khi Mg(OH)2 và Zn(OH)2 đạt cực đại ta thêm 8b mol KOH và b mol Ba(OH)2:
+ Lượng kết tủa sinh thêm là lượng BaSO4: nBaSO4 = nBa(OH)2 = b mol
=> mBaSO4 = 233b (gam)
+ Lượng kết tủa bị tan ra: nZn(OH)2 = nOH-: 2 = 10b : 2 = 5b (mol)
=> mZn(OH)2 = 99.5b = 495b (gam)
Ta thấy khối lượng kết tủa sinh ra nhỏ hơn khối lượng kết tủa bị tan nên khối lượng kết tủa lớn nhất là thời điểm Mg(OH)2 và Zn(OH)2 đạt cực đại. Khi đó: nBa(OH)2 = a = 0,028 mol
=> V = 0,028 : 0,05 = 0,56 (lít)
Kết tủa sau phản ứng gồm có:
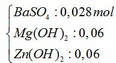
Mg(OH)2 → t ∘ MgO + H2O
0,06 mol → 0,06 mol
Zn(OH)2 → t ∘ ZnO + H2O
0,06 mol → 0,06 mol
=> m = mBaSO4 + mMgO + mZnO = 0,028.233 + 0,06.40 + 0,06.81 = 13,784 gam

gọi kim loại hóa trị II là Mpt pứ:M+2HCl−−−>MgCl2+H2Fe+2HCl−−−>FeCl2+H2dd X: MgCl2,FeCl2,HCldưThêm NaOH dư vào X và biết nó không tạo kết tủa với hidroxit nên ta có pt pứFeCL2+2NaOH−−−>Fe(0H)2+2NaCl4Fe(OH)2+02−−−>2Fe203+4H20n Fe203 = 0, 075 moltừ các pt pu --->n H2= n Fe= n FeCl

Đáp án A
Bài 21. Giải:
• X + nước dư → dung dịch Y + H2
=> Chứng tỏ X tan hết.
• Có n Ba = n H 2 = 1 , 344 22 , 4 = 0 , 06 mol
• Nhỏ từ từ đến 0,02 mol HCl thì thấy bắt đầu xuất hiện kết tủa, tức là OH - phản ứng vừa hết.
⇒ n OH - = 0 , 02 mol ⇒ n AlO 2 - = 0 , 06 . 2 - 0 , 02 = 0 , 1 mol
• Thêm 0,18 mol H2SO4:
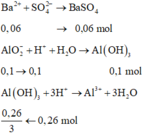
• Lọc kết tủa, nung đến khối lượng không đổi được:
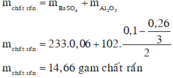




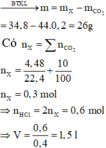
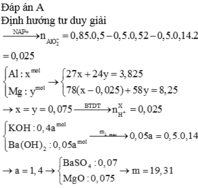
đổi 400ml=0,4 lít
nCO2=4,48/22,4=0,2(mol)
nKOH=0,25.0,4=0,1(mol)
nK2CO3=0,4.0,4=0,16(mol)
CO2 + 2KOH -> K2CO3 + 2H2O
ban đầu 0,2 0,1 0 (mol)
pứ 0,05 <---0,1 -----> 0,05 (mol)
sau pứ 0,15 0 0,05 (mol)
\(\Sigma\)nK2CO3=0,05+0,16=0,21(mol)
CO2 + K2CO3 +H2O-> 2KHCO3
bđ 0,15 0,21 0 (mol)
pứ 0,15--->0,15------------> 0,3 (mol)
sau pứ 0 0,06 0,3 (mol)
dd X gồm dd K2CO3 dư và dd KHCO3
BaCl2 + K2CO3 -> BaCO3\(\downarrow\) + 2KCl
0,06 ---------->0,06 (mol)
mCR=mBaCO3=0,06.197=11,82(g)=>m=11,82