A là 1 hợp kim gồm Zn, Cu được chia đôi. Phần 1 hoà tan bằng HCl dư thấy còn lại 1g không tan. Phần 2 được thêm vào đó 4g Cu để được hh B thì % lượng Zn trong B nhỏ hơn % lượng Zn trong A là 33,33%.tìm %lượng Cu trong A. Biết rằng khi ngâm B vào dd Naoh thì sau1 thời gian Vh2 thoát ra vượt quá 0,6l đktc
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Do cả 3 kim loại đều tạo hợp chất hóa trị 2 nên ta đặt công thức chung cho oxit là MO, công thức chung cho muối là MCl2. Rõ ràng ta thấy là số nguyên 2 công thức chỉ khác nhau ở chỗ O và Cl2, tức là thế 1 O = 2 Cl sẽ thu được muối (số mol nguyên tử Cl hay Cl- = 2 lần số mol O).
Khối lượng Oxi thu vào để tạo Oxit là:
mO = 44,6 – 28,6 = 16 g
nO = 16/16 = 1 mol (ở đây tính số mol của nguyên tử Oxi chứ không phải phân tử O2)
\(\Rightarrow n_{Cl^-}\) = 2 mol
Khối lượng Cl- xem như bằng khối lượng Cl do khối lượng electron không đáng kể
\(\Rightarrow m_{Cl^-}\) = \(2.35,5\) = 71g
\(\Rightarrow\)Tổng khối lượng kim loại ban đầu sẽ tạo thành muối trong dung dịch (do tan hết trong axit)
\(\Rightarrow\)Tổng khối lượng muối = khối lượng kim loại + Khối lượng Cl-
= 28,6 + 71 = 99,6 g
ĐA= 99,6g

Mg + 2HCl = MgCl2 +H2
x x
2Al + 6HCl= 2AlCl3 + 3H2
y y
2Cu + O2 = 2CuO
z z = 8/80 = 0,1 mol
3NaOH + AlCl3 = Al(OH)3 + 3NaCL
y y
Al(OH)3 + NaOH = NaALO2 + 2H2O
y y
2NaOH + MgCl2 = Mg(OH)2 + 2NaCl
x x
Mg(OH)2 = MgO + H2O
x x = 4/40 = 0,1 mol
=>mCu= 0,1*64=6,4
mMg=0,1*24=2,4
mAl=10-6,4-2,4=1,2

\(n_{H_2}=0.065\left(mol\right)\)
\(2H^++2e\rightarrow H_2\)
\(O_2+4e\rightarrow2O^{2-}\)
\(n_{O_2}=\dfrac{2\cdot0.065}{4}=0.0325\left(mol\right)\)
\(BTKL:\)
\(m_{oxit}=\dfrac{2.29}{2}+0.0325\cdot32=2.185\left(g\right)\)

Đáp án A
Ta có: mFe = 40%.m = 0,4m (g) → mCu = m - 0,4m = 0,6m (g)
Sau phản ứng còn 0,65m (g) kim loại > mCu = 0,6m (g)
Khối lượng Fe còn dư: 0,65m - 0,6m = 0,05m (g)
Vậy: mFe phản ứng = 0,4m - 0,05m = 0,35m (g)
Do Fe còn dư sau phản ứng nên tạo thành muối Fe2+
Quá trình nhường electron:
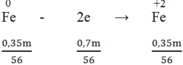
Quá trình nhận electron:
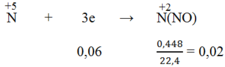
Áp dụng định luật bảo toàn electron, ta có:
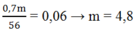
Ta có:
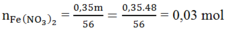
![]()

Đáp án B
Cho Cu vào dung dịch thấy tan ra và có màu xanh chứng tỏ trong dung dịch có Fe3+: Cu + 2Fe3+ → 2Fe2+ + Cu2+
Cho KMnO4 vào thấy dung dịch bị mất màu → chứng tỏ dung dịch có cả Fe2+ (xảy ra phản ứng oxi hóa khử giữa Fe2+ và KMnO4 do Mn(+7) + 5e → Mn+2 và Fe+2 → Fe+3+ 1e

Đáp án B
Cho Cu vào dung dịch thấy tan ra và có màu xanh chứng tỏ trong dung dịch có Fe3+: Cu + 2Fe3+ → 2Fe2+ + Cu2+
Cho KMnO4 vào thấy dung dịch bị mất màu → chứng tỏ dung dịch có cả Fe2+ (xảy ra phản ứng oxi hóa khử giữa Fe2+ và KMnO4 do Mn (+7) + 5e → Mn+2 và Fe+2 → Fe+3+ 1e
