g. Nguyên tử khối trung bình của Cu là 63,54. Đồng có 2 đồng vị. Biết đồng vị 1 là Cu chiếm 73%. Tìm đồng vị thứ 2. Hỏi khi có 54 nguyên tử đồng vị 2 thì sẽ có bao nhiêu nguyên tử Cu
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a), Đặt đồng vị thứ 2 của đồng là A2.
\(\overline{NTK}_{Cu}=63,54\\ \Leftrightarrow\dfrac{63.73\%+A_2.27\%}{100\%}=63,54\\ \Leftrightarrow A_2=65\left(đ.v.C\right)\)
b, Khi có 81 nguyên tử đồng vị thứ 2 thì số nguyên tử 63Cu là:
\(\dfrac{81.73}{27}=219\left(nguyên.tử\right)\)
c) Phần trăm khối lượng đồng vị 63Cu có trong phân tử Cu2O là:
\(73\%.\dfrac{63,54.2}{63,54.2+16}\approx64,837\%\)

Ta có: \(\overline{M}=\dfrac{63.73+x.\left(100-73\right)}{100}\Leftrightarrow x=\dfrac{100.63,54-63.73}{100-73}=65\)
Đồng vị thứ hai là \(^{65}_{29}Cu\)

Đặt số khối đồng vị còn lại là `x`
`\%` Đồng vị còn lại là `100-73=27\%`
`->M_{Cu}={63.73+27x}/{100}=63,54`
`->x=65`
Vậy đồng vị còn lại là \(_{29}^{65}Cu\)

Đáp án B.
Gọi số khối của hai đồng vị X, Y là A1 và A2; phần trăm số nguyên tử của hai đồng vị này là x1 và x2. Theo giả thiết ta có:
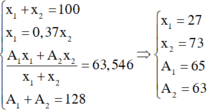

Đáp án A
Gọi số khối của đồng vị X, Y lần lượt là x, y
Chú ý Số nguyên tử đồng vị X = 0,37 số nguyên tử đồng vị Y nên nếu có 1 nguyên tử Y thì có 0,37 nguyên tử X
Ta có hệ:
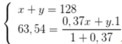
⇒
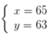
Vậy số notron của đồng vị Y hơn số notron của đồng vị X là : 65- 63 = 2

Gọi x là số phần trăm của đồng vị 63Cu
Suy ra phần trăm đồng vị 65Cu là 100 – x
M = [63.x + 65(100 – x)]/100 = 63,546
<=> x = 72,7%
Từ đây dễ dàng tìm được % của 63Cu trong tinh thể CuSO4.5H2O là 18,43%
=> Đáp án D