Cho 9,8 tấn H2SO4 tác dụng với Ca3(PO4)2 dư, người ta thu được 20,24 tấn supe photphat đơn. Hãy tính hiệu suất của quá trình?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Câu 1:
Ta có: 1 tấn = 1000 kg
⇒ mFe = 1000.95% = 950 (kg)
\(\Rightarrow n_{Fe}=\dfrac{950}{56}\left(kmol\right)\)
BTNT Fe, có: \(n_{Fe_2O_3\left(LT\right)}=\dfrac{1}{2}n_{Fe}=\dfrac{475}{56}\left(kmol\right)\)
Mà: H = 80% \(\Rightarrow n_{Fe_2O_3\left(TT\right)}=\dfrac{475}{56}:80\%=\dfrac{2375}{224}\left(kmol\right)\)
\(\Rightarrow m_{Fe_2O_3\left(TT\right)}=\dfrac{2375}{224}.160=\dfrac{11875}{7}\left(kg\right)\)
⇒ m quặng \(=\dfrac{m_{Fe_2O_3}}{60\%}\approx2827,38\left(kg\right)\)
Câu 2:
Ta có: 65nZn + 27nAl = 3,79 (1)
PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Theo PT: \(n_{H_2}=n_{Zn}+\dfrac{3}{2}n_{Al}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=0,05\left(mol\right)\\n_{Al}=0,02\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=0,05.65=3,25\left(g\right)\\m_{Al}=0,02.27=0,54\left(g\right)\end{matrix}\right.\)

\(n_{Ca\left(H_2PO_4\right)_2}=\dfrac{234}{234}=1\left(kmol\right)\)
Từ PTHH ta thấy :
\(n_{Ca_3\left(PO_4\right)_2}=\dfrac{1}{3}\left(kmol\right)\)
\(n_{Ca_3\left(PO_4\right)_2\left(tt\right)}=\dfrac{1}{3\cdot80\%}=\dfrac{5}{12}\left(kmol\right)\)
\(m_{Ca_3\left(PO_4\right)_2}=\dfrac{5}{12}\cdot310=\dfrac{775}{6}\left(kg\right)\)
\(m_{quặng}=\dfrac{775}{6\cdot38.75\%}=333.3\left(kg\right)\)

Đáp án B
Giả sử m = 1 kg = 1000g => mCa3(PO4)2=930 gam => nCa3(PO4)2= 930/310 = 3mol
Ca3(PO4)2+2H2SO4 (đặc)→Ca(H2PO4)2+2CaSO4↓
3 3
Ca(H2PO4)2→P2O5
3 3
=> %mP2O5 = 3.142/1000=42,6%
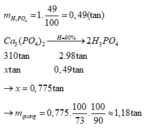
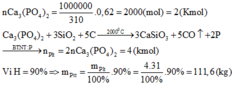
2H2SO4 + Ca3(PO4)2 -------> Ca(H2PO4)2 + 2CaSO4
10^5mol ........5,10^4mol ...........10^5mol
Số mol H2SO4=9,8*10^6/98=10^5mol
KL Supephotphat đơn thu được (lý thuyết)=5,10^4*234+10^5*136=25,3*10^6(g)= 253tấn
H% :20,24/25,3*100=80%