Hòa tan m gam Potassium oxide (K2O) vào nước ta thu được 150g dung dịch A có nồng độ 11,2 %. Tính giá trị của m.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Sửa đề: 9,2 gam Na
\(a,n_{Na_2O}=\dfrac{9,2}{23}=0,4\left(mol\right)\)
PTHH: \(Na_2O+H_2O\rightarrow2NaOH\)
0,4------------------>0,8
\(\rightarrow C_{M\left(NaOH\right)}=\dfrac{0,8}{0,5}=1,6M\)
\(b,n_{K_2O}=\dfrac{37,6}{94}=0,4\left(mol\right)\)
PTHH: \(K_2O+H_2O\rightarrow2KOH\)
0,4----------------->0,8
\(\rightarrow C\%_{KOH}=\dfrac{0,8.56}{362,4+37,6}.100\%=11,2\%\)

Chọn đáp án C
Bình 1 tăng 2,52 ⇒ nH2O = 0,14 mol.
+ Bình 2 tăng 4,4 gam ⇒ nCO2 = 0,1 mol.
+ Nhận thấy nH2O > nCO2 ⇒ 2 CxHy thuộc dãy đồng đẳng của ankan.
⇒ nHỗn hợp ankan = 0,14 – 0,1 = 0,04 mol
⇒ C trung bình = 0,1 ÷ 0,04 = 2,5 ⇒ Chọn C

Chọn đáp án A.
n K 2 O = 9 , 4 94 = 0 , 1 m o l
![]()
![]()
→ B T K L mdung dịch sau phản ứng = 80 gam
![]()

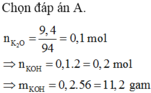
mdung dịch sau phản ứng = 9,4 + 70,6 = 80 gam
C % = 11 , 2 80 . 100 % = 14 %

Chọn đáp án B
K2O + H2O → 2KOH
Ta có nK2O = 0,1 mol ⇒ nKOH = 0,2 mol.
⇒ mKOH = 11,2 gam.
⇒ C%KOH = 11 , 2 9 , 4 + 70 , 6 × 100 = 14%.
⇒ Chọn B

Chọn đáp án B
K2O + H2O → 2KOH
Ta có nK2O = 0,1 mol ⇒ nKOH = 0,2 mol.
⇒ mKOH = 11,2 gam.
⇒ C%KOH = 11 , 2 9 , 4 + 70 , 6 × 100 = 14%.

\(K_2O+H_2O\rightarrow2KOH\)
\(n_{K_2O}=\dfrac{47}{94}=0,5\left(mol\right)\)
\(\Rightarrow n_{KOH}=2.n_{K_2O}=1\left(mol\right)\)
\(\Rightarrow m_{KOH}=56\left(g\right)\)
\(C\%KOH=\dfrac{56}{47+106}.100\%\simeq36,6\%\)
Khối lượng K2O ban đầu: 47 gam.Khối lượng nước: 106 gam.Khối lượng KOH (Kali Hydroxide) = Khối lượng K2O (Kali Oxide).Tổng khối lượng dung dịch = Khối lượng K2O + Khối lượng nước = 47 gam + 106 gam = 153 gam.
Nồng độ phần trăm KOH = (Khối lượng KOH / Tổng khối lượng dung dịch) x 100 Nồng độ phần trăm KOH = (47 gam / 106 gam) x 100 ≈ 36.6%
Vậy nồng độ phần trăm của dung dịch KOH thu được là khoảng 36,6%.
\(K_2O+H_2O\rightarrow2KOH\\ n_{KOH}=\dfrac{150.11,2\%}{56}=0,3\left(mol\right)\\ n_{K_2O}=\dfrac{0,3}{2}=0,15\left(mol\right)\\ m_{K_2O}=0,15.94=14,1\left(g\right)\\ \Rightarrow m=14,1\left(g\right)\)