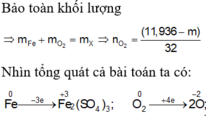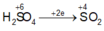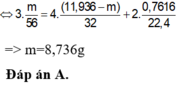Để m gam bột sắt (A) ngoài không khí, sau 1 thời gian biến thành hỗn hợp B có khối lượng 12 g gồm Fe,FeO,Fe3O4, Fe2O3. Cho B tác dụng hoàn toàn với 200 ml dung dịch HNO3thấy sinh ra 2.24 lít khí NO duy nhất. Tính m, CM HNO3
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


2Fe +O2 --> 2FeO(1)
4Fe +3O2 -->2Fe2O3 (2)
3Fe + 2O2 -->Fe3O4 (3)
Fe +4HNO3 --'> Fe(NO3)3 +NO +2H2O(4)
3FeO +10HNO3 --> 3Fe(NO3)3 +NO +5H2O (5)
3Fe3O4 +28HNO3 --> 3Fe(NO3)3 +NO +14H2O(6)
giả sử nFe= a(mol)
nFeO=b(mol)
nFe2O3=c(mol)
nFe3O4=d(mol)
=> 56a+72b+160c+232d =12 (I)
theo (4) :nNO=nFe=a(mol)
theo(5) : nNO=1/3 nFeO=1/3c(mol)
theo (6) : nNO=1/3 nFe3O4=1/3d(mol)
=> a+1/3c+1/3d=2,24/22,4=0,1(II)
nhân (II) với 56 rồi lấy (I) trừ (II) ta có :
\(\dfrac{56a+72b+160c+232d}{56a+\dfrac{56}{3}c+\dfrac{56}{3}d}=\dfrac{160}{3}b+160c+\dfrac{640}{3}d\)
\(\Leftrightarrow\)b+3c+4d=0,12
ta có :
nO(trong FeO)=nFeO=b(mol)
nO(trongFe2O3)=3nFe2O3=3c(mol)
nO(trong Fe3O4)=4nFe3O4=4d(mol)
=> mFe(ban đầu)= \(12-16\left(b+3c+4d\right)\)
= \(12-16.0,12=10,08\left(g\right)\)

Coi : B gồm : Fe ( x mol) , O ( y mol)
\(m_B=56x+16y=12\left(h\right)\left(1\right)\)
\(n_{SO_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
Bảo toàn e :
\(3x=2y+0.15\cdot2\left(2\right)\)
\(\left(1\right),\left(2\right):x=0.18,y=0.12\)
\(m_{Fe}=0.18\cdot56=10.08\left(g\right)\)
Quy đổi hỗn hợp về Fe và O.
Giả sử: \(\left\{{}\begin{matrix}n_{Fe}=x\left(mol\right)\\n_O=y\left(mol\right)\end{matrix}\right.\)
⇒ 56x + 16y = 12 (1)
Ta có: \(n_{SO_2}=0,15\left(mol\right)\)
Theo ĐLBT mol e, có: 3x - 2y = 0,15.2 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,18\left(mol\right)\\y=0,12\left(mol\right)\end{matrix}\right.\)
⇒ mFe = 0,18.56 = 10,08 (g)
Bạn tham khảo nhé!

Cách này ko cần viết phương trình :3
Quy đổi hh gồm Fe (a mol) và O (b mol)
\(\Rightarrow56a+16b=30\) (1)
Ta có: \(n_{NO}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Bảo toàn electron: \(3n_{Fe}=2n_O+3n_{NO}\) \(\Rightarrow3a-2b=0,75\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,45\\b=0,3\end{matrix}\right.\)
Vì mFe trong oxit cũng là mFe ban đầu \(\Rightarrow m_{Fe}=0,45\cdot56=25,2\left(g\right)\)

Quy đổi hỗn hợp thành : Fe ( x mol ) , O ( y mol )
\(m=56x+16y=12\left(g\right)\left(1\right)\)
Bảo toàn e :
\(3x=0.1\cdot3+2y\left(2\right)\)
\(\left(1\right),\left(2\right):x=0.18,y=0.12\)
\(m_{Fe}=0.18\cdot56=10.08\cdot\left(g\right)\)
\(m_{Fe\left(NO_3\right)_3}=0.18\cdot242=43.56\left(g\right)\)

Đáp án B
Xét giai đoạn A tác dụng với H2SO4 đặc, nóng, dư:
Số mol SO2 thu được là: n SO 2 = 0 , 15 mol
Qui đổi hỗn hợp A thành Fe : a mol; O : b mol
![]()
Sơ đồ phản ứng :
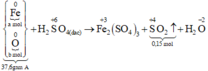
Các quá trình nhường, nhận electron:
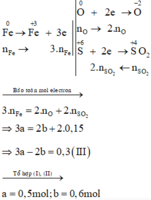
Xét giai đoạn để m gam Fe ngoài không khí:
Sơ đồ phản ứng :


Đáp án : A
nFe(OH)3 = 0,1 mol = nFe bđ => mO(X) = 4g
Qui X về 0,1 mol Fe và 0,25 mol O
Bảo toàn e : 3nFe = 2nO + 3nNO
=> nNO < 0 (Vô lý)
=> Fe3+ còn dư so với OH-
=> nOH- = nHNO3 dư + 3nFe(OH)3 => nHNO3 dư = 0,05 mol
=> nHNO3 pứ = 0,6 – 0,05 = 0,55 mol
Bảo toàn e : 3nFe = 2nO + 3nNO ; nHNO3 = 3nFe + nNO
Lại có : 56nFe + 16nO = 9,6g
=> nFe = 0,15 ; nO = 0,075 mol => nNO = 0,1 mol
=> V= 2,24 lit

a, \(2Fe+O_2\underrightarrow{t^o}2FeO\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(4Fe+3O_2\underrightarrow{t^o}2Fe_2O_3\)
\(2Fe+6H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
\(2FeO+4H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+SO_2+4H_2O\)
\(2Fe_3O_4+10H_2SO_{4\left(đ\right)}\underrightarrow{t^o}3Fe_2\left(SO_4\right)_3+SO_2+10H_2O\)
\(Fe_2O_3+3H_2SO_{4\left(đ\right)}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3H_2O\)
b, Ta có: mO2 = 3,2 (g) \(\Rightarrow n_{O_2}=\dfrac{3,2}{32}=0,1\left(mol\right)\)
\(n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
BT e, có: 3nFe = 4nO2 + 2nSO2
⇒ nFe = 0,2 (mol)
⇒ mFe = 0,2.56 = 11,2 (g)