Hòa tan hoàn toàn 93,15g R trong dung dịch HNO3 theo sơ đồ phản ứng: R + HNO3 ---> R(NO3)2 + NO +H2O Biết thể tích NO thu đc (đktc) là 6,72 lít. Xác định R?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, Ta có: \(n_{NO}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
Theo ĐLBT e, có: 2nR = 0,02.3 ⇒ nR = 0,03 (mol)
\(\Rightarrow M_R=\dfrac{1,92}{0,03}=64\left(g/mol\right)\)
Vậy: R là Cu.
b, Ta có: nHNO3 (pư) = 4nNO = 0,08 (mol)
Mà: HNO3 dùng dư 10% so với lượng cần pư.
⇒ nHNO3 = 0,08 + 0,08.10% = 0,088 (mol)
\(\Rightarrow C_{M_{HNO_3}}=\dfrac{0,088}{0,1}=0,88\left(M\right)\)

Chọn đáp án B
Gọi hóa trị của kim loại R là n. Áp dụng đl bảo toàn e ta có.
nR × n = 3nNO ⇔ 4 , 8 n R = 0 , 15 ⇔ R = 32n
⇒ R là Cu ứng với n=2 ⇒ Chọn B

Đáp án D
Gọi n là số oxi hóa của M trong sản phẩm tạo thành.
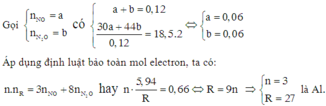

PTHH: 3R + 8HNO3 -> 3R(NO3)2 + 2NO + 4H2O
Ta có: nNO = 0,3mol
Theo PTHH: => nR = 3/2nNO = 0,45mol
=> MR=92,15/0,45=204,77
ĐỀ SAI RỒI, EM KIỂM TRA LẠI ĐI NHÉ.

\(n_{H2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Pt : \(R+2HCl\rightarrow RCl_2+H_2\)
\(n_R=n_{H2}=0,3\left(mol\right)\Rightarrow M_R=\dfrac{16,8}{0,3}=56\left(Fe\right)\)
Vậy kim loại R là sắt

mdd HNO3=592,2g
--> nHNO3=0,94 mol
Gọi x,y lần lượt là số mol từng khí
x+y=0,12
44x+30yx+y=18,5.244x+30yx+y=18,5.2
x=y=0,06 mol
Bảo toàn e
5,94R.3=0,06.8+0,06.35,94R.3=0,06.8+0,06.3
--> R=27 --> Al
Các chất trong dd A gồm Al(NO3)3 và HNO3 dư
mdd sau phản ứng=5,94+592,2-0,06.44-0,06.30=593,7
CC
nHNO3 phản ứng=0,22.3+0,06.2+0,06=0,84 ( bảo toàn N)
--> CCHNO3 dư=(0,94−0,84).63593,7=1,06
3R+8HNO3\(\rightarrow\)3R(NO3)2+2NO+4H2O
\(n_{NO}=\dfrac{6,72}{22,4}=0,3mol\)
\(n_R=\dfrac{3}{2}n_{NO}=\dfrac{3}{2}.0,3=0,45mol\)
MR=\(\dfrac{93,15}{0,45}=207\left(Hg\right)\)