Cho 17.04 gam hỗn hợp gồm Fe, FeO, Fe 2O3 và Fe3O4 phản ứng hết với dung dịch HNO 3 loãng dư thu được 2,016 lít khí NO (sản phẩm khử duy nhất ở đktc) v à dung dịch X. Cô cạn dung dịch X thu được m gam muối khan. Giá trị của m l à :
53,25. B. 51,9. C. 73,635. D. 58,08

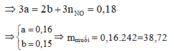
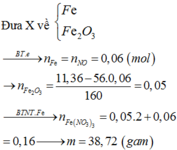
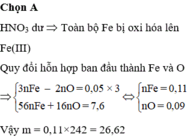



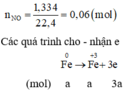

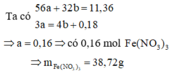
Giả sử hỗn hợp gồm Fe (x mol) và O (y mol)
\(n_{NO}=0,09\left(mol\right)\\ m_{hh}=m_{Fe}+m_O\\ \Leftrightarrow56x+16y=17,04\left(1\right)\)
Qúa trình trao đổi e:
\(Fe^0\rightarrow Fe^{+3}+3e\\ O^0+2e\rightarrow O^{-2}\\ N^{+5}+3e\rightarrow N^{+2}\)
Áp dụng ĐLBT e:
\(3n_{Fe}=2.n_O+3.n_{NO}\\ \Leftrightarrow3x=2y+3.0,09\\ \rightarrow3x-2y=0,27\left(2\right)\)
Từ (1), (2) giải được: x=0,24; y=0,225
Bảo toàn nguyên tố Fe:
\(n_{Fe\left(NO_3\right)_3}=n_{Fe}=0,24\left(mol\right)\\ \Rightarrow m_{muối}=m_{Fe\left(NO_3\right)_3}=242.0,24=58,08\left(g\right)\)
Vậy: CHỌN D