Nguyên tố X có 3 đồng vị là A1 chiếm 92,3 % , A2 chiếm 4,7 % , A3 chiếm 3%(về số nguyên tử).Tổng số khối của 3 đồng vị là 87. Số notron trong A2 nhiều hơn trong A1 là 1 hạt . Khối lượng nguyên tử trung bình của X là 28,107 đvC.
a, Hãy tìm số khối các đồng vị.
b, Biết trong A1 có số proton bằng số notron .Hãy tìm số notron trong mỗi đồng vị.

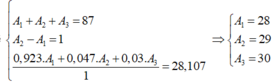
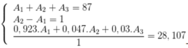
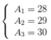
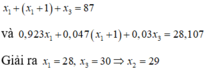
A1+A2+A3=87(1)
A2-A1=1(2)
\(\dfrac{92,3A_1+4,7A_2+3A_3}{100}=28,107\)
92,3A1+4,7A2+3A3=2810,7(3)
Giải hệ phương trình 1,2,3 ta được:
A1=28, A2=29 , A3=30
- Trong A1: A1=P1+N1=28 , do P1=N1 nên P1=N1=14
- Trong A2:
N2=N1+1=14+1=15\(\rightarrow\)P2=A2-N2=29-15=14
- Trong A3=30:
P3=14\(\rightarrow\)N3=16