1/ Cho hỗn hợp Zn và Mg tác dụng với 30ml dung dịch H2SO4 đặc nóng dư thu đc 100,4g muối khan và 44,8g SO2
a/tính khối lượng mỗi kim loại trong hỗn hợp ban đầu
b/để trung hòa lượng Axit dư thì cần 4g NAOH.Tính CM H2SO4 đã dùng.

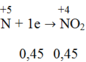
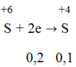
\(a)\)\(Zn\left(a\right)+2H_2SO_{4\left(đđ\right)}-t^o->ZnSO_4\left(a\right)+SO_2\left(a\right)+2H_2O\)
\(Mg\left(b\right)+2H_2SO_{4\left(đđ\right)}-t^o->MgSO_4\left(b\right)+SO_2\left(b\right)+2H_2O\)
Ta có: \(\left\{{}\begin{matrix}161a+120b=100,4\\a+b=0,7\end{matrix}\right.\)\(\Rightarrow\left\{{}\begin{matrix}a=0,4\left(mol\right)\\b=0,3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m\)mỗi kim loại.
\(b)\)\(n_{NaOH}=0,1\left(mol\right)\)
\(H^+\left(0,1\right)+OH^-\left(0,1\right)\rightarrow H_2O\)
\(\Rightarrow n_{H_2SO_4}=\dfrac{1}{2}n_{H^+}=0,05\left(mol\right)\)
\(\Rightarrow\left[H_2SO_4\right]=\dfrac{5}{3}\left(M\right)\)
Kí hiệu [X] hay dùng để kí hiệu nồng độ của các chất ở trạng thái cân bằng trong quá trình phân lí