Một loại đá chứa CaCO3, MgCO3, Al2O3,( các chất khác không đáng kể) khối lượng của Al2O3=1/8 khối lượng cacbonat. Đem nung đá ở nhiệt độ cao 1200 độ C ta thu được chất rắn có khối lượng =6/10 khối lượng đá trước khi nung. Tính thành phần phần trăm MgCO3 trong đá
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi \(n_{CaCO_3}=x\left(mol\right);n_{MgCO_3}=y\left(mol\right)\)
\(m_{Al_2O_3}=\dfrac{100x+84y}{10}\)
Bảo toàn Ca \(\Rightarrow n_{CaO}=n_{CaCO_3}=x\left(mol\right)\)
Bảo toàn Mg \(\Rightarrow n_{MgO}=n_{MgCO_3}=y\left(mol\right)\)
\(\Rightarrow m_Y=m_{CaO}+m_{MgO}+m_{Al_2O_3}\)\(=56x+40y+\dfrac{100x+84y}{10}\)
\(\Rightarrow56x+40y+\dfrac{100x+84y}{10}=56,8\%.m_X=56,8\%.\dfrac{11}{10}.\left(100x+84y\right)\)
\(=\dfrac{781}{1250}.\left(100x+84y\right)\)\(\Leftrightarrow56x+40y=\dfrac{328}{625}\left(100x+84y\right)\)
\(\Leftrightarrow x=\dfrac{29}{25}y\)
\(\%m_{CaCO_3}=\dfrac{100x}{\dfrac{11}{10}.\left(100x+84y\right)}.100\%=\dfrac{100.\dfrac{29}{25}y}{\dfrac{11}{10}.\left(100.\dfrac{29}{25}y+84y\right)}.100\%\approx52,73\left(\%\right)\)
\(\%m_{MgCO_3}=\dfrac{84y}{\dfrac{11}{10}.\left(100x+84y\right)}.100\%=\dfrac{84y}{\dfrac{11}{10}.\left(100.\dfrac{29}{25}y+84y\right)}.100\%\approx38,18\left(\%\right)\)
\(\Rightarrow\%m_{Al_2O_3}\approx9,09\left(\%\right)\)

Đáp án : B
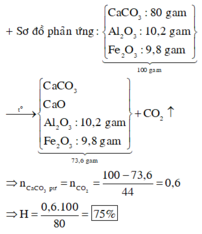
Giả sử khối lượng đá vôi là 100g
=> mCaCO3 = 80g => nCaCO3 = 0,8 mol
=> msau = 73,6g => mtrước – msau = 100 – 73,6 = mCO2
=> nCO2 = nCaCO3 pứ = 0,6 mol
=> H%pứ = 75%

Gọi KL của Al2O3 là x g thì KL muối Cacbonat là 8x g
=> KL hỗn hợp là 9x g
Do sau phân hủy thì khối lượng còn 6/10 ban đầu
=> KL CO2 bay đi là \(9x\left(1-\dfrac{6}{10}\right)=3,6x\)
Khi đó số mol muối cacbonat = số mol của CO2 = \(\dfrac{3,6x}{44}\)
Giờ ta giả sử cho dễ tính toán nha, để số tròn thì mình lấy x=11
Tổng khối lượng muối cacbonat là 88g => 100a + 84b = 88 (1)
Tổng số mol muối cacbonat là 0,9 mol => a + b = 0,9 (2)
Từ (1) và (2) ta có => a = 0,775 mol; b = 0,125 mol
=> %KL MgCO3 = \(\dfrac{\left(84x0,125\right)x100\%}{99}=10,6\%\)
a)
$CaCO_3 \xrightarrow{t^o} CaO + CO_2$
$MgCO_3 \xrightarrow{t^o} MgO + CO_2$
b)
Coi m hh = 102(gam)
Suy ra : m Al2O3 = 102/8 = 12,75(gam)
Gọi n CaCO3 = a(mol) ; n MgCO3 = b(mol)
=> 100a + 84b + 12,75 = 102(1)
m hh sau = 102.6/10 = 61,2(gam)
Bảo toàn khối lượng :
m CO2 = 102 -61,2 = 40,8(gam)
=> a + b = 40,8/44 = (2)
Từ (1)(2) suy ra a = 0,71 ; b = 153/704
Suy ra :
m MgCO3 = 153/704 .84 = 18,25(gam)
%m MgCO3 = 18,25/102 .100% = 17,9%

\(Đặt:m_{Al_2O_3}=g\left(g\right)\Rightarrow m_{CaCO_3}+m_{MgCO_3}=8g\left(g\right)\\ PTHH:CaCO_3\rightarrow\left(t^o\right)CaO+CO_2\\ MgCO_3\rightarrow\left(t^o\right)CO_2+MgO\\ Đặt:n_{CaCO_3}=a\left(mol\right);n_{MgCO_3}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}100a+84b=8g\\56a+40b+g=60\%.9g=5,4g\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}a=\dfrac{31}{440}g\\b=\dfrac{1}{88}g\end{matrix}\right.\\ \Rightarrow\%m_{Al_2O_3}=\dfrac{g}{9g}.100\%=11,111\%\)
\(\%m_{MgCO_3}=\dfrac{\dfrac{1}{88}g.84}{9g}.100\%\approx10,606\%\\ \%m_{CaCO_3}=\dfrac{\dfrac{31}{440}g.100}{9g}.100\approx78,283\%\)
\(b,\%m_{\dfrac{Al_2O_3}{A}}=\dfrac{g}{\dfrac{1}{88}.40g+\dfrac{31}{440}.56g+g}.100\approx18,5185\%\\ \%m_{\dfrac{MgO}{A}}=\dfrac{\dfrac{1}{88}.40g}{\dfrac{1}{88}.40g+\dfrac{31}{440}.56g+g}.100\approx8,4175\%\\ \Rightarrow m_{Al_2O_3}=18,5185\%.2=0,37037\left(g\right)\Rightarrow n_{Al_2O_3}=\dfrac{0,37037}{102}\left(mol\right)\\ m_{MgO}=8,4175\%.2=0,16835\left(g\right)\\ \Rightarrow n_{MgO}=\dfrac{0,16835}{40}\left(mol\right)\\ m_{CaO}=2-\left(0,37037+0,16835\right)=1,46128\left(g\right)\\ \Rightarrow n_{CaO}=\dfrac{1,46128}{56}\left(mol\right)\)
\(PTHH:Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\\ CaO+2HCl\rightarrow CaCl_2+H_2O\\ MgO+2HCl\rightarrow MgCl_2+H_2O\\ n_{HCl}=2.\left(\dfrac{1,46128}{56}+\dfrac{0,16835}{40}\right)+6.\dfrac{0,37037}{102}\approx0,0824\left(mol\right)\\ \Rightarrow V_{ddHCl}\approx\dfrac{0,0824}{0,5}\approx0,1648\left(lít\right)\approx164,8\left(ml\right)\)

a) \(CaCO_3\rightarrow^{t^0}CaO+CO_2\left(1\right)\)
\(MgCO_3\rightarrow^{t^0}MgO+CO_2\left(2\right)\)
Đặt a, x, y là số gam của Al2O3, CaCO3, MgCO3 trong hỗn hợp X.
Theo gt: \(m_{Al_2O_3}=\dfrac{1}{10}m\left(MgCO_3;CaCO_3\right)\Rightarrow x+y=10a\left(I\right)\)
Vậy mA = 10a + a = 11a gam. ( Chất rắn Y gồm: MgO; CaO; Al2O3
Theo gt: \(m_B=\dfrac{56,80}{100}m_A=6,248a\left(gam\right)\)
Vậy: \(\dfrac{56.x}{100}+\dfrac{40.y}{84}=6,248a-a=5,248a\left(II\right)\)
Giải hệ: \(\left(I;II\right)\Rightarrow x=5,8a\)
Vậy %mCaCO3 = \(\dfrac{5,8a.100}{11a}=52,73\%\)
\(\%m_{Al_2O_3}=\dfrac{a.100}{11a}=9,09\%\)
\(\%m_{MgCO_3}=38,18\%\)

Cho lượng hh bđ là 100 g => mAl2O3 = 10,2 g ; mFe2O3 = 9,8 g ; mCaCO3 = 80 g
PTHH. CaCO3 -> CO2 + CaO
Độ giảm khối lượng = 100 - 67 = 33 g chính là mCO2
=> nCO2 = 33/44 = 0,75 mol
Theo pt: nCaCO3 pư = nCO2 = 0,75 mol
=> mCaCO3 pư = 0,75 .100 = 75 g ; mCaCO3 dư = 5 g
nCaO = nCO2 = 0,75 mol
=>mCaO = 0,75 . 56 = 42 g
Vậy mAl2O3 = 10,2 g ; mFe2O3 = 9,8 g ; mCaCO3 pư = 75g
mCaCO3 dư = 5 g ; mCaO = 42 g

Giả sử loại đá vôi ban đầu nặng 100g
=> mCaCO3 = 95g ; mMgCO3 =1,28 g ; m tạp chất trơ = 3,72 gam
=> nCaCO3 = \(\dfrac{95}{100}\)=0,95 mol; nMgCO3 = \(\dfrac{1,28}{24}=0,015\left(mol\right)\)mol
Khi nung thì xảy ra phản ứng:
CaCO3 ––(t°)––> CaO + CO2 ↑
MgCO3 ––(t°)––> MgO + CO2 ↑
Ta có: nCO2 = 0,95+0,015=0,965cmol
Nếu đá vôi bị phân hủy hoàn toàn thì khối lượng giảm:
0,965.44=42,46g
Vì khối lượng chất rắn thu được giảm 40,22%
=> m giảm =100.44,22%= 40,22g
Vậy tỉ lệ đá vôi bị phân hủy là \(\dfrac{40,22}{42,46}.100=94,72\%\)