giúp ạa , camon nhiều ạa 
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



\(a,D=\dfrac{m}{V}=\dfrac{3,9}{0,5}=7,8\left(\dfrac{kg}{dm^3}\right)=7800\left(\dfrac{kg}{m^3}\right)=7,8\left(\dfrac{g}{cm^3}\right)\)
b, Vậy khối kim loại trên là một khối sắt
c, \(d=10D=10.7800=78000\left(\dfrac{N}{m^3}\right)\)

b: kẻ đường kính AD
góc ACD=90 độ=góc ABD
=>AC vuông góc CD và AB vuông góc BD
=>BH//CD và CH//BD
=>BDCH là hbh
=>H,N,D thẳng hàng và N là trung điểm của HD
=>NT là đường trung bình của ΔAHD
=>NT//AD và NT=1/2AD=OA
=>NT//OA
=>ATNO là hbh
EN=1/2BC
=>EN=BN
=>ΔNEB cân tại N
=>góc NBE=góc NEB
EJ=1/2AH=JH
=>ΔJEH cân tại J
=>góc JEH=góc JHE
góc NBE+Góc ACB=90 độ
góc HAC+góc ACB=90 độ
=>góc NBE=góc HAC
mà góc JHE+góc HAC=90 độ
nên góc JHE+góc NBE=90 độ
=>góc JEN=90 độ



Ta có: \(n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a. PTHH:
Na2SO3 + H2SO4 ---> Na2SO4 + SO2 + H2O (1)
K2SO3 + H2SO4 ---> K2SO4 + SO2 + H2O (2)
Theo PT(1,2): \(n_{H_2SO_4}=n_{SO_2}=0,3\left(mol\right)\)
=> \(m_{H_2SO_4}=0,3.98=29,4\left(g\right)\)
b. Gọi x, y lần lượt là số mol của Na2SO3 và K2SO3
Theo PT(1,2):
=> x + y = 0,3
Theo đề, ta có: 126x + 158y = 44,2
=> x = 0,1, y = 0,2
Theo PT(1): \(n_{Na_2SO_4}=n_{Na_2SO_3}=0,1\left(mol\right)\)
=> \(m_{Na_2SO_4}=0,1.142=14,2\left(g\right)\)
Theo PT(2): \(n_{K_2SO_4}=n_{K_2SO_3}=0,2\left(mol\right)\)
=> \(m_{K_2SO_4}=0,2.164=34,8\left(g\right)\)
=> \(m_{sau.phản.ứng}=34,8+14,2=49\left(g\right)\)
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{0,3.98}{m_{dd_{H_2SO_4}}}.100\%=20\%\)
=> \(m_{dd_{H_2SO_4}}=147\left(g\right)\)
Ta có: \(m_{dd_{sau.phản.ứng}}=147+44,2=191,2\left(g\right)\)
=> \(C_{\%_{dd_{sau.phản.úng}}}=\dfrac{49}{191,2}.100\%=25,63\%\)
c. Đổi 500ml = 0,5 lít
=> \(n_{Ba\left(OH\right)_2}=1.0,5=0,5\left(mol\right)\)
Ta có: \(T=\dfrac{n_{SO_2}}{n_{Ba\left(OH\right)_2}}=\dfrac{0,3}{0,5}=0,6< 1\)
Vậy PTHH là: \(SO_2+Ba\left(OH\right)_2--->BaSO_3+H_2O\) (Ba(OH)2 dư.)
Theo PT: \(n_{BaSO_3}=n_{SO_2}=0,3\left(mol\right)\)
=> \(m_{BaSO_3}=0,3.217=65,1\left(g\right)\)
\(n_{SO_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Na_2SO_3+H_2SO_4\rightarrow Na_2SO_4+H_2O+SO_2\)
\(x\) \(x\)
\(K_2SO_3+H_2SO_4\rightarrow K_2SO_3+H_2O+SO_2\)
\(y\) \(y\)
Ta có: \(\left\{{}\begin{matrix}126x+158y=44,2\\x+y=0,3\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
a)\(\Rightarrow\Sigma n_{H_2SO_4}=0,1+0,2=0,3mol\)
\(\Rightarrow m_{H_2SO_4}=0,3\cdot98=29,4\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{29,4}{20}\cdot100=147\left(g\right)\)
b)








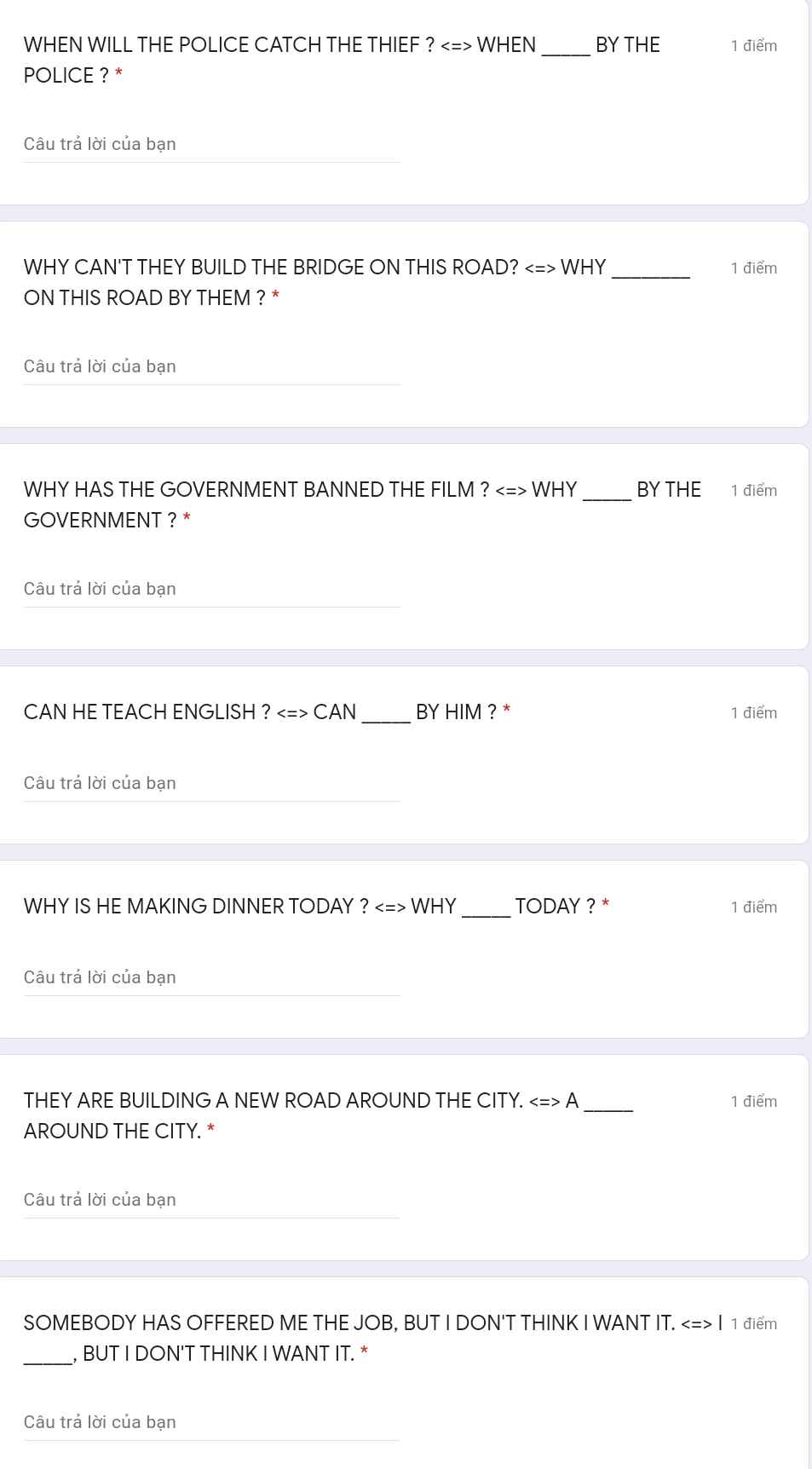 giúp em với ạa, bài này là bài tập không phải thi đâu ạa
giúp em với ạa, bài này là bài tập không phải thi đâu ạa


 giúp với ạa
giúp với ạa
\(4P+5O_2 \to 2P_2O_5\\ n_P=\frac{3,1}{31}=0,1(mol)\\ n_{O_2}=\frac{5}{32}=0,15625(mol)\\ \text{P hết}, O_2 \text{ dư}\\ a/ \\ m_{O_2}=(0,15625-0,125).32=1(g)\\ b/\\ \text{Chất tạo thành: } P_2O_5\\ n_{P_2O_5}=0,05(mol)\\ m_{P_2O_5}=0,05.142=7,1(g)\)