Cho 2,8 gam CaO tác dụng với một lượng nước lấy dư thu được dung dịch A. Sục 1,68 lít CO2 (đktc) vào dung dịch A.
a)Tính khối lượng kết tủa thu được.
b)Khi đun nóng dung dịch A thì khối lượng kết tủa thu được tối đa là bao nhiêu?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CaO+H2O−−−>Ca(OH)2(1)
nCaO=0,05(mol)nCaO=0,05(mol)
Theo PTHH: nNaOH=0,05(mol)nNaOH=0,05(mol)
Dung dich A thu được là NaOHNaOH
Khi sục 1,68 lít CO2 vào dung dich A thì:
nCO2=0,075(mol)nCO2=0,075(mol)
Ta có:\(\dfrac{nCO_2}{nNaOH}=\dfrac{0,075}{0,05}=1,5\)
⇒Sản phẩm thu được gồm hai muối
CO2(0,05)+Ca(OH)2(0,05)−−−>CaCO3(0,05)+H2O(2)
CaCO3(0,025)+CO2(0,025)+H2O−−−>Ca(HCO3)2(0,025)(3)
So sánh, ta chon nNaOH để tính.
Kết tủa thu được là CaCO3 dư sau phản ứng
Theo PTHH (1) và (2) nCaCO3(dư)=0,05−0,025=0,025(mol)
⇒mCaCO3=2,5(g)⇒mCaCO3=2,5(g)
b)
Dung dich A sau phản ứng là Ca(HCO3)2
Khi nung nóng dung dich A thì:
Ca(HCO3)2(0,025)−to−>CaCO3(0,025)+CO2+H2OCa(HCO3)(4)
Theo PTHH (4): mCaCO3=2,5(g)mCaCO3=2,5(g)
⇒∑mCaCO3=2,5+2,5=5(g)

Khi đun nóng dung dịch A
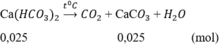
Khối lượng kết tủa tối đa thu được là m = (0,025 + 0,025).100 = 5g

Số mol CaO là nCaO = 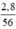 = 0,05 (mol)
= 0,05 (mol)
Số mol CO2 là nCO2 = 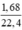 = 0,075 (mol)
= 0,075 (mol)
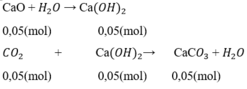
nCaCO3 = nCO2 pư = nCa(OH)2 = 0,05 mol
nCO2 dư = 0,075 – 0,05 = 0,025 (mol)
CaCO3 tạo thành 0,05 (mol) bị hòa tan 0,025 (mol)
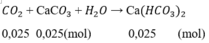
Số mol CaCO3 còn lại 0,05 – 0,025 = 0,025 (mol)
Khối lượng CaCO3 là m = 0,025. 100 = 2,5 (g)

Đáp án A
CaO+ H2O → Ca(OH)2
Ta có: nCa(OH)2= nCaO= 0,05 mol; nCO2= 1,68/22,4= 0,075 mol
Khi sục khí CO2 vào dung dịch A:
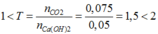
→ Tạo 2 muối
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
2CO2+ Ca(OH)2 → Ca(HCO3)2 (2)
Ca(HCO3)2→ CaCO3+ CO2+ H2O (3)
Đặt số mol CaCO3 PT 1 là x mol; số mol Ca(HCO3)2 PT 2 là y mol
Ta có: nCO2= x+2y= 0,075 mol; nCa(OH)2= x+y= 0,05 mol
→x=y= 0,025 mol→ m= mCaCO3= 0,025.100= 2,5 gam
Theo PT (2) và (3): nCaCO3= nCa(HCO3)2= 0,025 mol
→m'= mCaCO3= 0,025.100= 2,5 gam

\(n_{CaO}=\dfrac{2,8}{56}=0,2\left(mol\right)\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
0,2 0,2
a. \(n_{CO_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,075 0,075
vì \(\dfrac{0,075}{1}< \dfrac{0,2}{1}\) => dd \(Ca\left(OH\right)_2\) dư sau pứ.
=> \(m_{CaCO_3}=0,075.100=7,5\left(g\right)\)
b. \(n_{CaCO_3}=\dfrac{1}{100}=0,01\left(mol\right)\)
Thấy: \(n_{CaCO_3}< n_{Ca\left(OH\right)_2}\)
Nên ta có 2 trường hợp.
TH 1: \(dd.Ca\left(OH\right)_2.dư\)
Có:
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,1 0,1
m muối tạo thành là m kt = 1 (g)
\(V_{CO_2}=0,1.22,4=2,24\left(l\right)\)
TH 2: khí \(CO_2\) dư
Có:
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
0,2 0,2 0,2
\(CO_2+CaCO_3+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
0,1 0,1 0,1
\(m_{muối}=m_{CaCO_3}+m_{Ca\left(HCO_3\right)_2}=1+0,1.162=17,2\left(g\right)\)
\(V_{CO_2}=0,3.22,4=6,72\left(l\right)\)

a) nCaO = - 0,05 (mol); nCO2 = = 0,075 (mol)
CaO + H2O → Ca(OH)2
0,05 0,05 (mol)
A < nCO2 : nCa(OH)2 < 2 => tạo thành muối
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
0,05 0,05 0,05 (mol)
CaCO3 + CO2 + H2O → Ca(HCO3)2
0,025 (0,75 – 0,05) 0,025 (mol)
mCaCO3↓ = 100.(0,05-0,025) = 100.0,025 = 2,5 (gam)
b) Khi đun nóng dung dịch:
Ca(HCO3)2 CaCO3 + CO2 + H2O
0,025 0,025 (mol)
Khối lượng kết tủa tối đa thu được là: 0,05.100 = 5 (gam)

a) nCaO = - 0,05 (mol); nCO2 = = 0,075 (mol)
CaO + H2O → Ca(OH)2
0,05 0,05 (mol)
A < nCO2 : nCa(OH)2 < 2 => tạo thành muối
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
0,05 0,05 0,05 (mol)
CaCO3 + CO2 + H2O → Ca(HCO3)2
0,025 (0,75 – 0,05) 0,025 (mol)
mCaCO3↓ = 100.(0,05-0,025) = 100.0,025 = 2,5 (gam)
b) Khi đun nóng dung dịch:
Ca(HCO3)2 CaCO3 + CO2 + H2O
0,025 0,025 (mol)
Khối lượng kết tủa tối đa thu được là: 0,05.100 = 5 (gam).

a, nCaO=2.8/56=0.05(mol)
nCO2=1.68/22.4=0.075(mol)
dung dịch A chứa Ca(OH)2
CaO+H2O=>Ca(OH)2
0.05------------>0.05(mol)
=> nCa(OH)2=0.05(mol)
Ta có:
nCO2/nCa(OH)2=0.075/0.05=1.5
=>phản ứng sinh ra hai muối trung hòa và axit.
Gọi a,b là số mol của Ca(OH)2 ở (1)(2):
CO2+Ca(OH)2=>CaCO3+H2O(1)
a------->a------------->a(mol)
2CO2+Ca(OH)2=>Ca(HCO3)2(2)
2b-------->b------------>b(mol)
Ta có:
\(\begin{cases}a+2b=0.075\\a+b=0.05\end{cases} \)
<=> a=b=0.025
=>mCaCO3=0.025*100=2.5(g)
b, khi đun nóng dung dịch thì
Ca(HCO3)2 (t0)=> CaCO3 + CO2 + H2O
b------------------>b(mol)
=> nCaCO3= 0.025 mol
=> mCaCO3= 0.025*100= 2.5 g

\(CaO+H_2O--->Ca(OH)_2\)\((1)\)
\(nCaO=0,05(mol)\)
Theo PTHH: \(nNaOH=0,05(mol)\)
Dung dich A thu được là \(NaOH\)
Khi sục 1,68 lít CO2 vào dung dich A thì:
\(nCO_2=0,075(mol)\)
Ta có: \(\dfrac{nCO_2}{nNaOH}=\dfrac{0,075}{0,05}=1,5\)
\(\Rightarrow\)Sản phẩm thu được gồm hai muối
\(CO_2(0,05)+Ca(OH)_2(0,05)--->CaCO_3(0,05)+H_2O\)\((2)\)
\(CaCO_3(0,025)+CO_2(0,025)+H_2O--->Ca(HCO_3)_2(0,025)\)\((3)\)
So sánh, ta chon nNaOH để tính.
Kết tủa thu được là CaCO3 dư sau phản ứng
Theo PTHH (1) và (2) \(nCaCO_3(dư)=0,05-0,025=0,025(mol)\)
\(\Rightarrow mCaCO_3=2,5\left(g\right)\)
\(b)\)
Dung dich A sau phản ứng là \(Ca(HCO_3)_2\)
Khi nung nóng dung dich A thì:
\(Ca(HCO_3)_2(0,025)-t^o->CaCO_3(0,025)+CO_2+H_2O\)\((4)\)
Theo PTHH (4): \(mCaCO_3=2,5(g)\)
\(\Rightarrow\sum mCaCO_3=2,5+2,5=5\left(g\right)\)