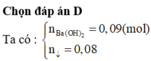Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt công thức chung của 2 muối trong A là MCO3
PTHH: MCO3 + H2SO4 ==> MSO4 + CO2 + H2O (1)
CO2 + Ba(OH)2 ==> BaCO3 + H2O (2)
2CO2 + Ba(OH)2 ==> Ba(HCO3)2 (3)
Ta có: +) nBaCO3 = \(\frac{15,76}{197}=0,08\left(mol\right)\)
+) nBa(OH)2 = 0,45 x 0,2 = 0,09 (mol)
=> nCO2 (PT2) = nBa(OH)2 (PT2) = 0,08 (mol)
=> nBa(OH)2 (PT3) = 0,09 - 0,08 = 0,01 (mol)
=> nCO2 (PT3) = 0,02 (mol)
\(\Rightarrow\sum n_{CO2}=0,08+0,02=0,1\left(mol\right)\)
=> nMCO3 = 0,1 (mol)
=> MMCO3 = \(\frac{7,2}{0,1}=72\left(\frac{g}{mol}\right)\)
=> MM = 12 (g/mol)
Vì 2 kiềm loại này thuộc 2 chu kì liên tiếp nhau và là kim loại kiềm thổ
=> 2 kim loại đó là Mg và Be

Đặt công thức chung của hai muối cacbonat là MCO3MCO3
M cũng là KLNTTB của hai kim loại IIA kế tiếp.
Phản ứng: MCO3+H2SO4→MSO4+CO2+H2OMCO3+H2SO4→MSO4+CO2+H2O (1)(1)
Khí B là CO2(nCO2−nMCO3)CO2(nCO2−nMCO3) tác dụng dung dịch Ba(OH)2Ba(OH)2 tạo kết tủa.
Có thể có hai phản ứng: CO2+Ba(OH)2→BaCO3+H2OCO2+Ba(OH)2→BaCO3+H2O (2)(2)
Có thể: 2CO2+Ba(OH)2→Ba(HCO3)22CO2+Ba(OH)2→Ba(HCO3)2 (3)(3)
Có hai trường hợp :
Trường hợp (1)(1): Ba(OH)2Ba(OH)2 dư chỉ có phản ứng (2)(2) xảy ra
nCO2=nBa(OH)2=15,76197=0,08mol⇒MCO3=7,20,08=90⇒M=30nCO2=nBa(OH)2=15,76197=0,08mol⇒MCO3=7,20,08=90⇒M=30
⇒⇒ hai kim loại kế tiếp nhau là Mg=24<30<Ca=40Mg=24<30<Ca=40
Công thức hai muối: MgCO3(x)mol,CaCO3(y)molMgCO3(x)mol,CaCO3(y)mol
Có hệ phương trình: Tổng mol hỗn hợp: x+y=0,08x+y=0,08 ; Tổng khối lượng hỗn hợp: 84x+100y=7,284x+100y=7,2
⇒MgCO3=84.0,057,2.100%=58,33%;%CaCO3=41,67%⇒MgCO3=84.0,057,2.100%=58,33%;%CaCO3=41,67%
Trường hợp (2)(2) : Ba(OH)2Ba(OH)2 phản ứng hết 0,45.0,2=0,09mol0,45.0,2=0,09mol (2)(2) phản ứng (2)(2) (3)(3) xảy ra:
nCO2nCO2(2)=0,08;nCO2=0,08;nCO2(3)=2nBa(OH)2=2.0,01=0,02=2nBa(OH)2=2.0,01=0,02
⇒nMCO3=nCO2=0,08+0,02=0,1⇒M=12⇒nMCO3=nCO2=0,08+0,02=0,1⇒M=12
Hai muối BeCO3;MgCO3BeCO3;MgCO3
%BeCO3=76,67%;%MgCO3=23,33%%BeCO3=76,67%;%MgCO3=23,33%

gọi công thức 2 muối cacbonat là : MCO3
MCO3 + H2SO4 -> MSO4 + H2O + CO2(1)
CO2 + Ba(OH)2 -> BaCO3 + 2H2O (2)
CO2 + BaCO3 + H2O -> Ba(HCO3)2(3)
nBaCO3=15,76/197=0,08 mol
nBa(OH)_2=O,2*0,45=0,09 mol
từ 1,2,3 => nCO_2=0,09+(0,09-0,08)=0,1 mol
=> MCO_3=7,2/0,1=72=>M=12
=>2 muối cacbonat là: MgCO3 và BeCO3
gọi công thức 2 muối cacbonat là : MCO3
MCO3 + H2SO4 -> MSO4 + H2O + CO2(1)
CO2 + Ba(OH)2 -> BaCO3 + 2H2O (2)
CO2 + BaCO3 + H2O -> Ba(HCO3)2(3)
nBaCO3=15,76/197=0,08 mol
nBa(OH)_2=O,2*0,45=0,09 mol
từ 1,2,3 => nCO_2=0,09+(0,09-0,08)=0,1 mol
=> MCO_3=7,2/0,1=72=>M=12
=>2 muối cacbonat là: MgCO3 và BeCO3

Đáp án B
7,2 gam MCO3 + HCl → CO2 + 0,09 mol Ba(OH)2 → 0,08 mol BaCO3↓
• CO2 + Ba(OH)2 → BaCO3↓ + H2O(*)
BaCO3 + CO2 + H2O → Ba(HCO3)2 (**)
Theo (*) nCO2(*) = 0,09 mol; nBaCO3 (*) = 0,09 mol
Theo (**) nBaCO3 (**) dư = 0,08 mol → nBaCO3 (**) phản ứng = 0,09 - 0,08 = 0,01 mol
→ nCO2 (**) = 0,01 mol → ∑nCO2 = 0,1 mol
• MCO3 + 2HCl → MCl2 + CO2 + H2O
nMCO3 = nCO2 = 0,1 mol → MMCO3 = 7,2 : 0,1 = 72 → MM = 12 → Be và Mg (9 < 20 < 24)

Gọi CT dạng chung của 2 muối cacbonat là \(M_2CO3\)
\(M2CO3+2HCl\rightarrow2MCl+H2O+CO2\)
Ta có: \(n_{Ba\left(OH\right)2}=0,7.0,5=0,35\left(mol\right)\)
\(n_{BaCO3}=\dfrac{29,55}{ }=0,15\left(mol\right)\)
=>TH1: Ba(OH)2 dư=> tạo 1 muối trung hoà
\(CO2+Ba\left(OH\right)2\rightarrow BaCO3+H2O\)
\(n_{CO2}=n_{BaCO3}=0,15\left(mol\right)\)
\(n_{M2CO3}=n_{CO2}=0,15\left(mol\right)\)
\(M_{M2CO3}=\dfrac{19,1}{0,15}=127,3\)
\(\Rightarrow M_M=\dfrac{127,3-12-16.3}{2}=33,65\)
=> 2 muối cacbonat là \(Na2CO3\) và K2CO3
Gọi \(n_{Na2CO3}=a\left(mol\right),n_{K2CO3}=b\left(mol\right)\)
khi đó:
\(\left\{{}\begin{matrix}106a+138b=19,1\\a+b=0,15\left(theo-CO2\right)\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}a=0,05\\b=0,1\end{matrix}\right.\)
\(\%m_{Na2CO3}=\dfrac{0,05.106}{19,1}.100\%=27,75\%\)
\(\%m_{K2CO3}=100-27,75=72.25\%\)
TH2: CO2 dư=>tạo 2 muối
\(CO2+Ba\left(OH\right)2\rightarrow BaCO3+H2O\)
0,15<---0,15<-----------0,15(mol)
\(\Rightarrow n_{Ba\left(OH\right)2}\)còn lại\(=0,25-0,15=0,2\left(mol\right)\)
\(2CO2+Ba\left(OH\right)2\rightarrow Ba\left(HCO3\right)2\)
0,4<-------0,2(mol)
\(\Rightarrow n_{M2CO3}=n_{CO2}=0,4\left(mol\right)\)
\(M_{M2CO3}=\dfrac{19,1}{0,4}=47,45\)
\(\Rightarrow M_M=\dfrac{47,45-12-16.3}{2}=-6,125\)
=> LOẠI
Chúc bạn học tốt^^
Cảm ơn câu trả lời và lời động viên của bạn nha!!!!![]()