đốt cháy hỗn hợp X gồm 2,4 gam Mg , 4,48 gam Fe bằng V lít hỗn hợp khí Y gồm O2 và Cl2 thu được hỗn hợp rắn Z gồm các muối clorua và oxit( ko còn khí dư). hòa tan Z bằng 160 ml dung dịch HCl 1M vừa đủ được dung dịch T. cho dung dihcj T tác dụng với dd AGNO3 dư thu được 62,785 gam kết tủa. giá trị V là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án : D
nMg = 0,08 mol ; nFe = 0,08 mol
Khi phản ứng với X thì có x mol Cl2 và y mol O2 phản ứng
Giả sử tạo a mol Fe2+ và (0,08 – a) mol Fe3+
Bảo toàn điện tích : 2.0,08 + 2a + 3(0,08 – a) = 2x + 4y
Hòa tan Y bằng HCl : 2Cl thay thế 1 O => nO = ½ nHCl = 0,12 mol = 2y
=> 0,4 – a = 2x + 4.0,06 (1)
,Sau đó : phản ứng với AgNO3 tạo : (2x + 0,24) mol AgCl và a mol Ag
=> 56,69 = 143,5(2x + 0,24) + 108a (2)
Từ (1),(2) => x = 0,07 ; a = 0,02 mol
=> %VCl2(X) = 53,85%

Chọn C
nMg = 0,08 mol ; nFe = 0,08 mol
Khi phản ứng với X thì có x mol Cl2 và y mol O2 phản ứng
Giả sử tạo a mol Fe2+ và (0,08 – a) mol Fe3+
Bảo toàn điện tích : 2.0,08 + 2a + 3(0,08 – a) = 2x + 4y
Hòa tan Y bằng HCl : 2Cl thay thế 1 O => nO = ½ nHCl = 0,12 mol = 2y
=> 0,4 – a = 2x + 4.0,06 (1)
,Sau đó : phản ứng với AgNO3 tạo : (2x + 0,24) mol AgCl và a mol Ag
=> 56,69 = 143,5(2x + 0,24) + 108a (2)
Từ (1),(2) => x = 0,07 ; a = 0,02 mol
=> %VCl2(X) = 53,85%

\(n_{HCl}=0,12.2=0,24\left(mol\right)\)
=> \(n_{H_2O}=0,12\left(mol\right)\)
=> \(n_{O\left(oxit\right)}=0,12\left(mol\right)\)
=> \(n_{O_2}=0,06\left(mol\right)\)
\(n_{Mg}=\dfrac{1,68}{24}=0,07\left(mol\right)\); \(n_{Al}=\dfrac{2,16}{27}=0,08\left(mol\right)\)
Gọi số mol Cl2 là x (mol)
Mg0 - 2e --> Mg+2
0,07->0,14
Al0 - 3e --> Al+3
0,08->0,24
O20 + 4e --> 2O-2
0,06->0,24
Cl20 + 2e --> 2Cl-
x--->2x
Bảo toàn e: 2x + 0,24 = 0,24 + 0,14
=> x = 0,07 (mol)
=> \(\%V_{Cl_2}=\dfrac{0,07}{0,06+0,07}.100\%=53,846\%\)

Đáp án : B
nMg = 0,08 mol ; nFe = 0,08 mol
Khi phản ứng với X thì có x mol Cl2 và y mol O2 phản ứng
Giả sử tạo a mol Fe2+ và (0,08 – a) mol Fe3+
Bảo toàn điện tích :
2.0,08 + 2a + 3(0,08 – a) = 2x + 4y
Hòa tan Y bằng HCl : 2Cl thay thế 1 O
=> nO = 1 2 nHCl = 0,12 mol = 2y
=> 0,4 – a = 2x + 4.0,06 (1)
Sau đó phản ứng với AgNO3 tạo :
(2x + 0,24) mol AgCl và a mol Ag
=> 56,69 = 143,5(2x + 0,24) + 108a (2)
Từ (1),(2) => x = 0,07 ; a = 0,02 mol
=> % V C l 2 X = 53,85%

Đáp án C
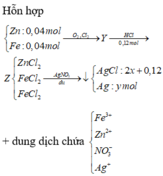
Khi tác dụng với HCl chỉ có các oxit bị hòa tan
→ nHCl = 4nO2 → nO2 = 0,03 mol
Gọi số mol của Cl2 và Ag lần lượt là x, y mol
Bảo toàn nguyên tố Cl → nAgCl = 2nCL2 + nHCl = 2. x + 0,12
→ 143,5( 2. x + 0,12) + 108y = 28,345
Bảo toàn electron cho toàn bộ quá trình 3nFe + 2nZn = 2nCl2 + 4nO2 + nAg
→ 3. 0,04 + 2.0,04 = 2.x + 4. 0,03 + y
Giải hệ → x= 0,035 và y = 0,01
![]()

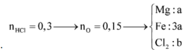
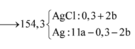
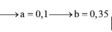
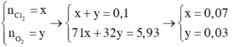
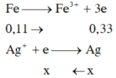
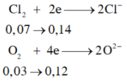
Coi rằng hh Y gồm O và x mol Cl cho đơn giản.
+) Z + HCl sinh ra muối và H2O, tất cả Oxi đã chui vào nước nên:
\(n_O=n_{H2O}=\frac{1}{2}n_{HCl}=\frac{0,16}{2}=0,08\left(mol\right)\)
+) Xét sự thay đổi số oxi hóa toàn bộ quá trình phản ứng:
\(Mg^0\rightarrow Mg^{2+};Fe^0\rightarrow Fe^{3+}\)
\(O\rightarrow O^{2-};Cl\rightarrow Cl^-;Ag^+\rightarrow Ag\downarrow\)
Bảo toàn e, ta có:
\(2n_{Mg}+3n_{Fe}=2n_O+n_{Cl}+n_{Ag}\)
\(\Rightarrow n_{Ag}=0,1\cdot2+0,08\cdot3-0,08\cdot2-x=0,28-x\left(mol\right)\)
+) Bảo toàn nguyên tố Cl, ta có:
\(n_{AgCl\downarrow}=n_{Cl}+n_{HCl}=x+0,16\left(mol\right)\)
+) 62,785 gam kết tủa gồm Ag và AgCl,
\(62,785=143,5\left(x+0,16\right)+108\left(0,28-x\right)\\ \Rightarrow x=0,27\)
Vậy hh Y chứa 0,08 mol O và 0,27 mol Cl
Hay Y chứa 0,04 mol O2 và 0,135 mol Cl2
V=(0,04+0,135)*22,4=3,92(l)
Bài này tương tự dạng NaOH tác dụng CO2, nhưng có thể sinh ra 3 loại muối, phải chia đến 4 trường hợp...Dài dã man nên mình không viết ra đâu :p
......
Trường hợp thỏa mãn là KOH dư, hỗn hợp cô cạn gồm 0,1 mol KOH, 0,2 mol K3PO4
m=14,2 g