Hỗn hợp X gồm 8,1 gam Al và 10,8 gam FeO. Hòa tan hết X trong dung dịch axit sunfuric loãng dư, sau khi kết thúc phản ứng thu được V lít khí (đktc). Giá trị của V là:
A. 10,08.
B. 6,72.
C. 11,2.
D. 22,4.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Đặt nN2O = nH2 = a (mol)
nNH4+ = b (mol)
=> nH+ = 10nN2O + 2nH2 + 10 nNH4+ = 12a + 10b
=> nNa+ = 12a + 10b + 0,06 ; nSO42- = 12a + 10b
nMg = nMg(OH)2 = 0,24 (mol)
Bảo toàn electron: 2nMg + 3nAl = 8nN2O + 2nH2 + 8nNH4+
=> nAl = (10a + 8b – 0,48)/3
BTNT N => 3nAl(NO3)3 + nNaNO3 = 2n N2O + nNH4+
=> nAl(NO3)3 = (2a + b – 0,06)/3
BTNT Al => nAl3+ trong X = nAl + nAl(NO3) = 4a + 3b – 0,18
Khối lượng muối trong X( Na+ ; Al3+; Mg2+; NH4+ ; SO42- ):
23( 12a + 10b + 0,06) + 27 ( 4a + 3b – 0,18) + 0,24.24 + 18b + 96 ( 12a + 10b) = 115, 28 (1)
nNaOH = 4nAl3+ + 2nMg2+ + nNH4+
=> 0,92 = 4 ( 4a + 3b – 0,18 ) + 2.024 + b (2)
Từ (1) và (2) => a = b = 0,04 (mol)
=> nT = 2a = 0,08 (mol)
=> V= 1,792 (lít)

Gọi x,y lần lượt là số mol của Al, Fe
nH2 = \(\dfrac{8,96}{22,4}\)=0,4 mol
Pt: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
......x.................................0,5x...........1,5x
.....Fe + H2SO4 --> FeSO4 + H2
.......y..........................y............y
Ta có hệ pt:
{27x+56y=11
1,5x+y=0,4
⇔x=0,2, y=0,1
% mAl = \(\dfrac{0,2.27}{11}\).100%=49,1%
% mFe = \(\dfrac{0,1.56}{11}\).100%=50,9%
mAl2(SO4)3 = 0,5x . 342 = 0,5 . 0,2 . 342 = 34,2 (g)
mFeSO4 = 152y = 152 . 0,1 = 15,2 (g)
Gọi CTTQ: MxOy
Pt: MxOy + yH2 --to--> xM + yH2O
\(\dfrac{0,4}{y}\)<-------0,4
Ta có: 232,2=\(\dfrac{0,4}{y}\)(56x+16y)
⇔23,2=\(\dfrac{22,4x}{y}\)+6,4
⇔\(\dfrac{22,4x}{y}\)=16,8
⇔22,4x=16,8y
⇔x:y=3:4
Vậy CTHH của oxit: Fe3O4

câu 7
MgO + 2HCl -> MgCl2 + H2O
x 2x
Fe2O3 + 6HCl -> 2FeCl3 + 3H2O
y 6y
CuO + 2HCl -> CuCl2 + H2O
z 2z
A--H2 dư----> MgO + H2O
Fe
Cu
Fe2O3 + 3H2 -> 2Fe + 3H2O
ky
CuO + H2 -> Cu + H2O
kz
nH2O=\(\dfrac{16,2}{18}\)0,09mol
Gọi nMgO=x, nFe2O3=y, nCuO=z (trong 4,8g hh A)
nMgO=kx, nFe2O3=ky, nCuO=kz (trong 0,09mol A)
=> kx+ky+kz =4,8
3ky + kz= 0,09=> 2ky = kx =>\(\left\{{}\begin{matrix}2y=x\\40x+160y+80z=4,8\\2x+6y+2z=\dfrac{5,84}{36,5}=0,16\end{matrix}\right.\)
+ x=0,02
=> mMgO= 0,8g
+y=0,01
=> mFe2O3=1,6g
+ z=0,03
=> mCuO=2,4g
Gọi x,y lần lượt là số mol của Al, Fe
nH2 = 8,9622,4=0,48,9622,4=0,4 mol
Pt: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
......x.................................0,5x...........1,5x
.....Fe + H2SO4 --> FeSO4 + H2
.......y..........................y............y
Ta có hệ pt: {27x+56y=111,5x+y=0,4⇔{x=0,2y=0,1{27x+56y=111,5x+y=0,4⇔{x=0,2y=0,1
% mAl = 0,2×2711.100%=49,1%0,2×2711.100%=49,1%
% mFe = 0,1×5611.100%=50,9%0,1×5611.100%=50,9%
mAl2(SO4)3 = 0,5x . 342 = 0,5 . 0,2 . 342 = 34,2 (g)
mFeSO4 = 152y = 152 . 0,1 = 15,2 (g)
Gọi CTTQ: MxOy
Pt: MxOy + yH2 --to--> xM + yH2O
0,4y0,4y<-------0,4
Ta có: 232,2=0,4y(56x+16y)232,2=0,4y(56x+16y)
⇔23,2=22,4xy+6,4⇔23,2=22,4xy+6,4
⇔22,4xy=16,8⇔22,4xy=16,8
⇔22,4x=16,8y⇔22,4x=16,8y
⇔xy=16,822,4=34⇔xy=16,822,4=34
Vậy CTHH của oxit: Fe3O4

Đáp án A
Quy hỗn hợp X về dạng Fe và O.
=> mX = 56nFe + 16nO = 14,4g (1)
- Khi X + H2SO4: Bảo toàn e: 3nFe = 2nO + 2nSO2
=> 3nFe – 2nO = 2.6,72: 22,4 = 0,6 mol (2)
Từ (1,2) => nFe = 0,24; nO = 0,06 mol
Vậy muối trong dung dịch sau phản ứng sẽ là: 0,12 mol Fe2(SO4)3
=> mFe2(SO4)3 = 0,12.400 = 48g

Chọn D.
Hỗn hợp Mg, Al và Al(NO)3 tác dụng với dung dịch chứa NaHSO4 (x mol) và 0,06 mol NaNO3.
Dung dịch X gồm
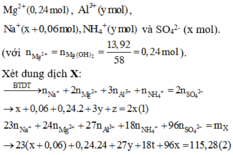
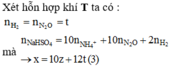
Xét dung dịch thu được sau khi cho X tác dụng với dung dịch chứa 0,92 mol NaOH, ta có:
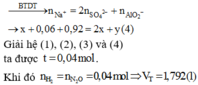

Đáp án C
Gọi số mol N2O và H2 là a mol, NH4+ có thể tạo ra là b mol.
Bảo toàn H+:

$n_{Al} = \dfrac{8,1}{27} = 0,3(mol)$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$FeO + H_2SO_4 \to FeSO_4 + H_2O$
$n_{H_2} = \dfrac{3}{2}n_{Al} = 0,45(mol)$
$V = 0,45.22,4 = 10,08(lít)$
\(n_{Al}=\frac{8,1}{27}=0,3mol\\ 2Al+3H_2SO_4\rightarrow Al_2(SO_4)_3 +3H_2 n_{H_2}=0,45mol\\ V=10,08l\)