nhúng 1 thanh sắt vào cốc đựng dung dịch Cuso4 cho đến khi màu xanh sau phản ứng thấy khối lượng kim loại tăng so với thanh sắt ban đầu là 0,8g . tính khối lượng đồng đã bám vào đinh sắt
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Fe + CuSO4 = FeSO4 + Cu
Sau phản ứng khối lượng thanh sắt tăng lên, chứng tỏ có 1 lượng Cu bám lên thanh sắt.
Khối lượng Cu phản ứng là: 16,4 - 15,6 = 0,8 (g)
Số mol Cu là: 0,8 : 64 = 0,0125 (mol)
Theo PTHH: n Fe= nCu = 0,0125 (mol)
Khối lượng sắt tham gia phản ứng là: 0,0125 x 56 = 0,7(g)

Đáp án B
Fe + Cu2+ → Fe2+ + Cu
PT 1 mol 1 mol 1mol
ĐB 0,2 mol
mthanh sắt tăng = 64 – 56 = 8 gam
← 1,6 gam

Đáp án B
Fe + Cu2+ → Fe2+ + Cu
PT 1mol 1mol 1mol mthanh sắt tăng = 64- 56 = 8 gam
ĐB 0,2 mol ← 1,6 gam
=> V = 0,2/1 = 0,2 lít = 200 ml

Đáp án B
Fe + Cu2+ → Fe2+ + Cu
PT 1 mol 1 mol 1mol
mthanh sắt tăng = 64 – 56 = 8 gam
ĐB 0,2 mol ← 1,6 gam

Đáp án B
Fe + Cu2+ → Fe2+ + Cu
PT 1 mol 1 mol 1mol mthanh sắt tăng = 64 – 56 = 8 gam
ĐB 0,2 mol ← 1,6 gam

Fe +CuSO4 → FeSO4 + Cu
Khối lượng thanh sắt tăng thêm đúng bằng khối lượng Cu thêm vào trừ đi khối lượng Fe tham gia phản ứng.
Gọi số mol của Fe tham gia phản ứng là x (mol)
Ta có : 64x−56x=51−50=1
=> x=0,125 (mol)
=> n CuSO4 pứ = n Fe(pứ) = 0,125 (mol)
\(CM_{CuSO_4}=\dfrac{0,125}{0,1}=1,25M\)
n FeSO4 = n Fe(pứ) = 0,125 (mol)
\(CM_{FeSO_4}=\dfrac{0,125}{0,1}=1,25M\)
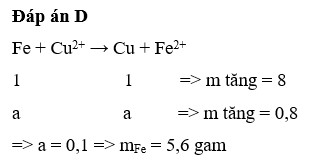
Đặt số mol Fe phản ứng là x (mol)
PTHH:
Fe + CuSO4 ===> FeSO4 + Cu
x................................................x
Theo đề ra, ta có:
mkim loại tăng = mCu(bám vào) - mFe(phản ứng) = 0,8
<=> 64x - 56x = 0,8
=> x = 0,1
=> mCu(bám vào) = 0,1 x 64 = 6,4 gam
1