Cho m gam (sắt ôxit) FeO tác dụng hết với 600ml dd HCl (axit clohidric) đặc tạo thành dd (sắt clorua) FeCl2 0,2M. Tính m?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Theo PTHH và đề bài, ta có:
nFeCl2=nFe= 0,5 (mol)
Khối lượng sắt clorua tạo thành:
mFeCl2=nFeCl2.MFeCl2=0,5.127=63,5(g)
c) nFe=
mFe/ MFe = 14/56 = 0,25 mol
Theo PTHH và đề bài, ta được:
nHCl= 2.nFe= 2.0,25=0,5 (mol)
Khối lượng HCl đã phản ứng:
mHCl=nHCl . MHCl= 0,5 . 36,5 = 18,25 (g)

a)
Zn + H2SO4 → ZnSO4 + H2
Fe + H2SO4 → FeSO4 + H2
b) Gọi số mol Zn và Fe có trong 17,7 gam hỗn hợp là x và y mol. nH2 = \(\dfrac{6,72}{22,4}\)=0,3 mol
Theo tỉ lệ phản ứng ta có\(\left\{{}\begin{matrix}x+y=0,3\\65x+56y=17,7\end{matrix}\right.\)=> x = 0,1 và y = 0,2
=>%n Zn=\(\dfrac{0,1}{0,3}100=33,33\%\)
=>%n Fe=66,67%
=>m muối= 0,1.161+0,2.152=46,5g
Gọi số mol Fe, Zn là a, b (mol)
=> 56a + 65b = 17,7 (1)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
a----------------->a--->a
Zn + H2SO4 --> ZnSO4 + H2
b------------------->b----->b
=> a + b = 0,3 (2)
(1)(2) => a = 0,2 (mol); b = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%n_{Fe}=\dfrac{0,2}{0,3}.100\%=66,67\%\\\%n_{Zn}=\dfrac{0,1}{0,3}.100\%=33,33\%\end{matrix}\right.\)
mmuối = 0,2.152 + 0,1.161 = 46,5 (g)

PTHH: \(MgO+2HCl\rightarrow MgCl_2+H_2O\)
Ta có: \(n_{MgO}=\dfrac{10}{40}=0,25\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{HCl}=0,5\left(mol\right)\\n_{MgCl_2}=0,25\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C_{M_{HCl}}=\dfrac{0,5}{0,5}=1\left(M\right)\\C_{M_{MgCl_2}}=\dfrac{0,25}{0,5}=0,5\left(M\right)\end{matrix}\right.\)
Ta có: nMgO = \(\dfrac{10}{40}=0,25\left(mol\right)\)
a. PTHH: MgO + 2HCl ---> MgCl2 + H2O
Theo PT: nHCl = 2.nMgO = 2.0,25 = 0,5(mol)
Đổi 500ml = 0,5 lít
=> \(C_{M_{HCl}}=\dfrac{0,25}{0,5}=0,5M\)
b. Ta có: \(V_{dd_{MgCl_2}}=10+0,5=10,5\left(lít\right)\)
Theo PT: \(n_{MgCl_2}=n_{MgO}=0,25\left(mol\right)\)
=> \(C_{M_{MgCl_2}}=\dfrac{0,25}{10,5}=0,024M\)

Gọi x là hóa trị của sắt
\(m_{FeCl_x}=\dfrac{10\cdot32,5\%}{100\%}=3,25\left(g\right)\\ n_{AgCl}=\dfrac{8,61}{143,5}=0,06\left(mol\right)\\ PTHH:FeCl_x+AgNO_3\rightarrow Fe\left(NO_3\right)_x+xAgCl\)
Theo PTHH: \(n_{FeCl_x}=\dfrac{n_{AgCl}}{x}=\dfrac{0,06}{x}\left(mol\right)\)
\(\Rightarrow M_{FeCl_x}=\dfrac{3,25}{\dfrac{0,06}{x}}=54x\\ \Rightarrow56+35,5x=54x\\ \Rightarrow x=3\)
Vậy CTHH cần tìm là \(FeCl_3\)

nH2 = 2.24/22.4 = 0.1 (mol)
Fe + 2HCl => FeCl2 + H2
0.1...............................0.1
mFe = 0.1 * 56 = 5.6 (g)

Phương trình: 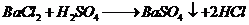
Vậy kết tủa là 

Số mol
Phương trình
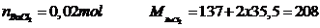

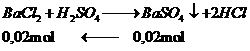
 khối lượng
khối lượng
Vậy m là 

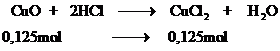
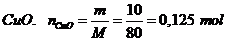

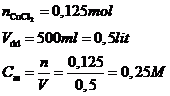

Nồng độ FeCl2: CM=0,2M thể tích dd: Vdd = 600ml = 0,6lit
Pt:
Vậy m là