X là một kim loại hóa trị hai .hòa tan hoàn toàn 6,082g X vào đ HCL dư thì thu được 5,6l khí dktc?
tìm khối lưongj nguyên tử và tên nguyên tố X.b) X có 3 đồng vị bik tổng số khối của 3 đồng vị là 75.số khối của đồng vị thứ hai bằng trung bình cộng số khối của hai đơn vị kia,đơn vị thứ nhất có số proton = notron,đơn vị thứ ba chiếm 11,4% số nguyên tử và có số nôtrn nhìu hơn đồng vị thứ hai la` 1 đơn vị.tTÌM số khối và số n of mỗi loại đồng vị.tìm % về số nguyên tử của hai đông vị còn lại.khi có 50 nguyên tử của đồng vị thứ hai thì có bao nhiu nguyên tử của các đồng vị còn lạiHãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi nFe=a(mol);nM=b(mol)⇒56a+Mb=9,6(1)
Fe+2HCl→FeCl2+H2
M+2HCl→MCl2+H2
nH2=a+b=0,2⇒a=0,2−b
Ta có :
56a+Mb=9,656a+Mb=9,6
⇔56(0,2−b)+Mb=9,6
⇔Mb−56b=−1,6
⇔b(56−M)=1,6
⇔b=1,656−M
Mà 0<b<0,20<b<0,2
Suy ra : 0<1,656−M<0,20<1,656−M<0,2
⇔M<48(1)
M+2HCl→MCl2+H2
nM=nH2<5,622,4=0,25
⇒MM>4,60,25=18,4
+) Nếu M=24(Mg)
Ta có :
56a+24b=9,656a+24b=9,6
a+b=0,2a+b=0,2
Suy ra a = 0,15 ; b = 0,05
mFe=0,15.56=8,4(gam)
mMg=0,05.24=1,2(gam)
+) Nếu M=40(Ca)
56a+40b=9,656a+40b=9,6
a+b=0,2
Suy ra a = b = 0,1
mCa=0,1.40=4(gam)
mFe=0,1.56=5,6(gam)

Gọi % đồng vị
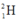
là a:
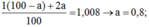

m của 1ml H2O: 1 gam
⇒ MH2O = 2. 1,008 + 16 = 18,016u
Khối lượng của 1 mol H2O là 18,016g.
Khối lượng của 1 mol H2O là 18,016g.
Số mol H2O =

mol
⇒ số mol nguyên tử H = 2.nH2O =
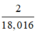
mol
1 mol nguyên tử chứa 6,022.1023 nguyên tử
⇒ Số nguyên tử H trong 1ml H2O =
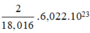
⇒ Số nguyên tử

Đáp án C
Gọi số khối của X lần lượt là A1, A2, A3
Ta có hệ
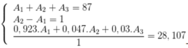
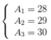

do là đồng vị nên các nguyên tử có cùng số proton =>
p + n1 + p + n2 + p + n3 = 75 <=> 3p + n1 + n2 + n3 =75 (1)
mà nguyên tử đồng vị 1 có p = n => (1) <=> 4p + n2 + n3 = 75 (2)
ta lại có n3 - n2 = 1 => (2) <=> 4p + 2 n2 = 74 <=> 2p + n2 = 37 dùng bất pt bạn được p =< 12,33 và p >= 10.5 vậy chỉ thỏa khi p = 12 => n2 = 13 Vậy số khối 3 đồng vị lần lượt là 24 25 26
A trung bình của X là = 24 . 115 + 25. 3 + 26. 2 / ( 115 + 3 +2 ) = 24,0583

Đáp án C
Do là đồng vị nên các nguyên tử có cùng số proton nên:
p + n1 + p + n2 + p + n3 = 75 ⇔ 3p + n1 + n2 + n3 =75 (1)
mà nguyên tử đồng vị 1 có p = n
⇒ (1) ⇔ 4p + n2 + n3 = 75 (2)
ta lại có n3 - n2 = 1
⇒ (2) ⇔ 4p + 2 n2 = 74 ⇔ 2p + n2 = 37
p ≤ 12,33 và p ≥ 10.5
p = 12 ⇒ n2 = 13 Vậy số khối 3 đồng vị lần lượt là 24, 25, 26


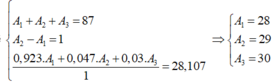
a.
X + 2HCl = XCl2 + H2
nX = nH2 = 5,6/22,4 = 0,25 mol
=> X = 6,082/0,25 = 24,328 (Mg)
b.
Mg có Z = 12
Gọi A1, A2, A3 lần lượt là số khối của 3 đồng vị
Tổng số khối của 3 đồng vị là 75
=> A1 + A2 + A3 = 75 (1)
Số khối của đồng vị thứ hai bằng trung bình cộng số khối của hai đồng vị kia
A2 = (A1 + A3)/2 => A1 - 2A2 + A3 = 0 (2)
Lấy (1) trừ (2) => 3A2 = 75 => A2 = 25 => N2 = A2 - Z = 25 - 12 = 13
Đồng vị thứ 3 có số neutron nhiều hơn đồng vị thứ 2 là 1 đơn vị
N3 - N2 = 1 => N3 = 1 + 13 = 14
=> A3 = 12 + 14 = 26
=> A1 = 75 - 26 - 25 = 24
Đồng vị 26Mg trong tự nhiên chiếm 11,4% số nguyên tử
=> %(24Mg, 25Mg) = 100% - 11,4% = 88,6%
Ta có : (88,6 - x)A1 + xA2 + 11,4A3 = 24,328.100
=> x = 10(%)
Vậy thành phần % của 3 đồng vị 24Mg, 25Mg và 26Mg lần lượt là
78,6%, 10% và 11,4%
c.
Giả sử có 100 nguyên tử Mg thì sẽ có
78,6 nguyên tử 24Mg ; 10 nguyên tử 25Mg ; 11,4 nguyên tử 26Mg
Vậy nếu có 50 nguyên tử 25Mg thì sẽ có
393 nguyên tử 24Mg và 57 nguyên tử 26Mg