Hoà tan m(g) hỗn hợp gồm FeO, Fe2O3, Fe3o4 vừa đủ hết trong V (ml) H2SO4 0,5M thu được dd A. Chia A làm 2 phần bằng nhau:
- cho dd NaOH vào phần 1 thu được kết tủa rồi nung trong không khí đến khối lượng ko đổi được 8,8 (g) chất rắn
- phần 2 làm mất màu 100 ml KMnO4 0,1M trong môi trường H2SO4 loãng dư. Tính m, V.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, Ta có: \(n_{CO}=\dfrac{6,72}{22,4}=0,3\left(mol\right)=n_{CO_2}\)
Theo ĐLBT KL, có: mhh + mCO = mFe + mCO2
⇒ mFe = 18,2 + 0,3.28 - 0,3.44 = 13,4 (g)
b, Giả sử: \(\left\{{}\begin{matrix}n_{Ca}=x\left(mol\right)\\n_{Mg}=y\left(mol\right)\end{matrix}\right.\)
⇒ x + y = 0,2 (1)
PT: \(Ca+2HCl\rightarrow CaCl_2+H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(CaCl_2+Na_2CO_3\rightarrow CaCO_{3\downarrow}+2NaCl\)
\(MgCl_2+Na_2CO_3\rightarrow MgCO_{3\downarrow}+2NaCl\)
Theo PT: \(\left\{{}\begin{matrix}n_{CaCO_3}=n_{Ca}=x\left(mol\right)\\n_{MgCO_3}=n_{Mg}=y\left(mol\right)\end{matrix}\right.\)
⇒ 100x + 84y = 18,4 (2)
Từ (1) và (2) ⇒ x = y = 0,1 (mol)
Theo PT: \(\left\{{}\begin{matrix}n_{CaCl_2}=n_{Ca}=0,1\left(mol\right)\\n_{MgCl_2}=n_{Mg}=0,1\left(mol\right)\end{matrix}\right.\)
⇒ a = mCaCl2 + mMgCl2 = 0,1.111 + 0,1.95 = 20,6 (g)
Bạn tham khảo nhé!

khi cho Fe vào HCl tạo Fe2+
áp dụng định luật bảo toàn e ta có:
Fe => Fe2+ + 2e 2H+ +2e => H2
nFe = 0,05 mol => mFe=2,8 g => mFe2O3 =7,2g => nFe2O3=0,045 mol
nói chung khi nung kết tủa trong không khí đều tạo Fe2O3 => m (chất rắn)= 7,6 g

- Phần 1:
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(Al_2\left(SO_4\right)_3+6NaOH\rightarrow2Al\left(OH\right)_3+3Na_2SO_4\)
\(Al\left(OH\right)_3+NaOH\rightarrow NaAlO_2+2H_2O\)
\(FeSO_4+2NaOH\rightarrow Fe\left(OH\right)_{2\downarrow}+Na_2SO_4\)
\(4Fe\left(OH\right)_2+O_2\underrightarrow{t^o}2Fe_2O_3+4H_2O\)
Ta có: \(n_{Fe_2O_3}=\dfrac{8}{160}=0,05\left(mol\right)\)
Theo PT: \(n_{Fe}=n_{FeSO_4}=n_{Fe\left(OH\right)_2}=2n_{Fe_2O_3}=0,1\left(mol\right)\)\
- Phần 2:
\(2Al+2NaOH+2H_2O\rightarrow2NaAlO_2+3H_2\)
Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo PT: \(n_{Al}=\dfrac{2}{3}n_{H_2}=0,1\left(mol\right)\)
%m trong 1 phần cũng là %m trong A.
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,1.56}{0,1.56+0,1.27}.100\%\approx67,47\%\\\%m_{Al}\approx32,53\%\end{matrix}\right.\)

Theo gt ta có: $n_{NO}=0,015(mol);n_{NaOH}=0,45(mol);n_{Fe_2O_3}=0,05(mol)$
Quy hỗn hợp về Fe và O
Bảo toàn e ta có: $n_{O}=0,1275(mol)$
Ta có: $n_{n_{Fe(OH)_3}=0,3(mol)\Rightarrow n_{H^+/du}=0,15(mol)$
Dùng phương trình $H^+$ ta được $n_{HNO_3}=0,465(mol)$
$\Rightarrow \%m_{HNO_3}=46,5\%$
n Fe2O3 = 8/160 = 0,05(mol)
=> n Fe(OH)3 = 2n Fe2O3 = 0,1(mol)
Ta có :
n NaOH = n HNO3(dư) + 3n Fe(OH)3
=> n HNO3 dư = 0,45 - 0,1.3 = 0,15(mol)
n NO = 0,015(mol)
Bảo toàn electron :
3n Fe = 2n O + 3n NO
<=> n O = (0,1.3 - 0,015.3)/2 = 0,1275(mol)
Phân bổ H+ :
n HNO3 = n HNO3 pư + n HNO3 dư = 2n O + 4n NO + n HNO3 dư
= 0,1275.2 + 0,015.4 + 0,15 = 0,465(mol)
C% HNO3 = 0,465.63/63 .100% = 46,5%

m dd A = 4 . 79,3 = 317,2g
Qui đổi hỗn hợp FeO, Fe2O3, Fe3O4về Fe3O4 có số mol là a
Ta có 232a + (a . 4 . 1,5 . 98) : 0,2 = 317,2
=> a = 0,1 mol
Dd ban đầu
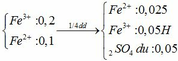
Phần 1:
8H2SO4 + 2KMnO4 + 10FeSO4 → 5Fe2(SO4)3 + 8H2O + 2MnSO4 + K2SO4
0,05 0,025
=> FeSO4 phản ứng hết
=> nKMnO4 = 0,005mol
=> V1= 0,1 lít = 100ml
Phần 2:
2Fe2+ + Br2 → 2Fe3+ + 2Br-
0,025 0,0125
=> V2 = 0,25 lít = 250ml
Phần 3:
2Fe3+ + 2I- → 2Fe2+ + I2
0,05 0,05
=> V3 = 1 lít = 1000ml
Phần 4:
Fe2+ + CO32- → FeCO3↓
0,025 0,025 0,025
2Fe3+ + 3CO32- + 3H2O → 2Fe(OH)3 + 3CO2
0,05 0,075 0,05 0,075
2H+ + CO32- →CO2 + H2O
0,1 0,05 0,05
=> nCO2 = 0,125
=> V4 = 2,8 lít
m kết tủa = mFeCO3 + mFe(OH)3 = 8,25g
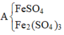
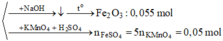


Quy hh về FeO : a mol và Fe2O3: b mol (trong từng phần)
Phần 1: mFe2O3=8,8g --> nFe2O3=0,055 mol -->a/2 +b=0,055
Phần 2: nKMnO4=0,01 mol -->n Fe2+=0,05=nFeO=a
-->b=0,03 mol
m=16,8 g ; nH2SO4=nO=0,28 mol -->V=0,56l