Khử hoàn toàn 16g bột oxit sắt bằng CO ở nhiệt độ cao. Sau phản ứng kết thúc thấy khối lượng chất rắn giảm 4,8g.
a) Xác định CTHH của oxit sắt trên?
b) Dẫn chất khí thu được qua dung dịch Ca(OH)2 dư. Tính khối lượng kết tủa tạo thành
c) Tính thể tích CO cần dùng cho phản ứng trên biết rằng phải dùng CO dư 10% so với lí thuyết và thể tích các chất khí đo ở ĐKTC
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nFe = 11,2/56 = 0,2 mol , Gọi CT Oxit sắt là Fe2OnII
PTPƯ: Fe2On + nCO ---> 2Fe + nCO2
0,2 mol Fe -----> 0,1 mol Fe2On
MFe2On =16/0,1= 160 g/mol
⇒ 112 + 16n = 160 ⇒ 16n =48 ⇒n=3
⇒ CTHH: Fe2O3

a)
CTHH: FexOy
\(n_{Fe_xO_y}=\dfrac{16}{56x+16y}\left(mol\right)\)
PTHH: FexOy + yCO --to--> xFe + yCO2
\(\dfrac{16}{56x+16y}\)--------->\(\dfrac{16x}{56x+16y}\)
=> \(\dfrac{16x}{56x+16y}.56=16-4,8=11,2\)
=> \(\dfrac{x}{y}=\dfrac{2}{3}\Rightarrow Fe_2O_3\)
\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3CO --to--> 2Fe + 3CO2
0,1------>0,3--------------->0,3
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,3----->0,3
=> \(m_{CaCO_3}=0,3.100=30\left(g\right)\)
b) nCO (thực tế) = 0,3.110% = 0,33(mol)
=> VCO = 0,33.22,4 = 7,392(l)

Đáp án C
Phản ứng của oxit + CO thực chất là:
CO + [O] → CO2
=> mchất rắn giảm = mO pứ = 4,8g => nO = 4,8 : 16 = 0,3 mol
=> mFe = mOxit – mO = 16 – 4,8 = 11,2 => nFe = 11,2 : 56 = 0,2 mol
=> nFe : nO = 0,2 : 0,3 = 2 : 3
=> Oxit là Fe2O3

Oxit sắt : FexOy
\(CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ n_{CO_2} = n_{CaCO_3} =\dfrac{22,5}{100} = 0,225(mol)\\ Fe_xO_y + yCO \xrightarrow{t^o} xFe + yCO_2\\ n_{oxit} = \dfrac{n_{CO_2}}{y} = \dfrac{0,225}{y}(mol)\\ \Rightarrow \dfrac{0,225}{y}(56x + 16y) = 12\\ \Rightarrow \dfrac{x}{y} = \dfrac{2}{3}\)
Vậy CTHH của oxit : Fe2O3

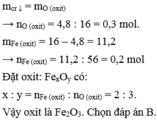
a. áp dụng định luật bảo toàn nguyên tố
=> 4,8 g là khối lượng O trong oxit sắt
=> nO = 0,3 ; nFe = 0,2
CT oxit sắt là Fe2O3
b. Fe2O3 + 3CO ---> 2Fe + 3CO2
nCO = 0,3 mol
dùng dư 10% => nCO = 0,3 x 110% = 0,33 mol
CÂU C BN TỰ LM NHA, LƯỜI WÁ
Gọi công thức oxit sắt:Fex0y.
Fex0y+yCO=>xFe+yC02
0.2/x------------>0.2(mol)
_Sau pư khối lượng chất rắn giảm 4.8 g so với ban đầu:
=>mFe=16-4.8=11.2(g)
=>nFe=11.2/56=0.2(mol)
=>n(Fex0y)=0.2/x(mol)
Mà nFex0y=16/(56x+16y) (mol)
=>16x=0.2(56x+16y)
<=>4.8x=3.2y
<=>x/y=2/3
Vậy công thức oxit sắt là Fe203.
_Khí sinh ra là C02 cho tác dụng với dd NaOH:
nC02=0.2*3=0.6(mol)
_Khối lượng dd tăng cũng chính là khối lượng C02 tham gia:
C02+2NaOH=>Na2S03+H20
0.6--->1.2-------->0.6(mol)
=>mC02=0.6*44=26.4(g)