Ở điều kiện thường, kim loại M có cấu trúc mạng lập phương tâm khối trong đó thể tích của các nguyên tử chiếm 68% thể tích tinh thể. D của M = 7,2g/cm2. Nếu coi nguyên tử M dạng hình cầu thì bán kính gần đúng của nó là 0,125nm. Tìm M?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Khối lượng riêng của Cr là 7,2 g/cm3;
nghĩa là 7,2 gam Cr ↔ 7,2 ÷ 52 × 6,023 × 1023 hạt nguyên tử Cr chiếm thể tích là 1cm3 = 10-6 m3.
Lại để ý: mỗi nguyên tử chỉ chiếm 68% thể tích tinh thể (còn lại là rỗng),
nghĩa là thể tích thực của mỗi nguyên tử Crom là:
V1 nguyên tử = 10-6 × 0,68 ÷ (7,2 ÷ 52 × 6,023 × 1023)) = 4 ÷ 3πr3.
Bấm fx CASIO có ngay r = 1,25 × 10-10 m = 0,125 nm.
ta chọn đáp án B.

Đáp án A
xét 1 mol nguyên tủ Crom: có số nguyên tử Crom là 6.022. 10 23 nguyên tử và khối lượng là 52.
Thể tích của 1 mol nguyên tử Crom là:
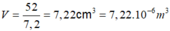
Thể tích thực của 1 nguyên tử Crom là:
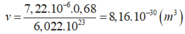
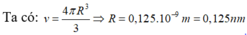

Thể tích của nguyên tố R: \(V_1=\dfrac{M}{d}\)
Giả thiết rằng, trong tinh thể R các nguyên tử là những hình cầu chiếm 74%
=> Thể tích của tất cả nguyên tử là:\(V_2=V_1.0,74\)
Thể tích của từng nguyên tử là: \(V_3=\dfrac{V_2}{6,023.10^{23}}\)
Mặt khác: \(V_3=\dfrac{4}{3}.pi.R^3=3,178.10^{-23}cm^3\)
\(\Rightarrow M=\dfrac{3,178.10^{-23}.6,023.10^{23}.1,55}{0,74}=40\)
=> R là Ca

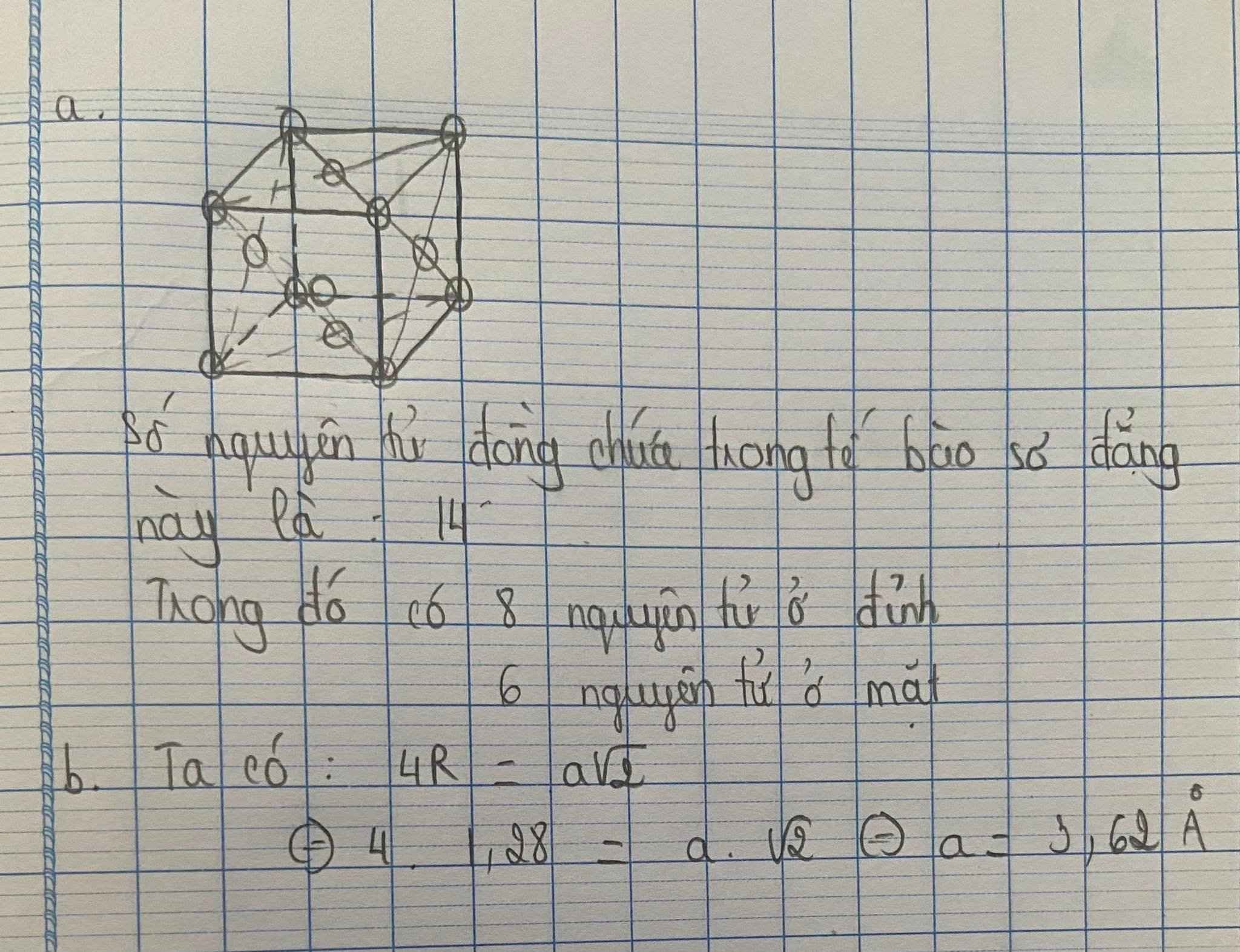
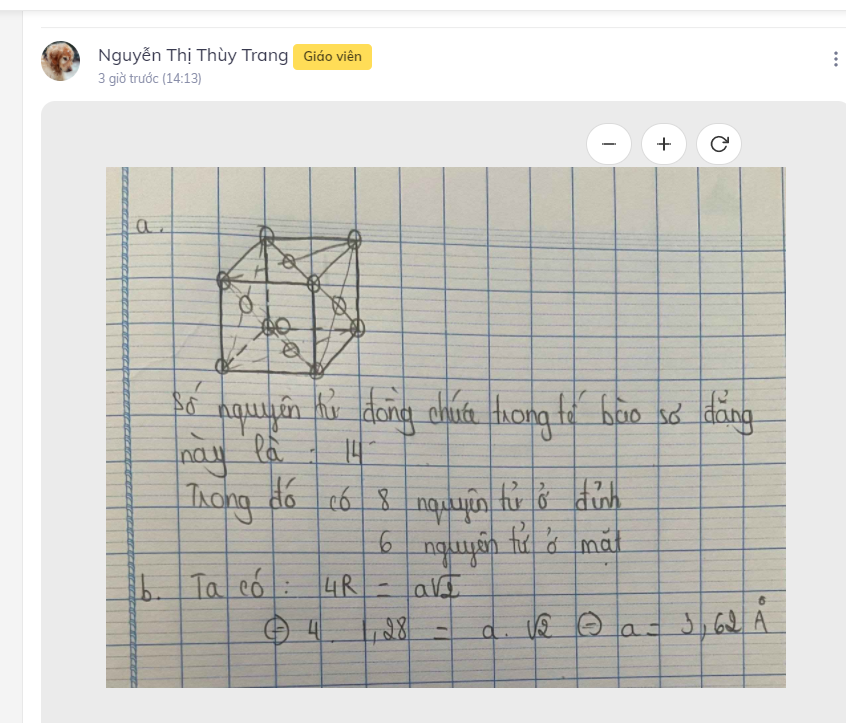
TL:
Thể tích của M là V = 0,68.(4/3).pi.r3 = 0,68.(4/3).3,14.(0,125.10-7 cm)3.
Khối lượng riêng: d = m/V = 7,2 g/cm3.
Suy ra: m = 7,2.V (g).
Khối lượng nguyên tử: M = m.NA = m.6,023.1023 \(\simeq\) 24 g/mol.
Như vậy, M là Mg.