Cho 6,2g Oxit kim loại M hóa trị I tác dụng với H2O dư được dung dịch A có tính kiềm.Chia A thành 2 phần bằng nhau:
Phần I:Cho tác dụng với 95ml dung dịch HCl 1M,thấy dng dịch sau phản ứng làm xanh quỳ tím
Phần II:Cho tác dụng với 55ml dung dịch HCl 2M,thấy dung dịch sau phản ứng làm đỏ quỳ tím
Xác định công thức oxit của M.Gọi tên
nêu cả cách giải vs

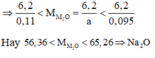


gọi Oxit kim loại M là A2O
cho M tác dụng với H2O dư được dung dịch A có tính kiềm
PTHH: \(A2O+H2O->2AOH\)(1)
theo phần 1 khi cho dung dịch thu được trong pư(1) tác dụng vs dd HCl (95ml) thấy dung dịch sau pư làm quỳ tím xanh
=>AOH+HCL\(->ACL+H2O\)
ta có \(C\left(HCL\right)=\dfrac{nHCL}{VHCL}=>nHCL=VHCl.C\left(HCL\right)=\dfrac{95}{1000}.1=0,095mol\)
do dung dịch sau pư LÀM quỳ tím háo xanh=>AOH dư
=>nA2O>nHCL=>nA2O>0,095(2)
theo phần 2 vì khi cho dung dịch thu đc sau pư (1) Cho tác dụng với 55ml dung dịch HCl 2M,thấy dung dịch sau phản ứng làm đỏ quỳ tím
=>pthh: AOH+HCL->ACL+H2O
tương tự trên =>\(nHCL=2.\dfrac{55}{1000}=0,11mol\)
vì sau pư thấy dd làm đỏ q tím=>HCL còn dư=>nA2O<nHCL=0,11(3)
từ(2)(3)=>0,095<nA2O<0,01=>\(\dfrac{6,2}{0,095}>\dfrac{6,2}{nA2O}>\dfrac{6,2}{0,11}\)
=>65,2>MA2O>56,3=>MA2O=62(g/mol)=>A là Na=>ct : NA2O
natri oxit