
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 4. Axit axetic có công thức C2H402. Hãy tính thành phần phần trăm khối lượng của các nguyên tố trong axit axetic.
Lời giải:
Từ C2H4O2 ta có: M = 60 g/mol; mC = 2 x 12 = 24 g; mH = 4 x 1 = 4 g;
MO = 2 x 16 = 32 g.
%C = (24 : 60) x 100% = 40%; %H = (4 : 60) x 100% = 6,67%;
%O = 100% - 40% - 6,67% = 53,33%.

Số mol C2H5OH = 9,2 : 46 = 0,2 (mol).
Phương trình phản ứng cháy :
C2H5OH + 3O2 -> 2CO2 + 3H2O.
0,2 0,6 0,4 mol
Thể tích khí CO2 tạo ra là : V = 0,4.22,4 = 8,96 (lít).
b) Thể tích khí oxi cần dùng là : V1 = 0,6 . 22,4 = 13,44 (lít).
Vậy thể tích không khí cần dùng là Vkhông khí = (lít).

PTHH: CaCO3 → CaO + CO2 ↑
MgCO3 → MgO + CO2 ↑
Gọi số mol của MgCO3 là a, số mol của CaCO3 là b
=> Số mol của CO2 sinh ra ở pt(1) là a , số mol CO2 sinh ra ở pt(2) là b
Số mol của CO2 là: 3,36 : 22,4 = 0,15 mol
Ta có hệ phương trình sau:
- 100a + 84b = 14,2
- a + b = 0,15
=> a = 0,1 mol , b = 0,05 mol
Khối lượng của CaCO3 là: 0,1 . 100 = 10gam
%CaCO3 trong hỗn hợp ban đầu là:
(10 : 14,2).100% = 70,423%
%MgCO3 trong hỗn hợp ban đầu là:
100% - 70,423% = 29,577%


P/s: Chị tag e khi e không biết làm kkk. Nên e vào mấy câu tương tự mà thấy mấy câu đó chia hết mà mấy câu này e chia không hết nên sai thì thôi nhá chị! (Không nhận đá gạch ạ)
a) M Na2CO3.10H2O = 23.2+12+16.3+10.(2.1+16) = 286
\(\%m_{H2O}=\frac{18.10}{286}.100\%=62,94\%\)
b) M CaSO4.2H2O = 40 + 32 +16.4 + 2.(2.1 + 16) = 172
\(\%m_{H2O}=\frac{18.2}{172}.100\%=20,93\%\)

Bài Làm:
a, \(M_{SO_2}=32+16.2=64\) (g/mol)
Trong 1 mol SO2 có 1 mol S và 2 mol O
\(\%m_S=\frac{32}{64}.100\%=50\%\)
\(\%m_O=\frac{16.2}{64}.100\%=50\%\)
Vậy ...
b, \(M_{Fe_2\left(SO_4\right)_3}=56.2+\left(32+16.4\right).3=400\) (g/mol)
Trong 1 mol Fe2(SO4)3 có 2 mol Fe, 3 mol S và 12 mol O.
\(\%m_{Fe}=\frac{56.2}{400}.100\%=24\%\)
\(\%m_S=\frac{32.3}{400}.100\%=24\%\)
\(\%m_O=100\%-24\%-24\%=48\%\)
Vậy ...
Good luck!

M Al2O3.2SiO2.2H2O =258
%mAl = \(\dfrac{54.100\%}{258}\)=20,93%

có ở trên mạng nha
https://vn.answers.yahoo.com/question/index?qid=20120515074638AAH9nU1
http://viplam.net/diendan

Giả sử: hh khí có 1 mol
Đặt:
nCO= x mol
nH2= y mol
\(\overline{M}\)=12.7*2=25.4g
<=> \(\frac{28x+2y}{x+y}=25.4\)
<=> 28x + 2y= 25.4 (1)
Mặt khác:
x + y = 1 (2)
Giải (1) và (2) :
x= 0.9
y= 0.1
mCO= 0.9*28=25.2g
mH2= 0.1*2=0.2g
%mCO= 99.21%
%mH2= 0.79%
%VCO= 90%
%VH2=10%

a) PTHH: Na2CO3 + H2SO4 -> Na2SO4 + H2O + CO2
nCO2= 1,68/22,4= 0,075(mol)
=> nNa2CO3= nCO2=nH2SO4=nNa2SO4(sản phẩm)= 0,075(mol)
=> mNa2CO3= 0,075. 106=7,95(g)
=> %mNa2CO3= (7,95/9,37).100 \(\approx\)84,845%
b) mH2SO4= 98.0,075= 7,35(g)
=> mddH2SO4= (7,35.100)/9,8= 75(g)
c) mddsau = m(hỗn hợp A)+ mddH2SO4- mCO2= 9,37+75-0,075.44=81,07(g)
Chất tan trong dd sau phản ứng chỉ có Na2SO4
mNa2SO4= mNa2SO4(hỗn hợp A) + mNa2SO4(sản phẩm)= (9,37-7,95)+0,075.142=12,07(g)
=> C%ddNa2SO4= (12,07/81,07).100\(\approx\) 14,888%
Đặt số mol Na2CO3 và Na2SO4 lần lượt là a và b
Ta có :
\(\text{106a+142b=9.37}\)
\(\text{a. Na2CO3+ H2SO4}\rightarrow\text{Na2SO4+H2O+CO2}\)
\(\text{nCO2=}\frac{1,68}{22,4}\text{=0.075=nNa2CO3=a}\)
\(\rightarrow\text{mNa2CO3=0,075.106=7,95}\)
\(\rightarrow\text{%mNa2CO3}=\frac{\text{7,95}}{\text{9,37}}.100\%\text{=84,84%}\)
\(\rightarrow\text{%mNa2SO4=15,16%}\)
b.nH2SO4=nCO2=0,075
\(\rightarrow\)mH2SO4=0,075.98=7,35g
\(\rightarrow\text{mdd H2SO4}=\frac{\text{7.35}}{9,8}.100\%\text{=75g}\)
c.mdd sau phản ứng=9,37+mddH2SO4-mCO2
=9,37+75-0,075.44=81,07
mNa2SO4 tạo ra là 0,075.142=10,65
\(\rightarrow\)Tổng khối lượng \(Na2SO4=\text{10,65+9,37-7,95=12,07}\)
\(\rightarrow C\%Na2SO4=\frac{12,07}{81,07}.100\%=\text{14,88%}\)
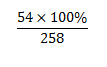 =20,93%
=20,93%