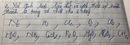Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

HD:
Coi hh X chỉ gồm 2 nguyên tố là Fe (x mol) và O (y mol). Ta có: 56x + 16y = 3 (1).
Theo đề bài ta có:
Fe - 3e = Fe+3.
x 3x
O + 2e = O-2;
y 2y
N+5 +3e = N+2
0,075 0,025 mol
Như vậy ta có: 3x = 2y + 0,075 (2).
Giải hệ (1) và (2) thu được: x = 0,045; y = 0,03 mol.
Như vậy: m = 56.x = 2,52 g.
Gọi x,y lần lượt là số mol của Fe, O
Ta có: 56x + 16y = 3 (1)
Ta lại có: \(Fe^0\rightarrow Fe^{+3}+3e\)
O\(^0\)+2e\(\rightarrow\)O\(^{-2}\)
N\(^{+5}\) + 3e \(\rightarrow\) N\(^{+2}\)
Áp dụng định luật bảo toàn e:
=> 3x - 2y = 0.025x3 (2)
Giải hpt (1),(2) => x = 0.045 (mol); y = 0.03 (mol)
m\(_{Fe}\) = n.M = 0.045x56 = 2.52g

Cẩm Vân Nguyễn Thị Hong Ra On Hồ Hữu Phước Hoàng Tuấn Đăng
nFe3O4 = 0,1 => nFe2+=0,1 và nFe3+=0,2.
Vì Al tác dụng với dd X thì thu được dd Y, suy ra không tạo thành kim loại Fe.
PT ion: 3Fe3+ + Al -> 3Fe2+ + Al3+
..............3x..........x........3x..........x
Khi nung toàn bộ kết tủa trong không khí thì thu được 25,275g chất rắn.
Vì 25,275 > mFe2O3 (=0,15*160=24g) , suy ra trong lượng chất rắn đó có Al2O3.
=> nAl2O3=0,0125 => nAl3+ =0,025=x.
=> nFe3+(pứ) =3x=0,075
=> nFe3+(ddY)=0,2-0,075=0,125
=> nFe2+(ddY)=0,1+0,075=0,175
=> nOH = 3nFe3+(ddY) + 2nFe2+(ddY) +3nAl3+ =0,8 > nNaOH (đã cho) (=0,725)
Đề hình như sai.
Cô nghĩ là cho sai số liệu chất rắn sau khi nung. Vì lượng NaOH cho vào đến khi ion Fe kết tủa hoàn toàn thì ion Al chưa kết tủa. Nên chất rắn sau khi nung không thể chứa Al2O3 được.

Từ 23/7 -> 26/7 không phải là hết ngày 26 à cô ==''
Em lỡ kế hoạch rồi =="" còn câu 6 nữa định mai làm ==""

Dễ thấy :
Với X , từ I2 lên I3 tăng đột ngột , vậy ion \(X^{2+}\) có cấu hình của một khí hiếm nên :
\(X:\left[Ar\right]4s^2\left(Ca\right)\)
Với Y , từ I4 lên I5 tăng đột ngột , vậy ion \(I^{4+}\)có cấu hình của một khí hiếm nên :
\(Y:\left[He\right]2s^22p^2\left(C\right)\)
Vậy ...
P/s : bài này mk có lm rồi :D

Iot bị lẫn tạp chất NaI vào nước, sau đó sục khí clo vào dung dịch để oxi hóa I- thành I2, để tận thu I2 ta đun nóng nhẹ ở áp suất khí quyển, I2 thăng hoa thành hơi màu tím.
Cl2 + NaI → 2NaCl + I2
Iot bị lẫn tạp chất NaI .Iot bị lẫn tạp chất NaI . Làm thế nào để loại bỏ tạp chất đó.Hướng dẫn giải:Iot bị lẫn tạp chất NaI vào nước, sau đó sục khí clo vào dung dịch để oxi hóa I- thành I2, để tận thu I2 ta đun nóng nhẹ ở áp suất khí quyển, I2 thăng hoa thành hơi màu tím.pt:2NaI +Cl2--->2NaCl+I2

mHF =\(\frac{40.2,5}{100}\) = 1kg
Phương trình phản ứng hóa học:
CaF2 + H2SO4 ---> CaSO4 + 2HF
78kg 40kg
X kg 1 kg
mCaF2 cần dùng: \(\frac{1.78}{40}.\frac{100}{80}\) = 2,4375 kg
mHF = = 1kg
Phương trình phản ứng hóa học:
CaF2 + H2SO4 CaSO4 + 2HF
78kg 40kg
X kg 1 kg
cần dùng:
= 2,4375 kg

cho lần lượt từng dund dịch vào dd AgNO3 dung dịch nào tạo kết tủa trắng là NaCl,dung dịch còn lại là NaF.pt: NaCl+AgNO3---->AgCl(kết tủa trắng)+NaCl.
còn NaF không phản ứng với AgNO3.
Cho dung dịch AgNO3 vào 2 mẫu thử chứa dung dịch NaF và dung dịch NaCl, mẫu thử nào có kết tủa trắng là NaCl, còn lại không tác dụng là NaF.
AgNO3 + NaF → không phản ứng( AgF dễ tan trong nước)
AgNO3 + NaCl → AgCl ↓ + NaNO3