hòa tan 6,5g Zn và dung dịch Hcl 3,65% vừa đủ
a)Viết phương trình hóa học
b)TÍnh khối lượng dung dịch HCl
c)Dung dịch HCl phản ứng
d)Tính c% của dung dịch sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Em dùng bảng tính tan để tra nhé, nó sẽ rất đầy đủ í.

\(CaSiO_3:20+14+8.3=58\\ H_3PO_4:3+15+8.4=50\\ Al_2\left(SO_4\right)_3:13.2+\left(16+8.4\right).3=170\\ KMnO_4:19+25+8.4=76\\ Na_2S:11.2+16=38\\ BaCl_2:56+17.2=90\)

Gọi CTPT của Y là \(C_xH_yO_z\)
Ta có: \(n_{O_2}=\dfrac{4}{32}=0,125\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{CO_2}=x\left(mol\right)\\n_{H_2O}=y\left(mol\right)\end{matrix}\right.\Rightarrow x:y=2:1\left(1\right)\)
Theo ĐLBTKL: \(m_Y+m_{O_2}=m_{CO_2}+m_{H_2O}\)
`=>` \(m_{CO_2}+m_{H_2O}=4+3,95=7,95\left(g\right)\)
`=> 44x + 18y = 7,95 (2)`
Từ `(1), (2) =>` \(\left\{{}\begin{matrix}x=0,15\left(mol\right)\\y=0,075\left(mol\right)\end{matrix}\right.\) `=>` \(\left\{{}\begin{matrix}n_C=0,15\left(mol\right)\\n_H=0,15\left(mol\right)\end{matrix}\right.\)
\(\xrightarrow[]{\text{BTNT O}}n_{O\left(Y\right)}+2n_{O_2}=2n_{CO_2}+n_{H_2O}\)
`=>` \(n_{O\left(Y\right)}=2.0,15+0,075-0,125.2=0,125\left(mol\right)\)
`=>` \(x:y:z=0,15:0,15:0,125=6:6:5\)
Do Y có CTPT trùng với CTĐGN `=>` CTPT của Y là `C_6H_6O_5`
Mà Y phản ứng với NaOH với tỉ lệ mol 1 : 2
`=>` Y là este 2 chức và có gốc ancol tạo thành tử etylen glicol
`=>` CTCT của Y là \(HOOC-C\equiv C-COOC_2H_4OH\)
`=>` X là \(HOOC-C\equiv C-COOH\)
`- A` đúng vì `6 + 2 = 8`
`- B` sai do X có chứa liên kết \(C\equiv C\) nên không có đồng phân hình học
`- C` đúng vì trong CTCT của Y không có gốc \(-CHO\)
`- D` đúng vì có liên kết \(C\equiv C\) trong CTCT
Bai nay lam gi co trong lop 1 :))??
Cai nay cho len lop 11 moi dung :))

Gọi kim loại cần tìm là R
$R + 2HCl \to RCl_2 + H_2$
Theo PTHH : $n_R = n_{H_2} = \dfrac{5,6}{22,4} = 0,25(mol)$
$M_R = \dfrac{10}{0,25} = 40$
Suy ra, kim loại cần tìm là Canxi
HOẶC LÀ
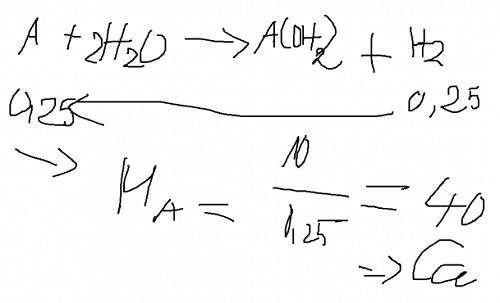
A + 2H2O --> A(OH)2 + H2
0,25 0,25
nH2 = V/22,4 = 5,6/22,4 = 0,25 mol
MA = m/n = 10/0,25 = 40
=> A là Canxi

Gọi CTHH của muối sắt clorua là FeCln \(\left(n\in\left\{2;3\right\}\right)\)
\(m_{FeCl_2}=20.32,5\%=6,5\left(g\right)\Rightarrow n_{FeCl_n}=\dfrac{6,5}{56+35,5n}\left(mol\right)\)
PTHH: \(FeCl_n+nAgNO_3\rightarrow nAgCl\downarrow+Fe\left(NO_3\right)_n\)
\(\dfrac{6,5}{56+35,5n}--\rightarrow\dfrac{6,5n}{56+35,5n}\rightarrow\dfrac{6,5}{56+35,5n}\)
\(Fe\left(NO_3\right)_n+\left(3-n\right)AgNO_3\rightarrow Fe\left(NO_3\right)_3+\left(3-n\right)Ag\downarrow\)
\(\dfrac{6,5}{56+35,5n}------------\rightarrow\dfrac{6,5\left(3-n\right)}{56+35,5n}\)
=> \(108.\dfrac{6,5\left(3-n\right)}{56+35,5n}+143,5.\dfrac{6,5n}{56+35,5n}=17,22\)
=> n = 3
Vậy CTHH của muối sắt là FeCl3
`a)PTHH:`
`Zn + 2HCl -> ZnCl_2 + H_2`
`0,1` `0,2` `0,1` `0,1` `(mol)`
\(b)n_{Zn}=\dfrac{6,5}{65}=0,1(mol)\)
\(=>m_{dd HCl}=\dfrac{0,2.36,5}{3,65}.100=200(g)\)
\(c)\) Đề ko rõ
\(d)C%_{ZnCl_{2}}=\dfrac{0,1.136}{6,5+200-0,1.2}.100=6,6%\)
Chưa có đề bài mà có lệnh hỏi là sao em nhỉ?