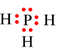BÙI GIA HÂN
Giới thiệu về bản thân



































khối lượng dung dịch glucose là:
mdd = Vdd x Vdd = 500ml x 1,1g/ml = 550(g)
khối lượng glucose là:
mglucose = 5% x mdd = 0,05 x 550 = 27,5(g)
khối lượng mol của glucose là:
Mglucose = 6(12) + 12(1) + 6(16) = 180(g/mol)
số mol glucose là:
nglucose = \(\dfrac{m_{glucose}}{M_{glucose}}\) =\(\dfrac{27,5}{180}\)=0,1528(mol)
theo phản ứng, 1mol glucose phân huỷ giải phóng 2803,0 kJ năng lượng.
Năng lượng tối đa nhận được từ 0,1528 mol glucose là:
E= 0,1528 x 2803,0= 428,3 kJ
a) chất khử: HCl ; chất oxi hoá: MnO2
b) phương trình hoá học của phản ứng:
MnO2 + 4HCl →MnCl2 +Cl2 +2H2O
1.phản ứng toả nhiệt:
- đốt cháy than
- cho vôi sống vào nước
2. phản ứng thu nhiệt
- băng tan
- nung đá vôi
P (Z = 15): 1s22s22p63s23p3 Þ P có 5 electron hóa trị cần thêm 3 electron để đạt octet.
H (Z = 1): 1s1 Þ H có 1 electron hóa trị cần thêm 1 electron để đạt octet.
Khi hình thành liên kết, P góp chung 3 electron với 3 electron của 3 H ⇒ Trong PH3, xung quanh P có 8 electron giống khí hiếm Ar còn 3 H đều có 2 electron giống khí hiếm He.