Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Lý thuyết SVIP
I. ĐỊNH NGHĨA, PHÂN LOẠI
1. Định nghĩa
Ancol là những hợp chất hữu cơ trong phân tử có nhóm hidroxyl -OH liên kết trực tiếp với nguyên tử cacbon no. Nhóm -OH này được gọi là nhóm -OH ancol.


2. Phân loại
- Dựa vào đặc điểm gốc hidrocacbon
| Ancol no, đơn chức, mạch hở | Phân tử có một nhóm -OH liên kết với gốc ankyl: CnH2n+1OH Ví dụ: C2H5OH, C3H7OH... |
| Ancol không no, đơn chức, mạch hở | Phân tử có một nhóm -OH liên kết với nguyên tử cacbon no của gốc hidrocacbon không no. Ví dụ: CH2=CH-CH2-OH |
| Ancol thơm, đơn chức | Phân tử có nhóm -OH liên kết với nguyên tử cacbon no thuộc mạch nhánh của vòng benzen. Ví dụ: |
| Ancol vòng no, đơn chức | Phân tử có một nhóm -OH liên kết với nguyên tử cacbon no thuộc gốc hidrocacbon vòng no. |
- Dựa vào số nhóm -OH trong phân tử
| Ancol đơn chức | Phân tử chỉ có 1 nhóm -OH Ví dụ: |
| Ancol đa chức | Phân tử có từ 2 hay nhiều nhóm -OH. Ví dụ: |
- Dựa vào bậc của nguyên tử cacbon no liên kết với nhóm -OH
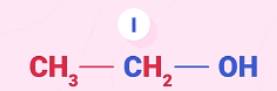
| Ancol bậc I | Nhóm -OH liên kết trực tiếp với nguyên tử cacbon no bậc I. Ví dụ: |
| Ancol bậc II | Nhóm -OH liên kết trực tiếp với nguyên tử cacbon no bậc II. Ví dụ: |
| Ancol bậc III | Nhóm -OH liên kết trực tiếp với nguyên tử cacbon no bậc III. Ví dụ: |
II. ĐỒNG PHÂN, DANH PHÁP
1. Đồng phân
Các ancol no, đơn chức, mạch hở có đồng phân mạch cacbon và đồng phân vị trí nhóm -OH.
Ví dụ: Ancol C4H10O có bốn đồng phân sau:


2. Danh pháp
- Tên thông thường
Một số ít ancol có tên thông thường.
| Tên thông thường ancol = Ancol + tên gốc ankyl + "ic" |
Tên gọi một số gốc ankyl phân nhánh thường gặp:
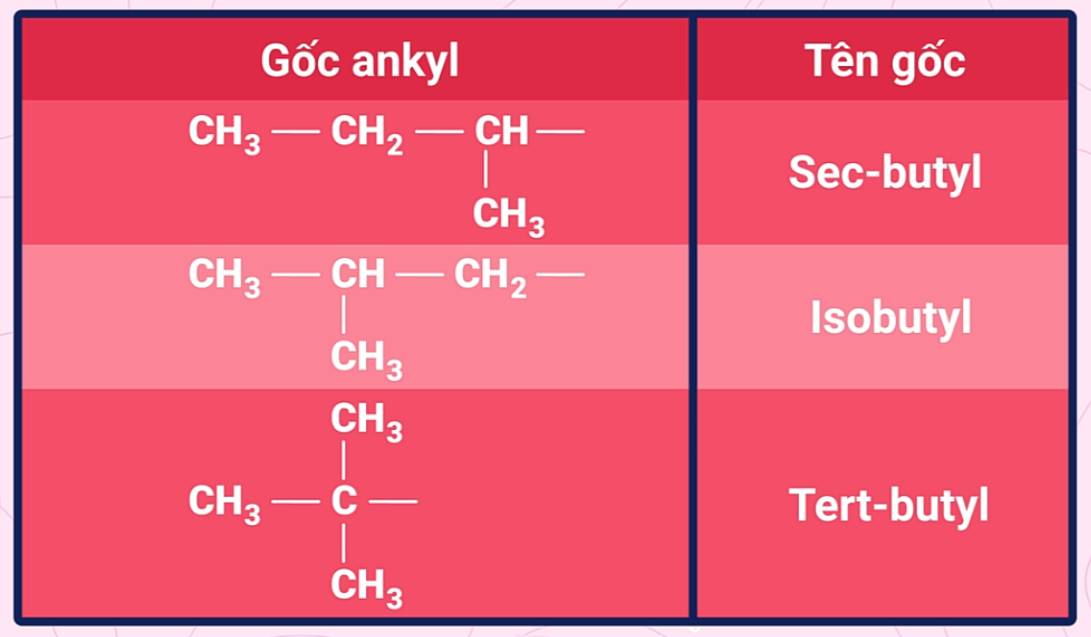
Ví dụ: C2H5OH ancol etylic
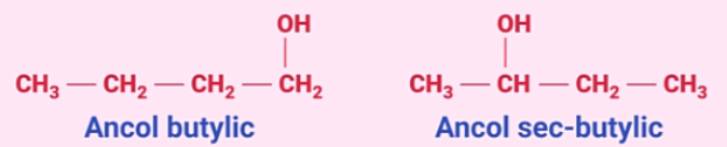
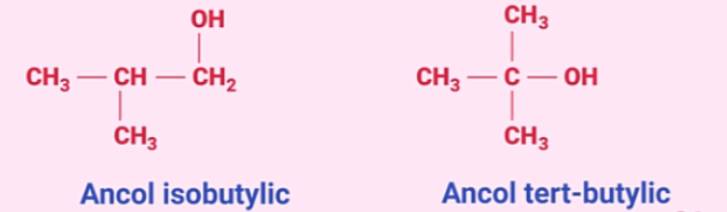
- Tên thay thế
Ancol được gọi tên theo danh pháp thay thế như sau:
| Tên hidrocacbon tương ứng với mạch chính + số chỉ vị trí nhóm -OH + "ol" |
Lưu ý: Mạch chính của phân tử ancol là mạch cacbon dài nhất liên kết với nhóm -OH. Khi đánh số thứ tự nguyên tử cacbon mạch chính phải đánh số bắt đầu từ phía gần nhóm -OH hơn.
Ví dụ:
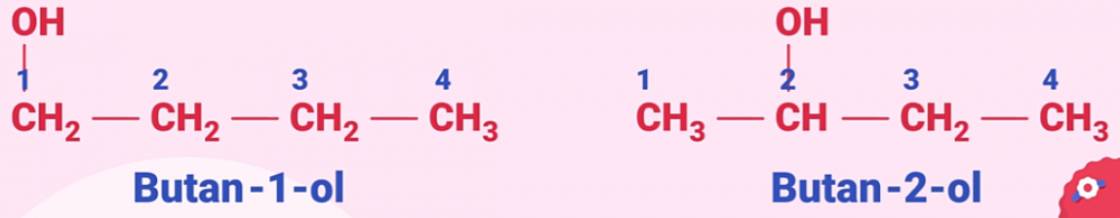

III. TÍNH CHẤT VẬT LÝ
- Các ancol là chất lỏng hoặc chất rắn ở điều kiện thường.
- Nhiệt độ sôi, khối lượng riêng tăng theo chiều tăng của phân tử khối, còn độ tan trong nước thì lại giảm khi phân tử khối tăng.
- Ancol có nhiệt độ sôi cao hơn đáng kể so với các hidrocacbon hay ete có cùng số nguyên tử cacbon trong phân tử do giữa các phân tử ancol có liên kết hidro.
- Các ancol đầu mạch (metanol, etanol, propanol) tan vô hạn trong nước, khi tăng số nguyên tử cacbon, độ tan của ancol trong nước giảm mạnh. Sở dĩ các ancol tan nhiều trong nước là vì phân tử ancol tạo được liên kết hidro với các phân tử nước.


Liên kết hidro giữa ancol với nước và liên kết hidro giữa các phân tử ancol với nhau.
IV. TÍNH CHẤT HÓA HỌC
Nguyên tử O có độ âm điện lớn hơn nguyên tử C và H nên các liên kết giữa C-OH và O-H đều phân cực về phía O. Do đó, nhóm -OH, hay nhất là nguyên tử H dễ bị thay thế hoặc tách ra trong các phản ứng hóa học.
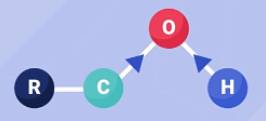
1. Phản ứng thế H của nhóm OH
a) Tính chất chung của ancol
Tác dụng với kim loại kiềm
Thí nghiệm: Cho vào ống nghiệm khô khoảng 5 ml etanol, sau đó cho vào ống nghiệm một mẩu natri bằng hạt đỗ và quan sát hiện tượng.
Hiện tượng: Mẩu natri phản ứng với etanol và dần tan ra, có bọt khí không màu tạo thành và thoát ra khỏi dung dịch.
Phương trình hóa học: 2C2H5-OH + 2Na → 2C2H5-ONa + H2
Tổng quát: 2R(OH)n + 2nNa → 2R(ONa)n + nH2
b) Tính chất đặc trưng của glixerol
Các ancol đa chức có từ 2 nhóm chức -OH nằm ở vị trị cạnh nhau trở lên có thể tham gia phản ứng với dung dịch Cu(OH)2 tạo dung dịch màu xam lam.
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O

Các ancol đơn chức không có tính chất này nên phản ứng trên dùng để phân biệt ancol đơn chức với các ancol đa chức có các nhóm -OH nằm cạnh nhau trong phân tử.
2. Phản ứng thế nhóm OH
a) Phản ứng với axit vô cơ
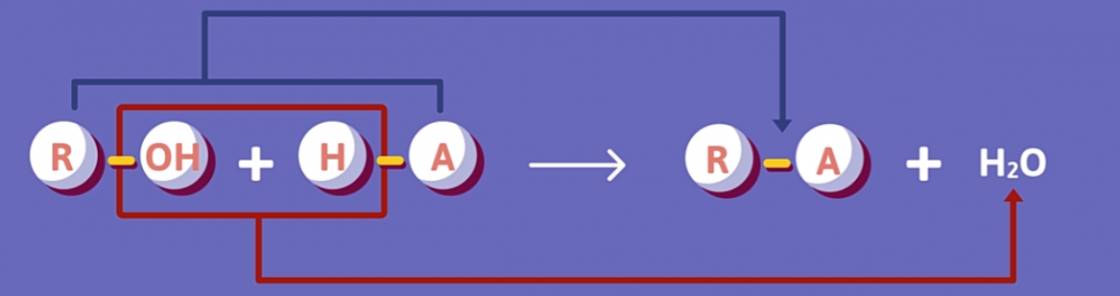
Ví dụ: C2H5-OH + H-Br 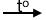 C2H5-Br + H2O
C2H5-Br + H2O
Các ancol khác cũng có phản ứng tương tự. Phản ứng này chứng tỏ phân tử ancol có nhóm -OH.
b) Phản ứng với ancol
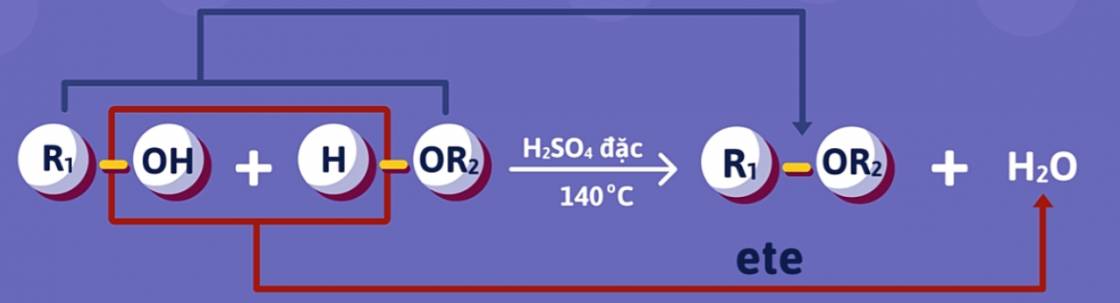
![]()
Số ete tối đa tạo được từ n ancol khác nhau là: \(\dfrac{n\left(n+1\right)}{2}\)
3. Phản ứng tách nước
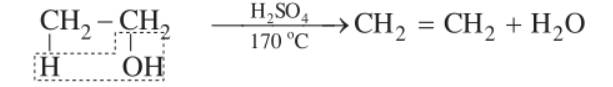
Tính chất này dùng để điều chế etilen trong phòng thí nghiệm.
Trong điều kiện tương tự, các ancol no, đơn chức, mạch hở (trừ metanol) có thể bị tách nước tạo thành anken:
CnH2n+1OH  CnH2n + H2O
CnH2n + H2O
4. Phản ứng oxi hóa
a) Phản ứng oxi hóa không hoàn toàn
- Ancol bậc 1 → Anđehit (-CH=O).
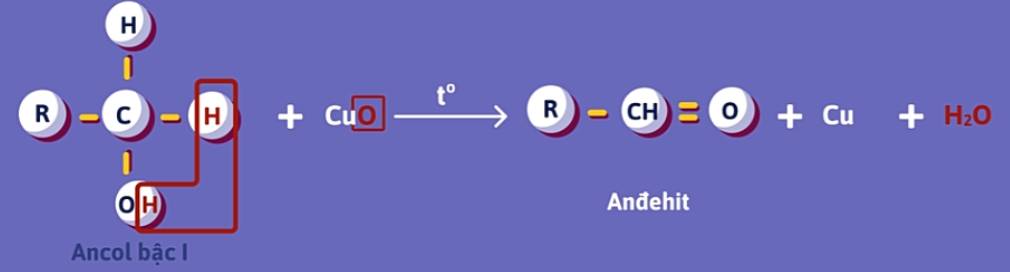
Ví dụ: CH3CH2OH + CuO 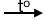 CH3-CHO + Cu + H2O
CH3-CHO + Cu + H2O
- Ancol bậc 2 → Xeton (=C=O)

Ví dụ:
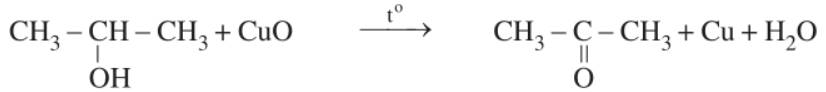
- Ancol bậc 3 không bị oxi hóa

b) Phản ứng oxi hóa hoàn toàn
Khi bị đốt, các ancol cháy tỏa nhiều nhiệt.
Ví dụ: C2H5OH + 3O2 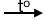 2CO2 + 3H2O
2CO2 + 3H2O
Tổng quát: Khi đốt cháy ancol no, đơn chức mạch hở ta có:
CnH2n+2O + \(\dfrac{3n}{2}\)O2 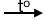 nCO2 + (n+1)H2O
nCO2 + (n+1)H2O
nH2O > nCO2 và nAncol = nH2O - nCO2
V. ĐIỀU CHẾ
1. Phương pháp tổng hợp
Etanol được điều chế từ etilen bằng phản ứng hợp nước có xúc tác ở nhiệt độ cao:
CH2=CH2 + H2O  C2H5OH
C2H5OH
2. Phương pháp sinh hóa
Etanol được điều chế từ các loại nông sản chứa nhiều tinh bột như gạo, ngô, khoai, sắn qua các quá trình thủy phân và lên men.
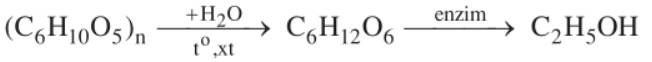
VI. ỨNG DỤNG





Bạn có thể đánh giá bài học này ở đây