Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Lý thuyết SVIP
I. KIẾN THỨC CẦN NHỚ
1. Tính chất hóa học của oxit
| Tính chất | Oxit axit | Oxit bazơ |
Tác dụng với nước
| Nhiều oxit axit như P2O5, SO2, SO3, N2O5... tác dụng với nước tạo thành dung dịch axit. P2O5 + H2O → H3PO4 | Một số oxit bazơ tác dụng được với nước tạo thành dung dịch bazơ tương ứng (kiềm). CaO + H2O → Ca(OH)2 |
| Tác dụng với bazơ/axit | Oxit axit tác dụng với dung dịch bazơ tạo thành muối và nước CO2 + Ca(OH)2 → CaCO3 + H2O | Oxit bazơ tác dụng với axit tạo thành muối và nước. CuO + 2HCl → CuCl2 + H2O |
| Tác dụng với oxit bazơ/oxit axit | Oxit axit tác dụng với một số oxit bazơ tạo thành muối. SO2 + Na2O → Na2SO3 | Một số oxit bazơ tác dụng với oxit axit tạo thành muối. CaO + CO2 → CaCO3 |
Tính chất hóa học của oxit được tóm tắt bằng sơ đồ dưới đây:
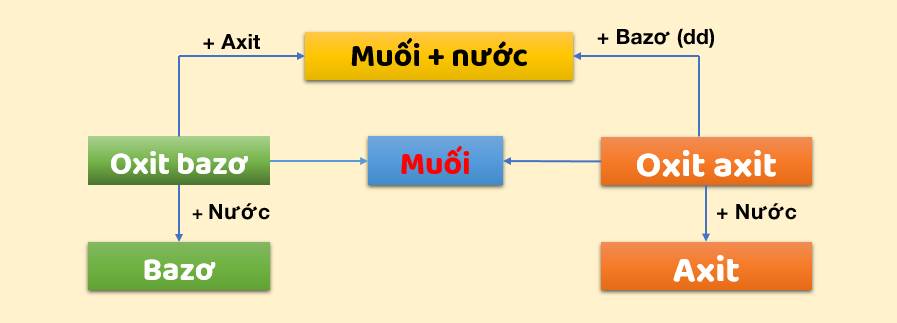
2. Tính chất hóa học của axit
| Tính chất | Axit |
| Làm đổi màu quỳ tím | Axit làm quỳ tím chuyển sang màu đỏ. |
Tác dụng với kim loại | Dung dịch axit tác dụng được với một số kim loại tạo thành muối và giải phóng khí hidro. 2Al + 6HCl → 2AlCl3 + 3H2 |
| Tác dụng với bazơ | Axit tác dụng với bazơ tạo thành muối và nước. Phản ứng của axit với bazơ được gọi là phản ứng trung hòa. Cu(OH)2 + H2SO4 → CuSO4 + 2H2O |
| Tác dụng với oxit bazơ | Axit tác dụng với oxit bazơ tạo thành muối và nước. Fe2O3 + 6HCl → 2FeCl3 + 3H2O |
| Tác dụng với muối | Axit tác dụng với muối tạo muối mới và axit mới. H2SO4 + BaCl2 → BaSO4↓ + 2HCl |
Lưu ý: Axit H2SO4 đặc có những tính chất hóa học riêng như:
- Tác dụng với nhiều kim loại không giải phóng khí hidro.
Cu + 2H2SO4 đặc 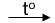 CuSO4 + SO2 + 2H2O
CuSO4 + SO2 + 2H2O
- Tính háo nước, hút ẩm.
C12H22O11 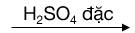 12C + 11H2O
12C + 11H2O
Tính chất hóa học của axit được tóm tắt qua sơ đồ sau
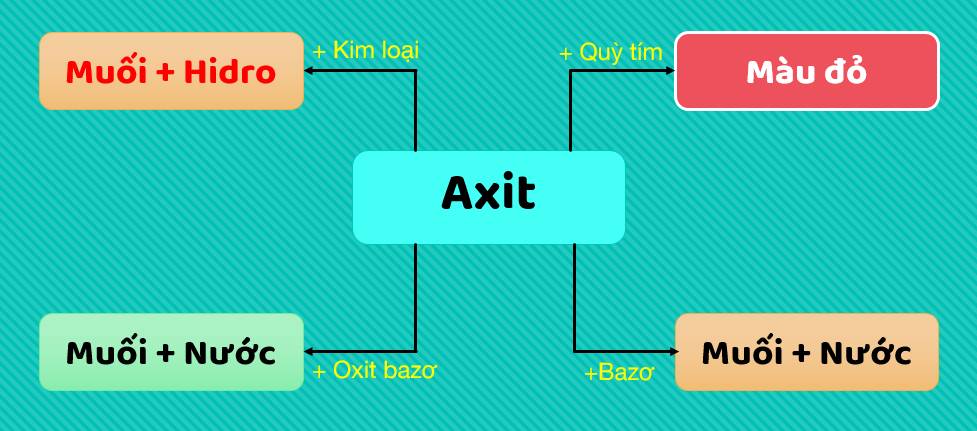
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!

Bạn có thể đánh giá bài học này ở đây