Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(2X+2H_2O\rightarrow2XOH+H_2\\ n_{H_2}=\dfrac{0,3}{2}=0,15\left(mol\right)\\ n_X=2.0,15=0,3\left(mol\right)\\ M_X=\dfrac{8,5}{0,3}\approx28,333\\ \Rightarrow M_{Na}< M_X< M_K\left(23< 28,333< 39\right)\\ Đặt:n_{Na}=a\left(mol\right);n_K=b\left(mol\right)\\ \Rightarrow\left\{{}\begin{matrix}23a+39b=8,5\\0,5a+0,5b=0,15\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\\ \Rightarrow\%m_{Na}=\dfrac{23a}{8,5}.100\%0=\dfrac{23.0,2}{8,5}.100\%\approx54,12\%\\ \Rightarrow Chọn.A\)

Gọi hóa trị của M là n
\(n_{H_2}=\dfrac{0,2479}{24,79}=0,01\left(mol\right);n_{M\left(OH\right)_n}=0,5.0,04=0,02\left(mol\right)\)
PTHH: \(2M+2nH_2O\rightarrow2M\left(OH\right)_n+nH_2\)
\(\dfrac{0,02}{n}\)<--------------\(\dfrac{0,02}{n}\)<--------0,01
\(M_2O_n+nH_2O\rightarrow2M\left(OH\right)_n\)
Theo PTHH: \(n_{M\left(OH\right)_n}=2n_{M_2O_n}+n_M\)
=> \(n_{M_2O_n}=\dfrac{0,02-\dfrac{0,02}{n}}{2}=0,01-\dfrac{0,01}{n}\left(mol\right)\)
=> \(\dfrac{0,01}{n}< 0,01\Leftrightarrow n>1\)
Do M là kim loại tan trong nước nên n = 2
=> \(n_M=\dfrac{0,02}{2}=0,01\left(mol\right)\)
\(\xrightarrow[]{\text{BTNT M}}n_{MO}=n_{M\left(OH\right)_2}-n_M=0,02-0,01=0,01\left(mol\right)\)
=> \(0,01.\left(M_M+16\right)+0,01.M_M=2,9\)
=> \(M_M=137\left(g/mol\right)\)
=> M là Barium (Ba)
M : x mol ; M2On : y mol
⇒ n M(OH)n = x + 2y = 0,02
+) n = 1 (KL kiềm ) ⇒ x = 0,02 ; y = 0 ⇒ loại
+) n = 2 (KL kiềm thổ) ⇒ x = 0,01 , y = 0,005
⇒ mhh = 0,01.M + 0,005.(2M + 16.2) = 2,9
⇒ M = Ba

a. Công thức Lewis của CO2: 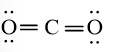
Công thức cấu tạo của CO2 là: O = C = O.
Công thức Lewis của NH3 là: 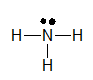
Công thức cấu tạo của NH3 là: \(H-N-H\)
\(|\)
H
b. Hợp chất tan trong nước: CO2 và NH3
Trong CO2CO2 chứa hai liên kết cộng hóa trị phân cực C=OC=O (đều phân cực về phía OO). Tuy nhiên, CO2CO2 có cấu trúc phân tử thẳng (O=C=OO=C=O) → 2 vectơ mô men cực cùng phương, ngược hướng triệt tiêu nhau → Phân tử CO2CO2 không phân cực nên có tan trong nước song là ít tan
+ NH3 tan tốt trong nước vì NH3 có liên kết cộng hóa trị phân cực trong phân tử

a, Y có số hiệu nguyên tử là 8 => Y là oxi
=> cấu hình electron là: \(1s^22s^22p^4\)
X có số hiệu nguyên tử là 11 => X là natri
=> cấu hình electron là: \(1s^22s^22p^63s^1\)
b.O + 2e → O2-
2Na \(\rightarrow\) 2Na\(^{1+}\)+2e
=> \(2Na^{1+}+O^{-2}\rightarrow Na_2O\)

Các nguyên tử khí hiếm đều có cấu hình electron lớp ngoài cùng đặc biệt bền vững: ns2np6ns2np6 (trừ heli có cấu hình 1s21s2). Các nguyên tử khí hiếm rất khó tham gia phản ứng hóa học. Trong tự nhiên, các khí hiếm đều tồn tại ở dạng nguyên tử (hay còn gọi là phân tử một nguyên tử) tự do (nên còn gọi là các khí trơ).
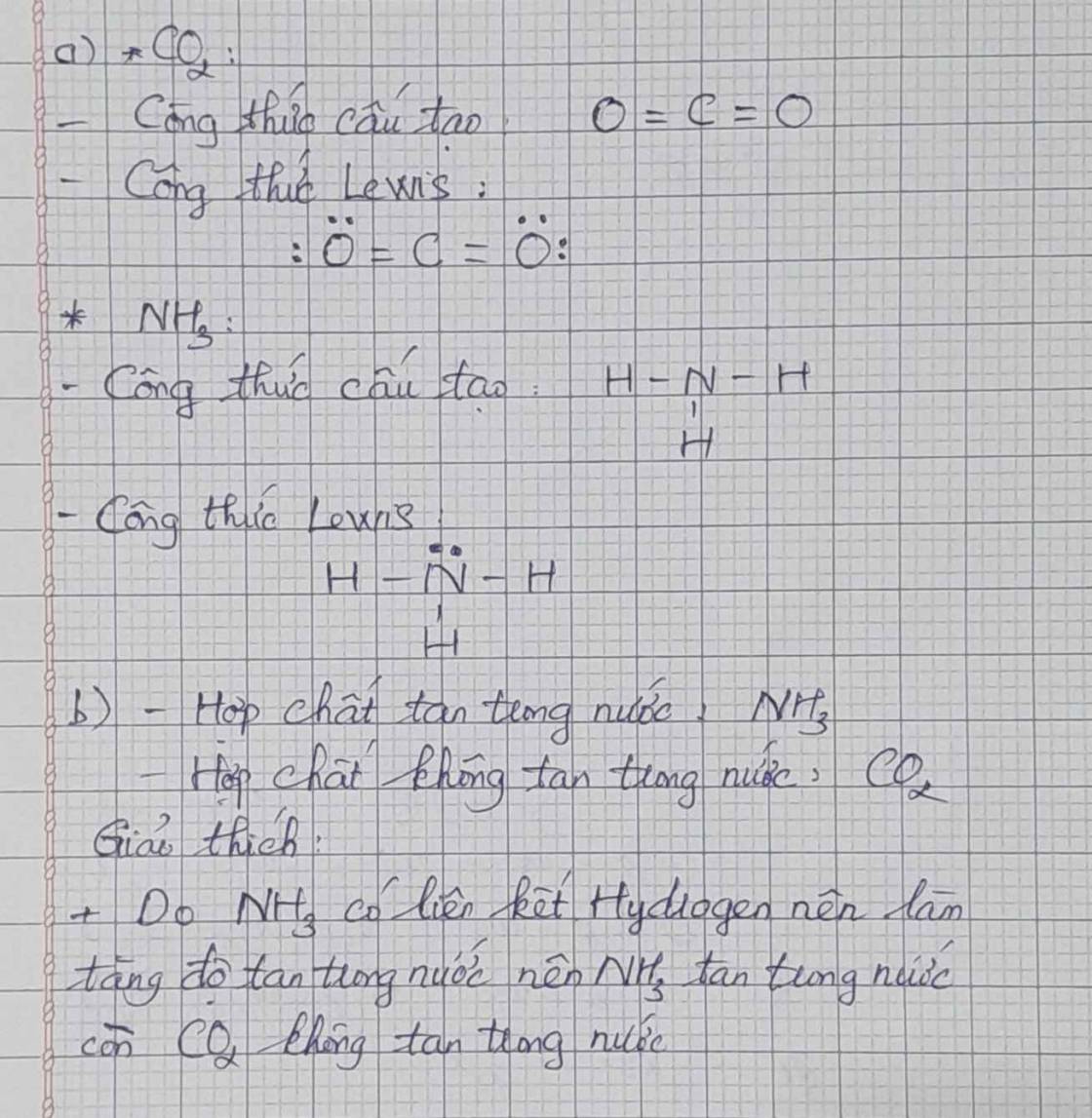
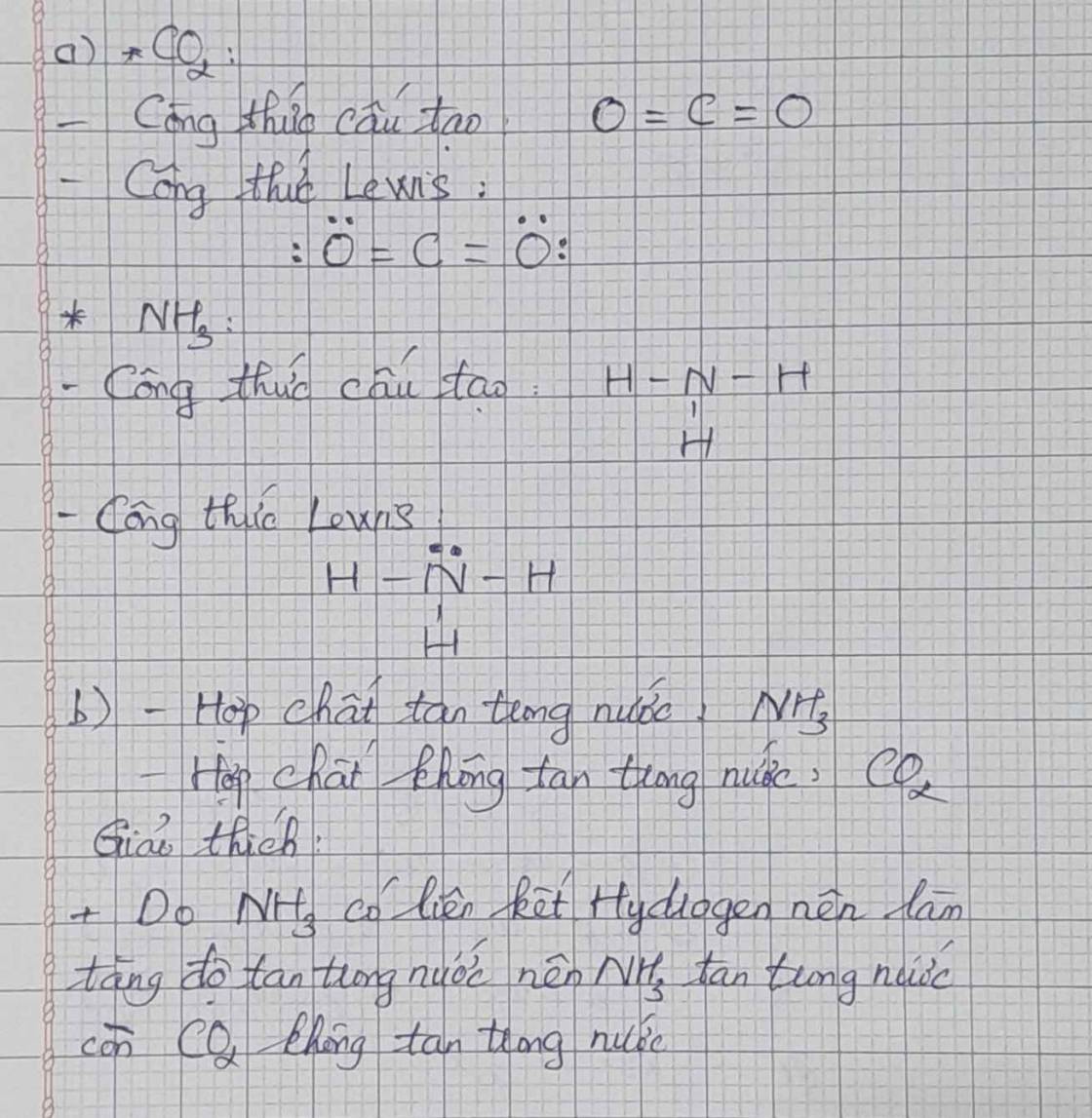

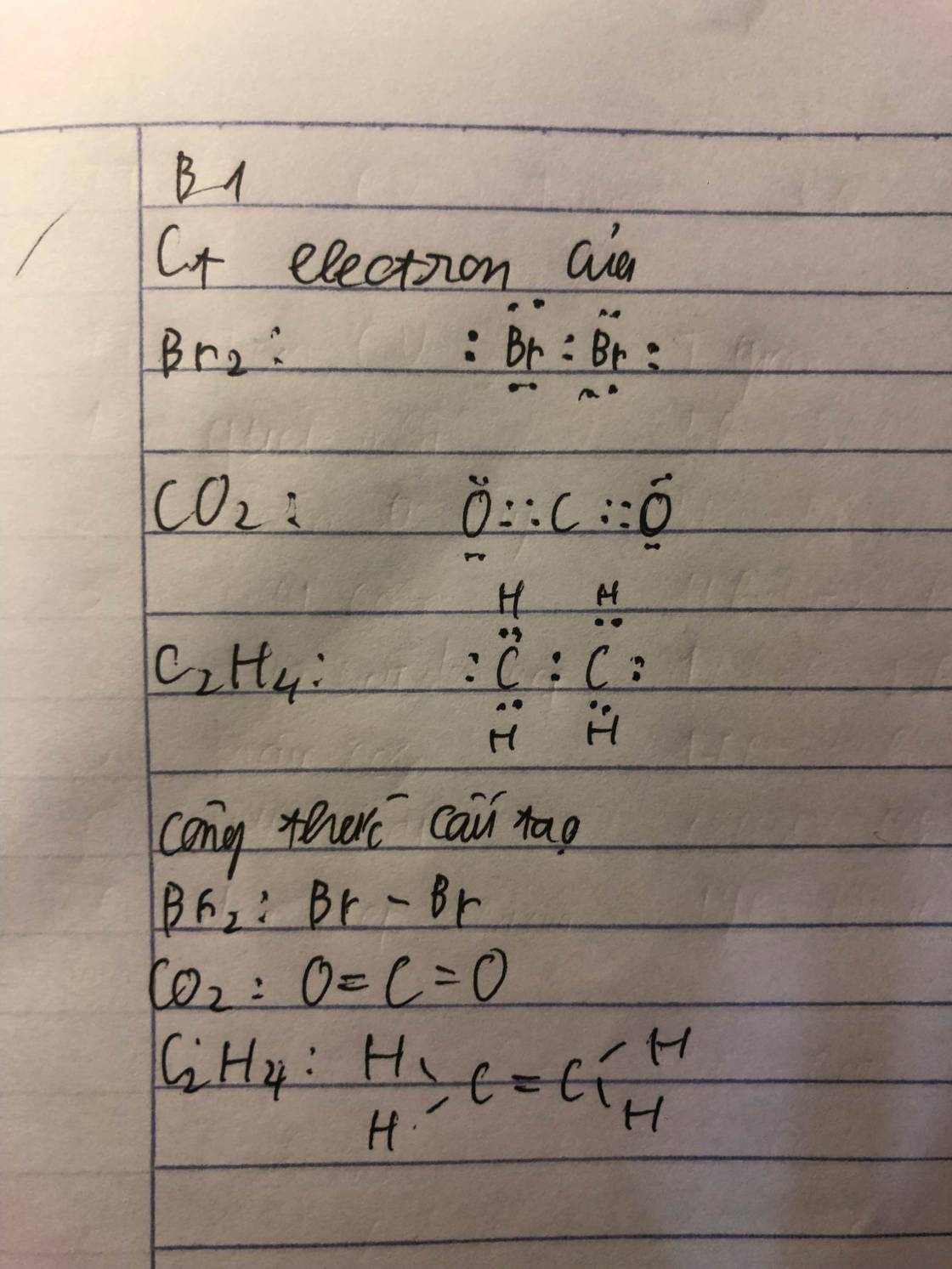


Ta có: \(\left\{{}\begin{matrix}p+e+n=58+2=60\\p=e\\p+e-n=20\end{matrix}\right.\Leftrightarrow p=e=n=\dfrac{60}{3}=20\)
=> X là Canxi
Cấu hình electron: \(1s^22s^22p^63s^23p^64s^2\)
=> Có 4 lớp e nên ở chu kì 4, lớp e cuối cùng có 2e nên ở nhóm IIA, vị trí số 20
a có: \left\{{}\begin{matrix}p+e+n=58+2=60\\p=e\\p+e-n=20\end{matrix}\right.\Leftrightarrow p=e=n=\dfrac{60}{3}=20⎩⎨⎧p+e+n=58+2=60p=ep+e−n=20⇔p=e=n=360=20
=> X là Canxi
Cấu hình electron: 1s^22s^22p^63s^23p^64s^21s22s22p63s23p64s2
=> Có 4 lớp e nên ở chu kì 4, lớp e cuối cùng có 2e nên ở nhóm IIA, vị trí số 20
Đúng(2)