Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Lý thuyết SVIP
A. AXIT PHOTPHORIC
I. CẤU TẠO PHÂN TỬ
Axit photphoric H3PO4 có công thức cấu tạo:
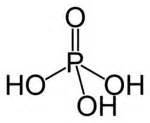

Trong hợp chất H3PO4, photpho có số oxi hóa cao nhất là +5.
II. TÍNH CHẤT VẬT LÍ
Axit photphoric là chất tinh thể, trong suốt, nóng chảy ở 42,5oC, rất háo nước nên dễ chảy rữa, tan tốt trong nước với bất kì tỉ lệ nào.
Axit photphoric thường dùng là dung dịch đặc, sánh, không màu, có nồng độ 85%.
III. TÍNH CHẤT HÓA HỌC
1. Axit H3PO4 là axit ba nấc, có độ mạnh trung bình, có tất cả những tính chất chung của axit. Trong dung dịch điện li yếu theo ba nấc (chủ yếu phân li theo nấc 1, nấc 2 kém hơn và nấc 3 rất yếu).
- Nấc 1: H3PO4 ⇌ H+ + H2PO4-
- Nấc 2: H2PO4- ⇌ H+ + HPO42-
- Nấc 3: HPO42- ⇌ H+ + PO43-
Trong dung dịch axit photphoric sẽ gồm (không kể sự phân li của H2O): H+, H2PO4-, HPO42-, PO43-, và các phân tử H3PO4 không phân li.
2. Khi tác dụng với dung dịch kiềm, tùy theo lượng chất tác dụng mà axit photphoric tạo ra muối axit, hoặc muối trung hòa, hoặc hỗn hợp các muối đó.
Ví dụ:
H3PO4 + NaOH → NaH2PO4 + H2O
H3PO4 + 2NaOH → Na2HPO4 + 2H2O
H3PO4 + 3NaOH → Na3PO4 + 3H2O
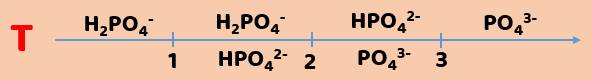
Để xác định cụ thể sản phẩm của phản ứng giữa axit photphoric và dung dịch kiềm, ta xét tỉ lệ T:
T = \(\dfrac{nOH^-}{nH_3PO_4}=\dfrac{nNaOH}{nH_3PO_4}\)
- T ≤ 1: Chỉ tạo muối của H2PO4-.
- 1 < T < 2: Tạo 2 muối của H2PO4- và HPO42-.
- T = 2: Chỉ tạo muối HPO42-.
- 2 < T < 3: Tạo 2 muối của HPO42- và PO43-.
- T ≥ 3: Chỉ tạo muối của PO43-.
3. Khác với axit nitric, axit photphoric không có tính oxi hóa.
IV. ĐIỀU CHẾ
1. Trong phòng thí nghiệm
Axit photphoric được điều chế bằng cách dùng HNO3 đặc oxi hóa photpho:
P + 5HNO3 đặc \(\underrightarrow{t^o}\) H3PO4 + 5NO2 + H2O
2. Trong công nghiệp
Có 2 phương pháp để điều chế axit photphoric trong công nghiệp.
Phương pháp 1: Cho axit sunfuric đặc tác dụng với quặng photphoric hoặc apatit:
Ca3(PO4)2 + 3H2SO4 (đặc) \(\underrightarrow{t^o}\) 3CaSO4 + 2H3PO4
Axit H3PO4 tạo thành được tách khỏi kết tủa CaSO4 bằng cách lọc, sau đó cô đặc. Axit H3PO4 sản xuất bằng phương pháp này thường không tính khiết nên để điều chế được H3PO4 có độ tinh khiết cao hơn người ta thực hiện theo phương pháp sau:
Phương pháp 2: Đốt cháy photpho để thu được P2O5, sau đó đem P2O5 thu được đi tác dụng với nước.
4P + 5O2 \(\underrightarrow{t^o}\) 2P2O5
P2O5 + 3H2O → 2H3PO4
V. ỨNG DỤNG
Một lượng lớn axit photphoric sản xuất ra được dùng để điều chế các muối photphat và để sản xuất phân lân, hợp chất cơ photpho (làm thuốc trừ sâu), H3PO4 tinh khiết được dùng trong công nghiệp dược phẩm.
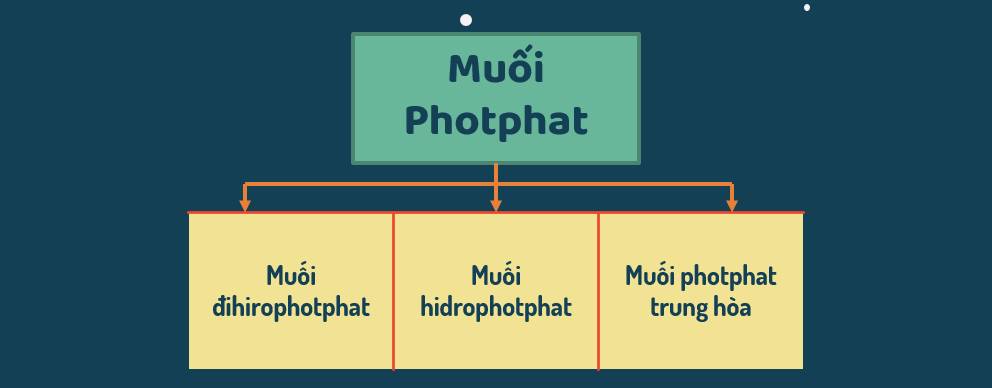
B. MUỐI PHOTPHAT
Khái niệm: Muối photphat là muối của axit photphoric.
Axit photphoric tác dụng với dung dịch kiềm tạo ra ba loại muối:
- Muối đihiđrophotphat: NaH2PO4, NH4H2PO4, Ba(H2PO4)2...
- Muối hiđrophotphat: K2HPO4, CaHPO4, Al2(HPO4)3,...
- Muối photphat trung hòa: Na3PO4, (NH4)3PO4, Ca3(PO4)2,...
I. TÍNH TAN
- Tất cả các muối đihiđrophotphat đều tan trong nước.
- Các muối trung hòa và muối hidrophotphat của kim loại natri, kali, amoni tan được trong nước, còn lại đều không tan hoặc ít tan trong nước.
II.NHẬN BIẾT ION PHOTPHAT
Thuốc thử để nhận biết ion PO43- trong dung dịch muối photphat là bạc nitrat. Ion Ag+ phân li ra từ AgNO3 trong dung dịch sẽ kết hợp với ion PO43- tạo thành kết tủa Ag3PO4 màu vàng. Kết tủa này không tan trong nước nhưng tan trong dung dịch axit nitric loãng.
3Ag+ + PO43- → Ag3PO4↓
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!

Bạn có thể đánh giá bài học này ở đây