Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Lý thuyết SVIP
I. KIẾN THỨC CẦN NHỚ
1. Ta nói là hiện tượng hóa học là hiện tượng khi có sự biến đổi từ chất này thành chất khác. Quá trình biến đổi của chất như thế được gọi là phản ứng hóa học.
Trong phản ứng hóa học chỉ diễn ra sự thay đổi liên kết giữa các nguyên tử làm cho phân tử biến đổi, kết quả là chất biến đổi. Còn số nguyên tử mỗi nguyên tố giữ nguyên trước và sau phản ứng.
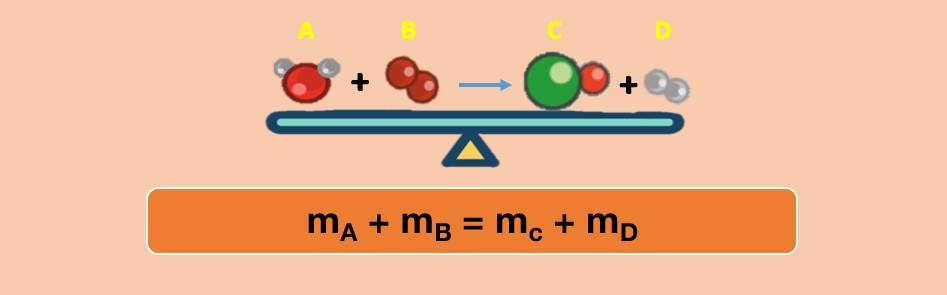
Dựa vào định luật bảo toàn khối lượng tính được khối lượng một chất khi biết khối lượng của các chất khác trong phản ứng.
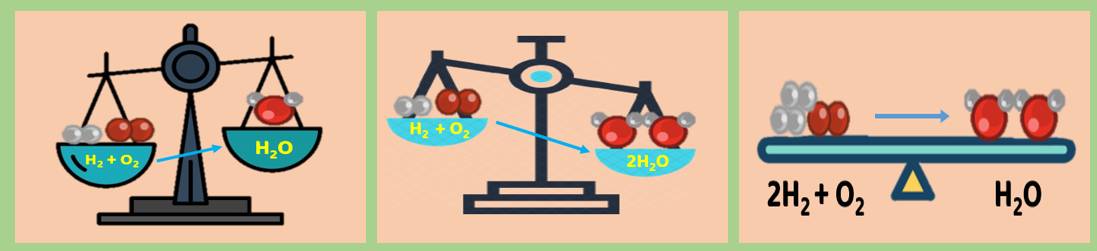
2. Phương trình hóa học gồm công thức hóa học của các chất trong phản ứng với hệ số thích hợp sao cho nguyên tử mỗi nguyên tố ở hai bên đều bằng nhau.
Để lập phương trình hóa học ta phải cân bằng số nguyên tử của mọi nguyên tố (và số nhóm nguyên tử nếu có).
Có 3 bước lập phương trình hóa học:
- Bước 1: Viết sơ đồ của phản ứng, gồm công thức hóa học của các chất phản ứng và sản phẩm.
- Bước 2: Cân bằng số nguyên tử mỗi nguyên tố, tìm hệ số thích hợp đặt trước các công thức hóa học của các chất sao cho số lượng các nguyên tử ở hai vế là bằng nhau.
- Bước 3: Viết phương trình hóa học.
Ví dụ: Lập phương trình hóa học của phản ứng có sơ đồ sau:
Al + HCl --➤ AlCl3 + H2
- Trước hết, ta làm chẵn số nguyên tử H ở bên trái.
Al + 2HCl --➤ AlCl3 + H2
- Bắt đầu cân bằng số nguyên tử Cl, bội số chung nhỏ nhất của 2 và 3 là 6, do đó:
Al + 6HCl --➤ AlCl3 + H2
- Tiếp đến, cân bằng số nguyên tử Al và H.
Al + 6HCl --➤ AlCl3 + 3H2
- Ta được phương trình hóa học hoàn chỉnh:
Al + 6HCl → AlCl3 + H2
Từ phương trình hóa học ta rút ra được tỉ lệ số nguyên tử, số phân tử giữa các chất trong phản ứng, tỉ lệ này bằng đúng tỉ lệ hệ số trước công thức hóa học mỗi chất.
II. BÀI TẬP
Bài 1. Lập phương trình hóa học cho các sơ đồ phản ứng sau:
a. KOH + H2SO4 --➤ K2SO4 + H2O
b. P + O2 --➤ P2O5
c. K + O2 --➤ K2O
d. Al + CuCl2 --➤ AlCl3 + Cu
Lời giải
a. 2KOH + H2SO4 → K2SO4 + 2H2O
b. 4P + 5O2 → 2P2O5
c. 4K + O2 → 2K2O
d. 2Al + 3CuCl2 → 2AlCl3 + 3Cu
Bài 2. Biết rằng kim loại nhôm tác dụng với axit sunfuric H2SO4 tạo ra khi hidro H2 và chất nhôm sunfat Al2(SO4)3.
a) Lập phương trình hóa học của phản ứng.
b) Cho biết tỉ lệ giữa sô nguyên tử Al lần lượt với số phân tử của ba chất trong phản ứng.
Lời giải
a) 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
b) Số nguyên tử Al: số phân tử H2SO4 = 2 : 3
Số nguyên tử Al: số phân tử Al2(SO4)3 = 2 :1
Số nguyên tử Al: số phân tử H2 = 2 : 3
Bài 3. Biết rằng khí hidro dễ tác dụng vơi chất chì (IV) oxit PbO2, chiếm lấy oxi của chất này để tạo ra nước.
a. Viết phương trình hóa học của phản ứng và gọi tên chất mới sinh ra.
b. Biết rằng 3g khí hidro tác dụng vừa đủ với 179,25 g PbO2, tạo ra 27 g nước. Tính khối lượng chất mới sinh ra.
Lời giải
a. Phương trình hóa học của phản ứng:
2H2 + PbO2 Pb + 2H2O
Chất sinh ra là kim loại Pb (chì)
b. Theo định luật bảo toàn khối lượng, ta có:
mPb = (mPbO2 + mH2) – mH2O = (179,25 + 3) – 27 = 155,25 (g)
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!

Bạn có thể đánh giá bài học này ở đây