Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:
CHÚC MỪNG
Bạn đã nhận được sao học tập

Chú ý:
Thành tích của bạn sẽ được cập nhật trên bảng xếp hạng sau 1 giờ!
Lý thuyết SVIP
00:00
I. KIẾN THỨC CẦN NẮM
1. Độ tan trong nước là gì? Những yếu tố nào ảnh hưởng tới độ tan?
- Độ tan của một chất trong nước (S) là số gam chất đó tan trong 100 gam nước để tạo thành dung dịch bão hòa ở nhiệt độ xác định.
- Yếu tố ảnh hướng đến độ tan của một chất trong nước là nhiệt độ (đối với chất khí tan trong nước còn phụ thuộc vào áp suất).
Ví dụ: SNaCl(25oC) = 36 g, có nghĩa là ở 25oC, trong 100 gam nước chỉ có thể hòa tan tối đa 36 gam NaCl để tạo ra dung dịch NaCl bão hòa.
@317831@@317832@
2. Nồng độ dung dịch cho biết những gì?
- Nồng độ phần trăm của dung dịch (C%) cho biết số gam chất tan có trong 100 g dung dịch:
.png)
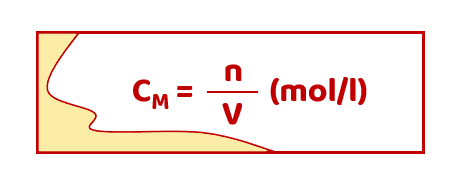
- Nồng độ mol của dung dịch (CM) cho biết số mol chất tan có trong 1 lít dung dịch:
@317833@@317834@
3. Cách pha chế dung dịch như thế nào?
Để pha chế một dung dịch theo nồng độ cho trước, ta thực hiện các bước sau:
| Bước 1 | Bước 2 |
Tính toán các đại lượng cần dùng | Pha chế dung dịch theo các đại lượng đã xác định.
|
Ví dụ: Pha chế 200 g dung dịch NaCl 20%.
Bước 1: Tìm các đại lượng liên quan.
- Khối lượng NaCl cần dùng là:
mNaCl = \(\dfrac{200.20}{100}\)= 40 gam.
- Khối lượng H2O cần dùng:
mH2O = mdd - mct = 200 - 40 = 160 gam.
Bước 2: Pha chế.
- Cân 40 g NaCl khan cho vào cốc.
- Cân 160 g H2O hoặc đong 160 ml nước cho dần dần vào cốc và khuấy cho đến khi NaCl tan hết, ta được 200 g dung dịch NaCl 20%.
@317835@
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!
OLMc◯2022


.jpg)
Bạn có thể đánh giá bài học này ở đây