Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 0 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Ethylic alcohol SVIP
1. Công thức phân tử, công thức cấu tạo của ethylic alcohol
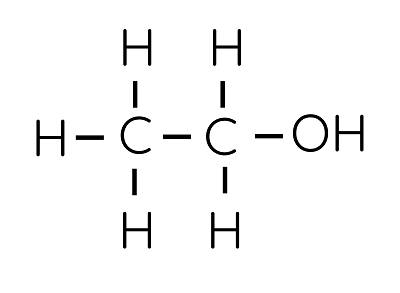
Ethylic alcohol (ethanol) là hợp chất hữu cơ có công thức phân tử C2H6O.
Trong phân tử ethylic alcohol có nhóm -OH, đây là nhóm nguyên tử gây nên tính chất đặc trưng của ethylic alcohol.
2. Tính chất vật lí của ethylic alcohol - độ cồn
Tìm hiểu về tính chất vật lí của ethylic alcohol
Ethylic alcohol là chất lỏng không màu, có mùi đặc trưng, vị cay, sôi ở 78,3 oC, có khối lượng riêng là 0,789 g/mL (ở 20 oC), tan vô hạn trong nước, hòa tan được nhiều chất như iodine, benzene,...
Tìm hiểu về độ cồn
Độ cồn (Xo hoặc X% vol) là số mililít ethylic alcohol nguyên chất có trong 100 mL dung dịch ở 20 oC.
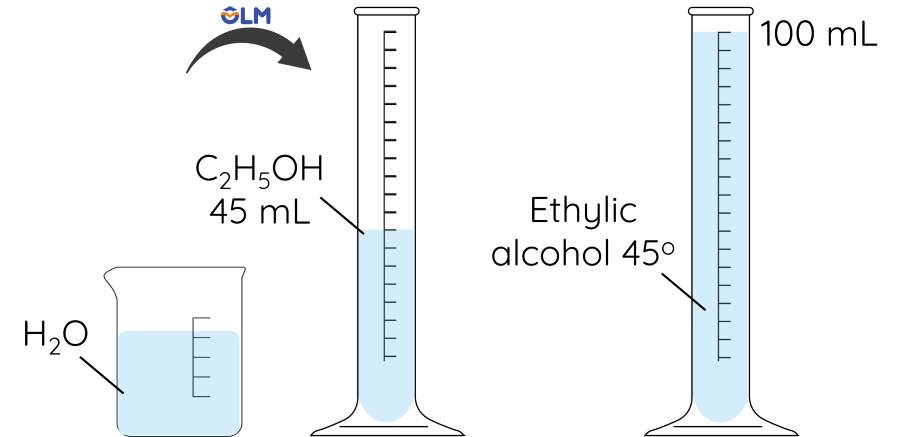
Ví dụ: Để có dung dịch ethylic alcohol 45o, ta thêm từ từ nước vào ống đong có chứa sẵn 45 mL ethylic alcohol nguyên chất cho đến khi được 100 mL dung dịch rồi khuấy đều.
3. Tính chất hóa học của ethylic alcohol
Thí nghiệm phản ứng cháy của ethylic alcohol
Thí nghiệm 1: Đốt cháy ethylic alcohol bằng oxygen trong không khí

Ethylic alcohol dễ cháy trong không khí tạo thành carbon dioxide, hơi nước và tỏa nhiều nhiệt.
C2H5OH + 3O2 \(\underrightarrow{t^o}\) 2CO2 + 3H2O
Thí nghiệm phản ứng của ethylic alcohol với sodium
Thí nghiệm 2: Ethylic alcohol phản ứng với sodium
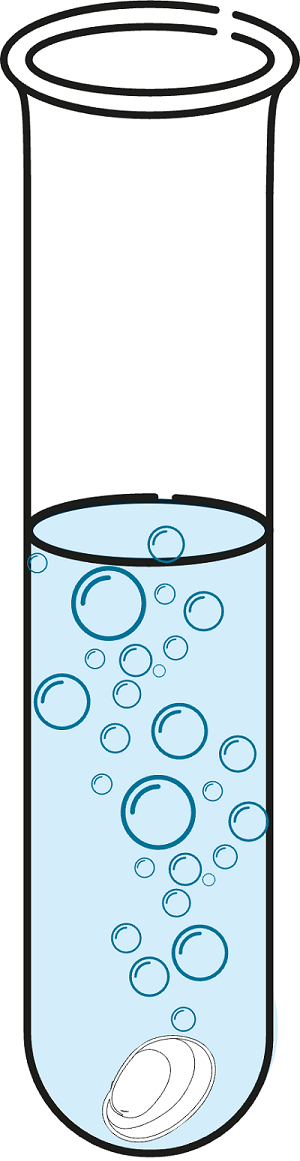
Các kim loại mạnh như Na, K thay thế được nguyên tử hydrogen trong nhóm - OH của ethylic alcohol, sản phẩm tạo thành có khí hydrogen.
2C2H5OH + 2Na → 2C2H5ONa + H2 ↑
4. Điều chế và ứng dụng của ethylic alcohol
Tìm hiểu phản ứng điều chế ethylic alcohol
Ethylic alcohol được điều chế bằng phương pháp lên men từ các nguyên liệu chứa tinh bột (gạo, ngô, sắn,...).
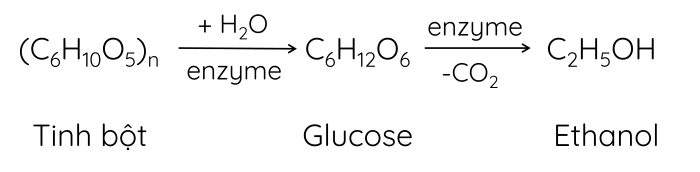
Ethylic alcohol còn được điều chế bằng phản ứng cộng nước vào ethylene.
CH2=CH2 + H2O \(\underrightarrow{t^o,H^+}\) C2H5OH
Tìm hiểu ứng dụng của ethylic alcohol
Ethylic alcohol có nhiều ứng dụng trong cuộc sống như: làm dung môi trong các ngành mĩ phẩm, dược phẩm,...; làm nhiên liệu để đun nấu hay chạy động cơ,...; làm nguyên liệu sản xuất giấm ăn, rượu bia,...

Tìm hiểu về tác hại của việc lạm dụng rượu, bia
Hiện nay, có nhiều loại đồ uống có cồn như rượu, bia, nước quả lên men,... Sử dụng quá nhiều đồ uống có cồn sẽ tăng nguy cơ bị viêm gan, viêm loét dạ dày, tăng huyết áp,... Việc lạm dụng rượu, bia là một trong các nguyên nhân gây tai nạn giao thông, tai nạn lao động, bạo lực trong các mối quan hệ gia đình và xã hội.
1. Ethylic alcohol có:
- Công thức phân tử C2H6O.
- Công thức cấu tạo thu gọn C2H5OH.
Đặc điểm công thức cấu tạo: Có chứa một nhóm -OH.
2. Ethylic alcohol là chất lỏng, không màu, sôi ở 78,3 oC, nhẹ hơn nước, tan vô hạn trong nước, hòa tan được một số chất như xăng, dầu hỏa,...
3. Độ cồn là số mililít ethylic alcohol nguyên chất có trong 100 mL, dung dịch ở 20 oC.
4. Tính chất hóa học của ethylic alcohol:
- Phản ứng tạo thành sản phẩm gồm khí carbon dioxide và nước, tỏa nhiều nhiệt.
- Phản ứng với sodium giải phóng khí hydrogen.
5. Ethylic alcohol được điều chế từ tinh bột hoặc ethylene.
6. Ethylic alcohol được sử dụng làm nguyên liệu, nhiên liệu, dung môi,...
7. Lạm dụng rượu, bia sẽ làm tổn hại đến sức khỏe, gây mất an toàn khi tham gia giao thông, gây mất trật tự xã hội.

Bạn có thể đánh giá bài học này ở đây