Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Điện phân SVIP
I. Hiện tượng điện phân
1. Khái niệm
- Điện phân là một quá trình oxi hóa – khử xảy ra tại các điện cực khi có dòng điện một chiều với hiệu điện thế đủ lớn đi qua chất điện li nóng chảy hoặc dung dịch chất điện li.
- Phản ứng oxi hóa – khử xảy ra trong quá trình điện phân là phản ứng không tự xảy ra mà phải nhờ tác động của điện năng.
- Chất tham gia vào quá trình điện phân có thể ở trạng thái nóng chảy (điện phân nóng chảy) hoặc dung dịch (điện phân dung dịch).
- Trong quá trình điện phân, dưới tác dụng của điện trường, các ion âm sẽ di chuyển về điện cực dương, các ion dương sẽ di chuyển về điện cực âm.
- Khi điện phân dung dịch, nước cũng có thể tham gia điện phân với vai trò chất khử (2H2O → O2 + 4H+ + 4e) hoặc chất oxi hóa (2H2O + 2e → H2 + 2OH-).
- Theo quy ước chung, đối với cả pin điện và bình điện phân, tại cathode xảy ra quá trình khử và tại anode xảy ra quá trình oxi hóa. Do vậy, trong điện phân cathode là cực âm, anode là cực dương.
Ví dụ: Quá trình điện phân NaCl nóng chảy được tiến hành như sau:
+ Bước 1: Nung NaCl trong bình đến nóng chảy, thu được chất lỏng có khả năng dẫn điện.
+ Bước 2: Nhúng hai điện cực than chì vào bình đựng NaCl nóng chảy rồi nối chúng với hai cực của nguồn điện một chiều (khoảng 7 V). Các ion di chuyển về các điện cực trái dấu, ở điện cực dương có khí Cl2 thoát ra và ở điện cực âm, Na được tạo thành.
2. Nguyên tắc (thứ tự) điện phân
- Khi bình điện phân chứa nhiều chất oxi hóa và chất khử, các quá trình xảy ra tại anode và cathode tuân theo thứ tự sau:
+ Tại anode: chất khử mạnh hơn bị oxi hóa trước.
+ Tại cathode: chất oxi hóa yếu mạnh hơn bị khử trước.
- Ở điều kiện chuẩn, độ mạnh yếu của các chất oxi hóa và chất khử được so sánh dựa vào giá trị thế điện cực chuẩn hoặc vị trí cặp oxi hóa – khử trong dãy điện hóa.
Ví dụ:
+ Thứ tự điện phân tại anode: I- > Br- > Cl- (các anion nhứ CO32-, NO3-, PO43-, SO42-, F- và ClO4- coi như không bị điện phân).
+ Thứ tự điện phân tại cathode: Au3+ > Ag+ > Hg2+ > Cu2+ > H+ > H2O
a) Điện phân dung dịch CuSO4 với các điện cực trơ (graphite)
- Thí nghiệm: Rót dung dịch CuSO4 0,5 M vào ống thủy tinh hình chữ U rồi nhúng hai điện cực than chì vào dung dịch. Nối hai điện cực than chì với hai cực của nguồn điện, tiến hành điện phân trong khoảng 5 phút. Trong quá trình điện phân, thấy có khí O2 thoát ra ở anode và kim loại Cu bám trên cathode.
- Giải thích thí nghiệm:
+ Ở anode có thể xảy ra sự oxi hóa ion SO42- hoặc phân tử H2O. Tuy nhiên, vì H2O dễ bị oxi hóa hơn SO42- nên H2O bị oxi hóa trước, tạo thành sản phẩm là khí O2.
2H2O → O2 + 4H+ + 4e
+ Ở cathode có thể xảy ra sự khử ion Cu2+ hoặc phân tử H2O. Vì ion Cu2+ dễ bị khử hơn H2O nên ion Cu2+ bị khử trước, tạo thành kim loại Cu bám trên cathode.
Cu2+ + 2e → Cu
- Sơ đồ điện phân:
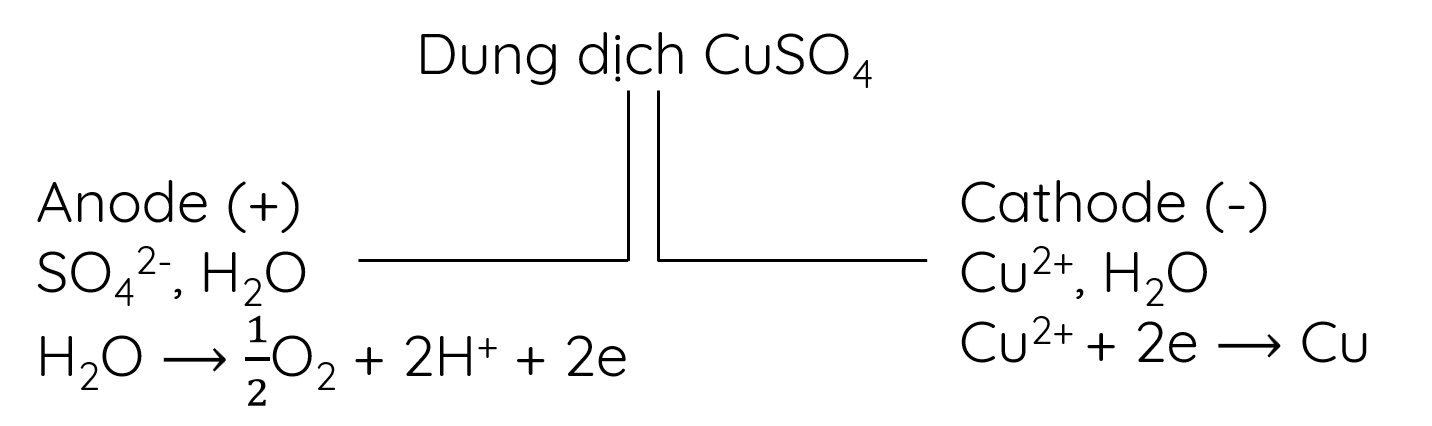
- Phương trình hóa học của quá trình điện phân:
CuSO4 + H2O → Cu + ½ O2 + H2SO4
b) Điện phân dung dịch NaCl với các điện cực trơ
II. Ứng dụng của phương pháp điện phân
1. Sản xuất kim loại
- Trong công nghiệp, một số kim loại trung bình và yếu được sản xuất bằng phương pháp điện phân dung dịch; các kim loại mạnh như Na, K, Mg, Ca, Al,... được sản xuất bằng phương pháp điện phân nóng chảy hợp chất ion của chúng.
+ Hơn 50% sản lượng kẽm trên thế giới được sản xuất bằng phương pháp điện phân:
ZnSO4 + H2O → Zn+ 1/2O2 + H2SO4
+ Trong công nghiệp, nhôm được sản xuất từ quặng bauxite theo hai giai đoạn chính:
-
Giai đoạn 1: Tinh chế quặng bauxite bằng phương pháp hóa học thu được Al2O3.
-
Giai đoạn 2: Điện phân Al2O3 nóng chảy. Do Al2O3 có nhiệt độ nóng chảy rất cao (2050oC) nên Al2O3 được trộn cùng với cryolite (Na3AlF6) để tạo thành hỗn hợp nóng chảy ở nhiệt độ gần 1000oC giúp tiết kiệm năng lượng, đồng thời tạo ra chất lỏng có tính dẫn điện tốt, nổi lên trên Al lỏng để năng cách Al lỏng với không khí.
Thùng điện phân có cathode là tấm than chì ở dưới đáy thùng, anode là những tấm than chì có thể di chuyển theo phương thẳng đứng.
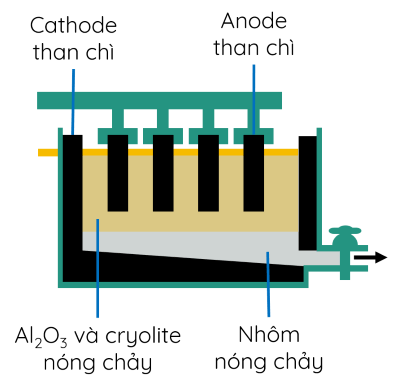
Khí O2 tạo thành ở nhiệt độ cao, đốt cháy dần điện cực anode than chì thành CO và CO2. Do vậy, trong quá trình điện phân phải hạ thấp dần các điện cực anode vào thùng điện phân.
2. Tinh chế kim loại
- Từ nguồn kim loại thô (kim loại phế liệu hoặc sau quá trình nhiệt luyện, thủy luyện), các kim loại như Zn, Ni, Co, Cu, Ag, Au,... được tinh chế bằng phương pháp điện phân.
- Quá trình tinh chế được thực hiện bằng cách điện phân dung dịch chất tan của kim loại đó với anode làm bằng kim loại thô tương ứng.
Ví dụ: Trong công nghiệp, đồng phế liệu hoặc đồng thô được tinh chế bằng phương pháp điện phân. Bình điện phân tinh chế đồng chức dung dịch muối CuSO4 trong dung dịch H2SO4, anode bằng đồng thô và cathode là đồng tinh khiết.
Tại anode: Cu bị oxi hóa thành ion Cu2+ đi vào dung dịch
Cu → Cu2+ + 2e
Tại cathode: Cu2+ bị thử thành Cu bám trên cathode:
Cu2+ + 2e → Cu
Quá trình điện phân này được coi như là sự chuyển dời kim loại Cu từ anode về cathode. Kết thúc quá trình điện phân thu được đồng tinh khiết ở cathode.
3. Mạ điện
- Phương pháp điện phân được sử dụng trong mạ điện, trong đó ion kim loại bị khử, tạo thành lớp kim loại rắn bao phủ trên bề mặt kim loại cần mạ nhằm trang trí bề mặt hoặc chống sự ăn mòn.
- Trong kĩ thuật mạ điện, các kim loại mạ thường là chromium, nickel, đồng, vàng, bạc, platinum,...
- Bình mạ điện chứa dung dịch muối của kim loại mạ, vật cần mạ và thanh kim loại mạ.
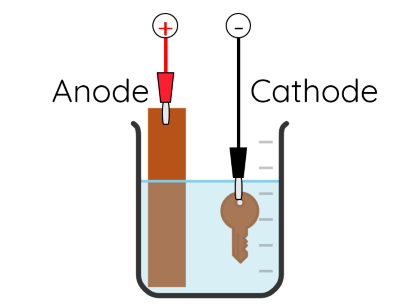
Ví dụ: Quá trình điện phân để mạ đồng lên một chiếc chìa khóa được mô tả trong hình sau.
Trong quá trình điện phân, thanh kim loại đóng vai trò là anode, chiếc chìa khóa đóng vai trò là cathode và dung dịch điện phân là dung dịch CuSO4. Các quá trình xảy ra ở các điện cực tương tự như quá trình điện phân tinh chế đồng với anode tan. Độ dày của lớp mạ tỉ lệ thuận với cường độ dòng điện chạy qua dung dịch điện phân và thời gian mạ.
1. Thứ tự điện phân:
- Tại anode: chất khử mạnh hơn bị oxi hóa trước.
- Tại cathode: chất oxi hóa yếu mạnh hơn bị khử trước.
2. Trong thực tiễn, phương pháp điệ phân được sử dụng để sản xuất kim loại, tinh chế kim loại, mạ điện.
3. Trong công nghiệp, nhôm được sản xuất bằng cách điện phân aluminium oxide nóng chảy.
4. Quá trình tinh chế đồng được thực hiện bằng phương pháp điện phân với anode bằng đồng thô.

Bạn có thể đánh giá bài học này ở đây