Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Đề thi minh họa Tốt nghiệp THPT môn Hóa học từ năm 2025 SVIP
Yêu cầu đăng nhập!
Bạn chưa đăng nhập. Hãy đăng nhập để làm bài thi tại đây!
Nguyên tử gồm hạt nhân và vỏ nguyên tử. Vỏ nguyên tử chứa loại hạt nào sau đây?
Các nguyên tử của cùng một nguyên tố hóa học là đồng vị của nhau có sự khác nhau về
Kí hiệu phân lớp electron nào sau đây sai?
Hình sau biểu diễn hình dạng orbital nguyên tử (AO) nào dưới đây?

Cấu hình electron của nguyên tử Al (Z = 13) là
Phân tử nào sau đây có liên kết cộng hóa trị không phân cực?
Biết số hiệu nguyên tử của hai nguyên tố X và Y lần lượt là 19 và 17. Cho các phát biểu sau:
(a) Độ âm điện của X nhỏ hơn độ âm điện của Y.
(b) Số electron độc thân của X nhỏ hơn số electron độc thân của Y.
(c) Trong các phản ứng hóa học, nguyên tử X có xu hướng nhường 2 electron.
(d) Khi hình thành liên kết với nguyên tử X, nguyên tử Y nhận 1 electron.
Số phát biểu đúng là
Chất nào sau đây không tạo được liên kết hydrogen giữa các phân tử?
Lưu huỳnh (sulfur, S) thuộc nhóm VIA trong bảng tuần hoàn các nguyên tố hóa học. Công thức của sulfuric acid (tương ứng với oxide cao nhất của S) là
Cho bảng số lượng electron, neutron, proton của các phần tử (nguyên tử hoặc ion) sau:
| Phần tử | Số electron | Số neutron | Số proton |
| (a) | 8 | 8 | 8 |
| (b) | 10 | 12 | 11 |
| (c) | 19 | 20 | 19 |
| (d) | 18 | 18 | 17 |
Những phần tử thuộc loại ion là
Số đồng vị bền của nguyên tố neon (Ne) được suy ra từ phổ khối lượng ở hình sau là
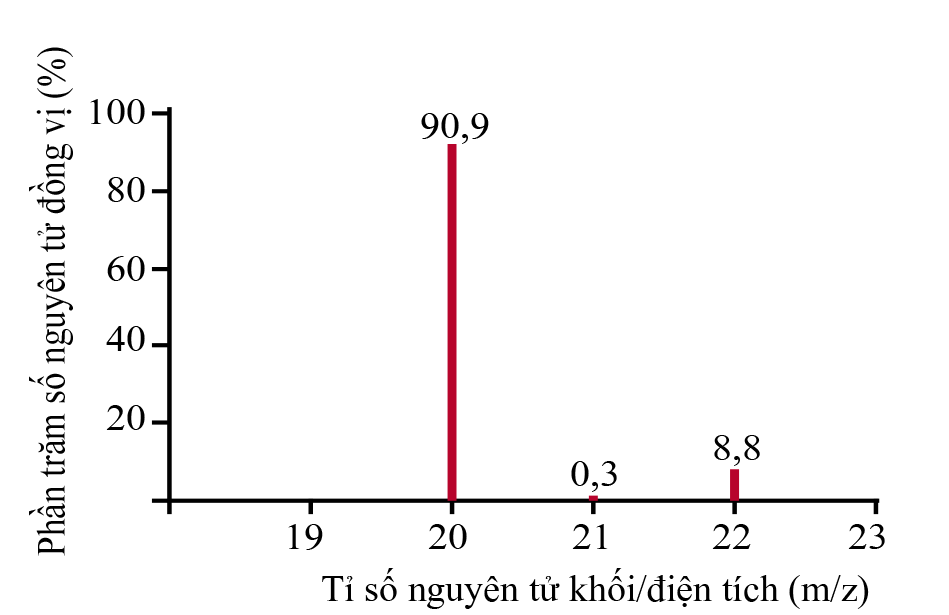
Trong bảng tuần hoàn các nguyên tố hóa học, các nguyên tố khí hiếm thuộc nhóm
Trong phân tử carbon dioxide (O=C=O), số liên kết σ và liên kết π lần lượt là
Trong một chu kì của bảng tuần hoàn các nguyên tố hóa học, theo chiều tăng dần điện tích hạt nhân, bán kính nguyên tử của các nguyên tố giảm dần do số lớp electron ...(I), lực hút giữa hạt nhân với electron lớp ngoài cùng ...(II). Cụm từ cần điền vào (I), (II) lần lượt là
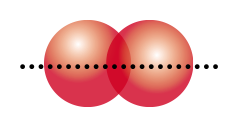
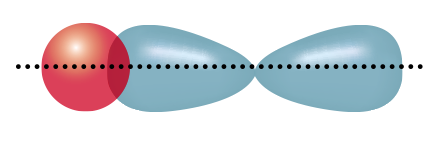
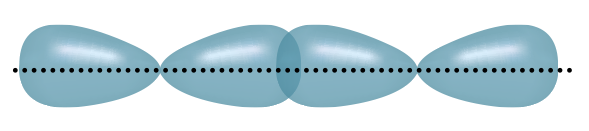
Cho các hình biểu diễn sự xen phủ orbital nguyên tử để tạo liên kết hóa học sau:
 |
 |
 |
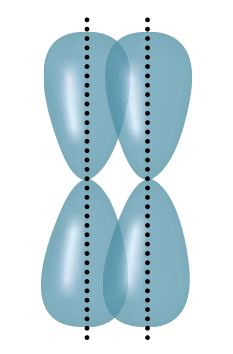 |
| (a) Xen phủ trục s-s | (b) Xen phủ trục s-p | (c) Xen phủ trục p-p | (d) Xen phủ bên p-p |
Biết số hiệu các nguyên tử H, F và S lần lượt là 1, 9 và 16. Sự tạo liên kết trong các phân tử H2S và F2 theo kiểu xen phủ tương ứng là
Cho số hiệu nguyên tử nguyên tố R là 7. Phát biểu nào sau đây sai?
Nguyên tố silicon (Si) thuộc chu kì 3, nhóm IVA trong bảng tuần hoàn các nguyên tố hóa học. Công thức oxide cao nhất của silicon là
Cho bảng số liệu sau:
| Chất | Nước (H2O) | Hydrogen sulfide (H2S) |
| Nhiệt độ sôi (oC) ở 1 atm | 100,0 | - 60,7 |
Phát biểu nào sau đây sai?
Chọn đúng hoặc sai.
Trong lịch sử các thuyết về về mô hình nguyên tử, có mô hình hành tinh nguyên tử (mô hình Rutherford - Bohr) và mô hình hiện đại của nguyên tử.
 |
 |
| Mô hình (1) của nguyên tử hydrogen | Mô hình (2) của nguyên tử hydrogen |
| Theo mô hình (1), electron chuyển động trên quỹ đạo xác định xung quanh hạt nhân. |
|
| Với nguyên tử hydrogen, mô hình (1) là mô hình hiện đại, mô hình (2) là mô hình hành tinh nguyên tử. |
|
| Khái niệm về orbital nguyên tử xuất phát từ mô hình hiện đại của nguyên tử. |
|
| Khái niệm về xác suất tìm thấy electron xuất phát từ mô hình hành tinh nguyên tử. |
|
Chọn đúng hoặc sai.
Natri (sodium, 11Na) và magnesium (12Mg) thuộc chu kì 3 trong bảng tuần hoàn các nguyên tố hóa học.
(Nhấp vào dòng để chọn đúng / sai)| Khi phản ứng với Cl2, Na và Mg đều tạo ra hợp chất ion. |
|
| Tính base của sodium hydroxide yếu hơn tính base của magnesium hydroxide. |
|
| Theo xu hướng biến đổi tính kim loại, Mg có tính kim loại yếu hơn Na. |
|
| Dựa vào mức độ phản ứng của Na và Mg với nước ở điều kiện thường, có thể so sánh được độ hoạt động hóa học giữa Na với Mg. |
|
Chọn đúng hoặc sai.
Khi đun nóng dung dịch sodium chloride bão hòa, thu được tinh thể sodium chloride khan. Sau đó, nung nóng đến khoảng 800oC thì tinh thể sodium chloride chảy lỏng.
(Nhấp vào dòng để chọn đúng / sai)| Quá trình hình thành tinh thể sodium chloride ở trên được gọi là sự kết tinh. |
|
| Tinh thể sodium chloride nóng chảy ở khoảng 800oC, chứng tỏ lực liên kết giữa các ion trong tinh thể là yếu. |
|
| Trong tinh thể sodium chloride, xung quanh 1 ion Na+ có 6 ion Cl- gần nhất. |
|
| Quá trình hình thành tinh thể sodium chloride ở trên là quá trình sắp xếp lại các ion Na+, Cl- từ chuyển động tự do thành cấu trúc có trật tự trong tinh thể. |
|
.png)
Chọn đúng hoặc sai.
Các nguyên tố phổ biến thuộc nhóm halogen (VIIA) trong bảng tuần hoàn các nguyên tố hóa học gồm: F (Z=9), Cl (Z=17), Br (Z=35) và I (Z=53). Đơn chất halogen tồn tại dạng phân tử X2, giữa các phân tử X2 thường có tương tác với nhau. Cho giá trị năng lượng liên kết X - X ở bảng sau:
| Liên kết | F - F | Cl - Cl | Br - Br | I - I |
| Năng lượng liên kết (kJ.mol-1) ở 25oC và 1 bar | 159 | 243 | 193 | 151 |
Năng lượng liên kết X - X càng lớn thì liên kết càng bền.
(Nhấp vào dòng để chọn đúng / sai)| Liên kết giữa các nguyên tử trong X2 là liên kết cộng hóa trị không phân cực. |
|
| Năng lượng liên kết Cl - Cl lớn nhất trong dãy trên vì Cl có bán kính nguyên tử nhỏ nhất. |
|
| Tương tác giữa các phân tử X2 là tương tác van der Waals. |
|
| Cấu hình electron lớp ngoài cùng của nguyên tử X có dạng ns2np5. |
|
Cho 6 nguyên tố có số hiệu nguyên tử lần lượt là 10, 13, 16, 18, 19 và 20. Trong số các nguyên tố trên, có bao nhiêu nguyên tố kim loại?
Trả lời: .
Nguyên tố Y thuộc chu kì 3 trong bảng tuần hoàn các nguyên tố hóa học. Công thức oxide cao nhất của Y là Y2O5. Khi cho 1 mol Y2O5 tác dụng với NaOH dư thì số mol NaOH phản ứng là bao nhiêu?
Trả lời: .
Có bao nhiêu hợp chất ion trong dãy các chất sau: NH3, CaO, KCl, CH4, NaOH.
Trả lời: .
Cho số hiệu của nguyên tố N và O lần lượt là 7 và 8. Biết rằng hóa trị của nguyên tố N trong phân tử HNO3 bằng tổng số liên kết σ và liên kết π mà nguyên tử N tạo thành khi liên kết với các nguyên tử xung quanh. Trong phân tử HNO3, nguyên tử N không liên kết với nguyên tử H mà liên kết với ba nguyên tử O. Từ đó, viết được công thức Lewis phù hợp của phân tử HNO3 với hóa trị của N là n. Giá trị của n là bao nhiêu?
Trả lời: .
Tổng số cặp electron dùng chung giữa các nguyên tử trong phân tử acetylene (C2H2) là bao nhiêu?
Trả lời: .
Từ phổ khối lượng (MS) của magnesium (Mg) ở hình dưới đây:
.png)
hãy cho biết giá trị nguyên tử khối trung bình của magnesium là bao nhiêu? Biết z = 1. (Làm tròn kết quả đến hàng phần mười).
Trả lời: .
