Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Dãy hoạt động hóa học SVIP
I. Xây dựng dãy hoạt động hóa học
Dựa vào khả năng và mức độ phản ứng của các kim loại với một số chất có thể so sánh được mức độ hoạt động hóa học của chúng với nhau.
Thí nghiệm 1: Cho khoảng 2 - 3 mL dung dịch AgNO3 vào ống nghiệm chứa dây đồng.
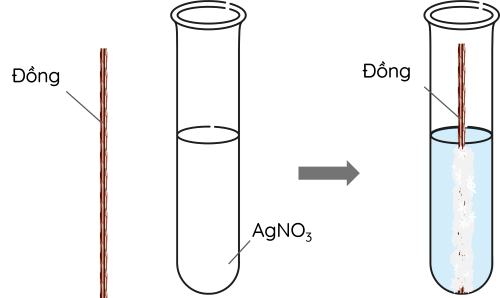
Thí nghiệm 2: Cho đinh sắt vào ống nghiệm chứa dung dịch HCl (1), dây đồng vào ống nghiệm chứa HCl (2), mẩu magnesium vào ống nghiệm chứa HCl (3).
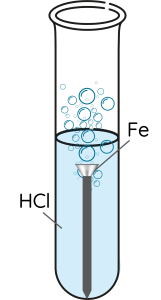
|
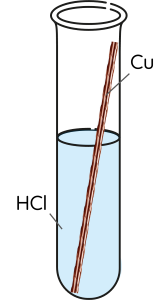
|

|
Thí nghiệm 3: Cho mẩu sodium vào chậu thủy tinh đựng nước có chứa vài giọt phenolphthalein (1), cho mẩu magnesium vào chậu thủy tinh đựng nước có chứa vài giọt phenolphthalein (2).

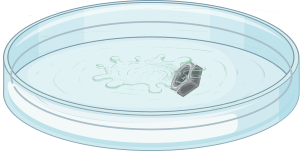
Dãy hoạt động hóa học:
K, Na, Ca, Mg, Al, Zn, Fe, Pb, H, Cu, Ag, Au
II. Ý nghĩa của dãy hoạt động hóa học
- Từ trái sang phải, mức độ hoạt động hóa học giảm dần.
- Các kim loại đứng trước Mg phản ứng mạnh với nước ở điều kiện thường tạo thành dung dịch kiềm và khí hydrogen.
- Kim loại đứng trước H có thể tác dụng với dung dịch acid, giải phóng khí hydrogen.
- Kim loại đứng trước (trừ K, Na, Ca,...) có thể đẩy kim loại đứng sau ra khỏi muối của nó.
Bằng các thí nghiệm khác nhau, người ta xây dựng được dãy hoạt động hóa học như sau:
K, Na, Ca, Mg, Al, Zn, Fe, Pb, H, Cu, Ag, Au

Bạn có thể đánh giá bài học này ở đây