Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Cấu trúc hạt nhân SVIP
I. THÍ NGHIỆM TÁN XẠ HẠT ALPHA
Mô hình nguyên tử đầu tiên giống như một chiếc bánh ngọt có mận khô bên trong: các mẩu mận khô biểu diễn các electron mang điện tích âm, phần còn lại của bánh biểu diễn phần còn lại của nguyên tử mang điện tích dương.

Thí nghiệm Rutherford - khám phá cấu tạo nguyên tử vàng
Trong thí nghiệm này, Rutherford sử dụng chùm hạt alpha mang điện tích dương (kí hiệu α, chính là hạt nhân nguyên tử He).
Chùm hạt này được phát ra từ nguồn R bắn vào lá vàng D rất mỏng (độ dày chỉ khoảng 4.10-7 m được đặt trong hộp chân không G. Ông sử dụng kính hiển vi M để quan sát các đốm sáng phát ra khi hạt này đập vào kính S có phủ chất huỳnh quang.
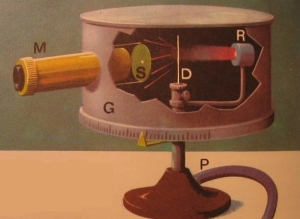
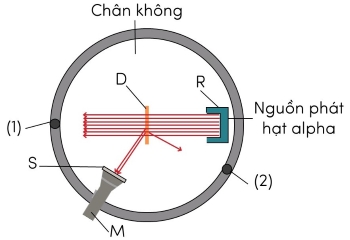
Khi di chuyển kính hiển vi từ vị trí (1) đến vị trí (2), tần suất đốm sáng xuất hiện trên màn S giảm đi rất nhanh. Tại vị trí (2) vẫn thấy xuất hiện các đốm sáng nhưng tần suất ít hơn so với vị trí (1) cỡ 104 lần.
Kết quả
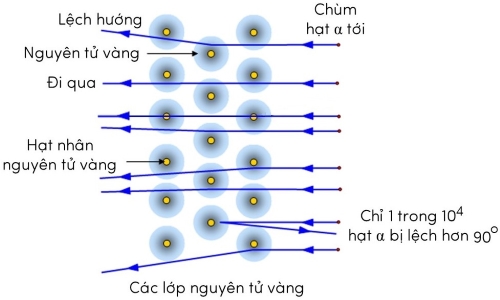
Hiện tượng lệch hướng chuyển động của hạt alpha khi đến gần hạt nhân vàng gọi là hiện tượng tán xạ hạt alpha.
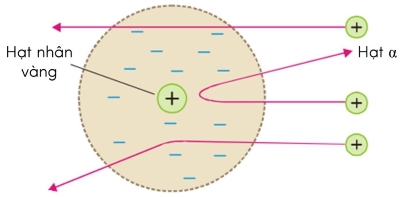
II. NUCLEON VÀ KÍ HIỆU HẠT NHÂN
1. Nucleon
Hạt nhân được tạo thành bởi hai loại hạt là proton và neutron, hai loại hạt này có tên chung là nucleon.
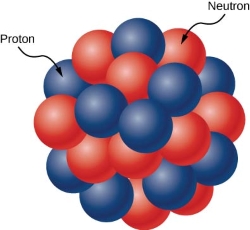
- Proton (kí hiệu p), có khối lượng mp \(\approx\) 1,67262.10-27 kg, điện tích là q = +e \(\approx\) 1,6.10-19 C.
- Neutron (kí hiệu n), có khối lượng mn \(\approx\) 1,67493.10-27 kg, trung hòa về điện.
Khối lượng nguyên tử bằng tổng khối lượng hạt nhân và electron có trong nguyên tử. Hạt nhân có khối lượng rất lớn so với khối lượng của các electron, vì vậy khối lượng nguyên tử gần như tập trung toàn bộ ở hạt nhân.
Chú ý: Để thuận lợi tính toán khối lượng của hạt nhân, người ta định nghĩa một đơn vị mới gọi là đơn vị khối lượng nguyên tử, kí hiệu là amu. Đơn vị amu có giá trị bằng $\dfrac{1}{12}$ khối lượng nguyên tử của đồng vị carbon-12:
1 amu \(\approx\) 1,66054.10-27 kg
Số proton trong hạt nhân bằng Z. Tổng số nucleon trong một hạt nhân được kí hiệu là A; A gọi là số khối.
Có thể coi hạt nhân nguyên tử như một quả cầu bán kính $R$; $R$ phụ thuộc vào tổng số hạt nucleon $A$ theo công thức gần đúng:
$R=1,2.10^{-15}.A^{\frac{1}{3}}$ (m)
| Tên nguyên tố | Số khối |
Bán kính nguyên tử 10-10 m |
Bán kính hạt nhân 10-15 m |
| Hydrogen | 1 | 1,2 | 0,9 |
| Helium | 4 | 1,4 | 1,7 |
| Oxigen | 16 | 1,5 | 2,7 |
| Silicon | 28 | 2,1 | 3,1 |
| Sắt | 56 | 1,9 | 3,7 |
| Cadimium | 114 | 1,6 | 4,6 |
| Vàng | 197 | 1,7 | 5,4 |
| Uranium | 238 | 1,9 | 5,9 |
2. Kí hiệu hạt nhân
Người ta dùng kí hiệu hóa học X của nguyên tố để kí hiệu cho hạt nhân, kèm theo hai số Z và A như sau: \(_Z^AX.\)
Ví dụ: hạt nhân carbon có 12 nucleon trong đó có 6 proton được kí hiệu \(_6^{12}C\).
3. Đồng vị
Các hạt nhân đồng vị là những hạt nhân có cùng số Z, khác số A, nghĩa là cùng số proton và khác số neutron.
Các đồng vị được chia làm hai loại: đồng vị bền và đồng vị phóng xạ (không bền). Hầu hết các mẫu chất trong tự nhiên đều là hỗn hợp của nhiều đồng vị.
Ví dụ: Carbon có ba đồng vị chính là \(_6^{12}C,\) \(_6^{13}C,\) \(_6^{14}C\). Trong đó đồng vị \(_6^{12}C\) và \(_6^{13}C\) là đồng vị bền chiếm hơn 99 % carbon tự nhiên.
1. Hạt nhân mang điện tích dương, có khối lượng gần bằng khối lượng nguyên tử chứa nó nhưng kích thước nhỏ hơn kích thước nguyên tử cỡ 104 lần.
2. Đơn vị khối lượng nguyên tử kí hiệu là amu; 1 amu có giá trị bằng \(\dfrac{1}{12}\) khối lượng nguyên tử của đồng vị \(_6^{12}C\); 1 amu \(\approx\) 1,66054.10-27 kg.
3. Hạt nhân nguyên tử được tạo thành bởi các hạt nucleon. Có hai loại nucleon là proton mang điện tích +1e và neutron trung hòa về điện. Các nucleon có khối lượng xấp xỉ bằng 1 amu.
4. Kí hiệu hạt nhân \(_Z^AX\), trong đó X, A, Z lần lượt là kí hiệu hóa học nguyên tố, số khối và số hiệu nguyên tử.
Bạn có thể đăng câu hỏi về bài học này ở đây
