Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Amine SVIP
I. Khái niệm, phân loại, đồng phân và danh pháp
1. Khái niệm
Amine là dẫn xuất của ammonia, trong đó nguyên tử hydrogen trong phân tử ammonia được thay thế bằng gốc hydrocarbon.
Ví dụ:
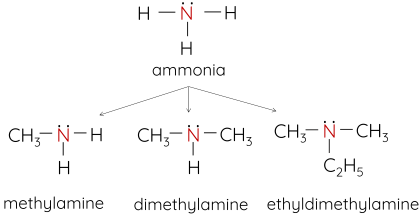
2. Phân loại
Amine thường được phân loại theo bậc của amine và bản chất gốc hydrocarbon.
- Bậc của amine được tính bằng số gốc hydrocarbon liên kết trực tiếp với nguyên tử nitrogen. Theo đó, amine được phân loại thành amine bậc một, amine bậc hai và amine bậc ba.

|
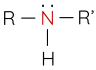
|

|
- Dựa trên đặc điểm cấu tạo của gốc hydrocarbon, amine được phân thành nhiều loại, trong đó hai loại điển hình là alkylamine (nhóm amine liên kết với gốc alkyl) và arylamine (nhóm amine liên kết trực tiếp với nguyên tử carbon của vòng benzene).
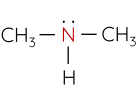
|
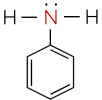
|
3. Đồng phân
Các amine có từ hai nguyên tử carbon trong phân tử bắt đầu xuất hiện đồng phân. Amine có thể có các đồng phân:
- Bậc amine.
- Mạch carbon.
- Vị trí nhóm amine.
4. Danh pháp
Tên của amine theo danh pháp gốc - chức:
![]()
Tên của amine theo danh pháp thay thế:
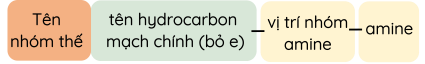
Ví dụ: CH3CH(NH2)-CH3 có tên gốc - chức là isopropylamine và tên thay thế là propan-2-amine.
@203193870847@
II. Đặc điểm cấu tạo
Trong phân tử amine, nguyên tử nitrogen còn cặp electron chưa liên kết. Cấu tạo của amine tương tự ammonia nên amine có một số tính chất hóa học tương tự ammonia.
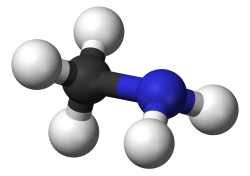
Aniline còn dễ tham gia phản ứng thế nguyên tử hydrogen trong nhân thơm do ảnh hưởng của nhóm –NH2.
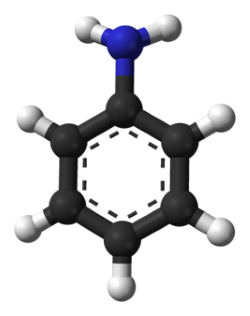
III. Tính chất vật lí
|
Amine |
Tên gọi | Nhiệt độ nóng chảy (oC) | Nhiệt độ sôi (oC) |
|
CH3NH2 |
Methylamine | -93,4 |
-6,4 |
|
CH3CH2NH2 |
Ethylamine |
-81,0 |
16,6 |
|
CH3NHCH3 |
Dimethylamine |
-93,0 |
7,3 |
|
CH3CH2CH2NH2 |
Propylamine |
-84,8 |
47,2 |
|
CH3CH(NH2)CH3 |
Isopropylamine |
-95,1 |
31,8 |
|
(CH3)3N |
Trimethylamine |
-117,1 |
2,8 |
|
C6H5NH2 |
Aniline |
-6,0 |
184,1 |
Amine có nhiệt độ sôi cao hơn hydrocarbon có cùng số nguyên tử carbon hoặc có phân tử khối tương đương.
Methylamine, ethylamine, dimethylamine và trimethylamine là những chất khí, có mùi tanh của cá hoặc mùi khai tương tự ammonia.
Các amine có số nguyên tử carbon nhỏ thường tan tốt trong nước nhờ tạo được liên kết hydrogen với nước. Khi số nguyên tử carbon trong gốc hydrocarbon tăng thì độ tan của các amine giảm.
Ở điều kiện thường, aniline là chất lỏng, ít tan trong nước.
IV. Tính chất hóa học
1. Tính base và phản ứng tạo phức
Thí nghiệm: Phản ứng của nhóm amine
- Phản ứng với chất chỉ thị
Nhỏ một giọt dung dịch methylamine 0,1 M lên mẫu giấy pH hoặc giấy quỳ tím đặt trên mặt kính đồng hồ.
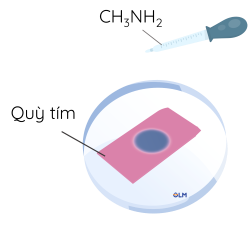
- Phản ứng với dung dịch acid
Bước 1: Thêm 1 giọt phenolphthalein vào ống nghiệm chứa 2 mL dung dịch methylamine 0,1 M.
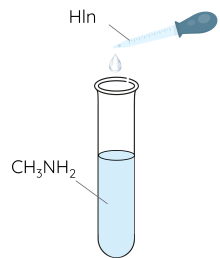
Bước 2: Nhỏ từ từ 2 mL dung dịch HCl 0,1 M vào ống nghiệm.

- Phản ứng với dung dịch muối
Thêm khoảng 3 mL dung dịch methylamine 0,1 M vào ống nghiệm chứa khoảng 1 mL dung dịch FeCl3 0,1 M.

- Phản ứng với copper(II) hydroxide
Bước 1: Cho khoảng 2 mL dung dịch CuSO4 0,1 M vào ống nghiệm.
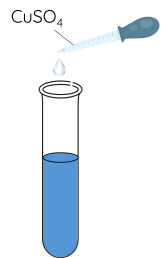
Bước 2: Thêm từ từ dung dịch methylamine 0,1 M vào ống nghiệm, lắc đều tới khi kết tủa tan hết.
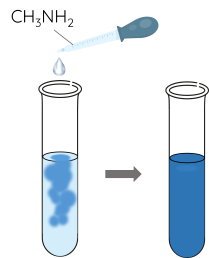
Tương tự như ammonia, amine thể hiện tính base yếu. Dung dịch các alkylamine có thể làm quỳ tím đổi màu xanh, còn dung dịch aniline không làm đổi màu quỳ tím.
Ví dụ:
\(CH_3NH_2+H_2O⇌CH_3NH_3^++OH^-\)
\(CH_3NH_2+HCl\rightarrow CH_3NH_3Cl\)
\(FeCl_3+3CH_3NH_2+3H_2O\rightarrow Fe\left(OH\right)_3+3CH_3NH_3Cl\)
Các amine như methylamine hay ethylamine tác dụng với Cu(OH)2 tạo dung dịch phức chất có màu xanh lam.
Ví dụ:
\(CuCl_2+2CH_3NH_2+2H_2O\rightarrow Cu\left(OH\right)_2+2CH_3NH_3Cl\)
\(Cu\left(OH\right)_2+4CH_3NH_2\rightarrow\left[Cu\left(CH_3NH_2\right)_4\right]\left(OH\right)_2\)
2. Phản ứng với nitrous acid
Alkylamine bậc một tác dụng với nitrous acid ở nhiệt độ thường tạo thành alcohol và giải phóng khí nitrogen (phản ứng này thường được dùng để nhận biết alkylamine bậc một).
Ví dụ:
\(CH_3NH_2+HONO\rightarrow CH_3OH+N_2+H_2O\)
Aniline tác dụng với nitrous acid ở nhiệt độ thấp (0 – 5 oC) tạo thành muối diazonium (thường được dùng trong tổng hợp phẩm nhuộm azo và dược phẩm).
\(C_6H_5NH_2+HONO+HCl\overset{0-5^oC}{\rightarrow}\left[C_6H_5N_2\right]^+Cl^-+2H_2O\)
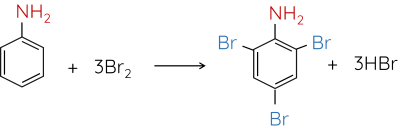
3. Phản ứng của aniline với nước bromine
Thí nghiệm: Phản ứng của aniline với nước bromine
Thêm từ từ vài giọt dung dịch aniline loãng vào ống nghiệm chứa khoảng 1 mL nước bromine.
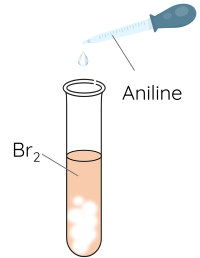
Do ảnh hưởng của nhóm –NH2, aniline dễ tham gia phản ứng thế nguyên tử H của vòng benzene hơn so với benzene, ưu tiên thế vào các vị trí ortho và para so với nhóm NH2.
V. Ứng dụng
Aniline là nguyên liệu tổng hợp một số hợp chất quan trọng trong các lĩnh vực khác nhau như công nghiệp phẩm nhuộm, dược phẩm (như paracetamol, sulfonamide) hay công nghiệp polymer.
Một số diamine được sử dụng làm nguyên liệu tổng hợp tơ sợi.
Ví dụ: Hexamethylenediamine là nguyên liệu tổng hợp nylon-6,6.

VI. Điều chế
1. Alkyl hóa ammonia
Alkylamine được điều chế từ ammonia và dẫn xuất halogen.
Ví dụ:
\(NH_3\xrightarrow[+CH_3I]{-HI}NH_2\left(CH_3\right)\xrightarrow[+CH_3I]{-HI}NH\left(CH_3\right)_2\xrightarrow[+CH_3I]{-HI}N\left(CH_3\right)_3\)
2. Khử hợp chất nitro
Aniline và các arylamine thường được điều chế bằng cách khử hợp chất nitrobenzene (hoặc dẫn xuất nitro tương ứng) bởi một số kim loại (Zn, Fe,...) trong dung dịch HCl.
Ví dụ:
\(C_6H_5NO_2+6\left[H\right]\xrightarrow[t^o]{Fe+HCl}C_6H_5NH_2+2H_2O\)
1. Amine là dẫn xuất của ammonia, trong đó nguyên tử hydrogen trong phân tử ammonia được thay thế bằng gốc hydrocarbon. Có thể phân loại amine theo bậc amine (amine bậc một, bậc hai và bậc ba) hoặc theo đặc điểm cấu tạo gốc hydrocarbon (alkylamine và arylamine).
2. Amine có tính base yếu; một số amine như methylamine, ethylamine tạo được hợp chất phức với Cu2+; các alkylamine bậc một phản ứng với HNO2 tạo thành alcohol và giải phóng N2; Aniline phản ứng với HNO2 ở nhiệt độ thấp tạo muối diazonium; aniline dễ tham gia phản ứng thế nguyên tử H của vòng benzene hơn so với benzene.
3. Các amine được điều chế bằng cách alkyl hóa ammonia hoặc khử hợp chất nitro.
4. Các amine là nguyên liệu cho công nghiệp tổng hợp phẩm nhuộm, dược phẩm, polymer và tơ sợi.

Bạn có thể đánh giá bài học này ở đây