Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Alkene SVIP
1. Khái niệm alkene
Alkene là những hydrocarbon mạch hở, trong phân tử có một liên kết đôi C=C.
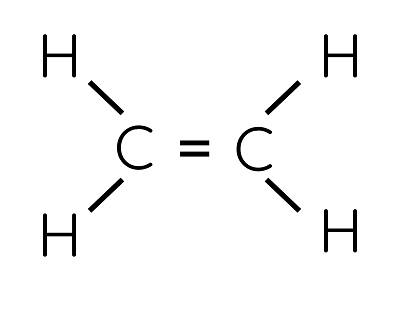
Alkene đơn giản nhất là ethylene, công thức cấu tạo thu gọn là CH2=CH2.
Ethylene là chất khí không màu, không mùi, rất ít tan trong nước.
2. Tính chất hóa học của ethylene
Thí nghiệm 1: Đốt cháy ethylene trong không khí
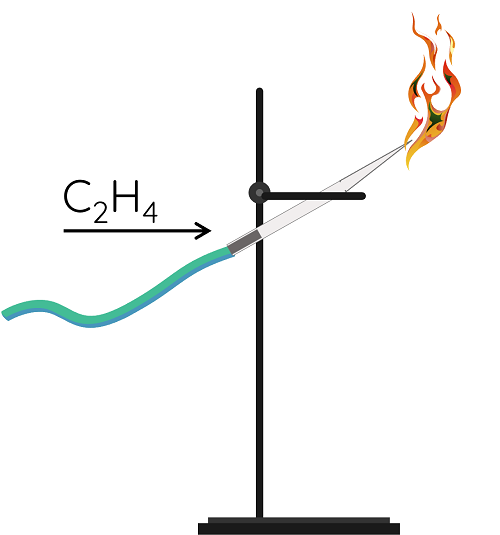
Phương trình phản ứng xảy ra:
C2H4 + 3O2 \(\underrightarrow{t^o}\) 2CO2 + 2H2O
Thí nghiệm 2: Ethylene với nước bromine

Nước bromine ban đầu có màu vàng nâu, sản phẩm của phản ứng giữa ethylene và nước bromine là hợp chất không màu.
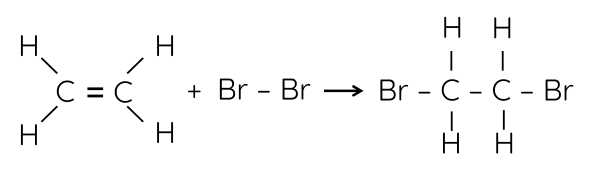
Ở điều kiện thích hợp, các phân tử ethylene cộng hợp liên tiếp với nhau, tạo thành chất có khối lượng phân tử lớn, gọi là polymer.
Phương trình hóa học của phản ứng trùng hợp polyethylene:
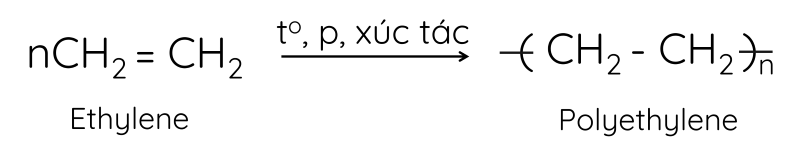
3. Một số ứng dụng của ethylene
- Sản xuất dung môi.
- Tổng hợp ethylic alcohol, acetic acid.
- Sản xuất polythylene (PE), poly(vinyl chloride) (PVC).
1. Alkene là những hydrocarbon mạch hở, chứa các liên kết đơn và một liên kết đôi trong phân tử.
2. Ethylene là chất khí, không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
3. Ethylene khi cháy trong không khí tạo thành sản phẩm chủ yếu gồm carbon dioxide và hơi nước, phản ứng tỏa nhiều nhiệt.
4. Ethylene làm mất màu nước bromine và tham gia phản ứng trùng hợp tạo thành polyethylene.
5. Tương tự ethylen, các alkene khác cũng có phản ứng cháy và phản ứng với nước bromine.
6. Ethylene được dùng để sản xuất ethylic alcohol và tổng hợp polyethylene trong công nghiệp.

Bạn có thể đánh giá bài học này ở đây