Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Vậy khối lượng H2SO4 có tong 20g dung dịch H2SO4 98% là:
mct=C%. mdd100%=98%. 20100%=19,6(gam)
Đáp số: 19,6g
Khối lượng dung dịch H2SO4 làm 20 x 98% : 100% = 19,6 (gam)

chào bạn Nguyễn trọng phúc
Ồ, xin lỗi nhé, mình đang làm những bài tập lớp 4 mà lại làm bẩn tay người khác à? Có lẽ mình cần phải học thêm cách không làm người ta cảm thấy khó chịu. Nhưng nếu bạn có câu hỏi thật sự cần giải đáp, cứ nói, mình sẽ giúp đỡ hết mình, đừng ngại nhé!"
a, X là Aluminium oxide (Al2O3)
b, Ta có: \(n_{Al}=\dfrac{8,1}{27}=0,3\left(mol\right)\)
PT: \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\)
Theo PT: \(n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=0,15\left(mol\right)\)
Ta có: nH2SO4 = 0,4.1,5 = 0,6 (mol)
Xét tỉ lệ: \(\dfrac{0,15}{1}< \dfrac{0,6}{3}\), ta được H2SO4 dư.
Theo PT: \(\left\{{}\begin{matrix}n_{Al_2\left(SO_4\right)_3}=n_{Al_2O_3}=0,15\left(mol\right)\\n_{H_2SO_4\left(pư\right)}=3n_{Al_2O_3}=0,45\left(mol\right)\end{matrix}\right.\)
⇒ nH2SO4 (dư) = 0,6 - 0,45 = 0,15 (mol)
\(\Rightarrow C_{M_{H_2SO_4}}=C_{M_{Al_2\left(SO_4\right)_3}}=\dfrac{0,15}{0,4}=0,375\left(M\right)\)

Hỗn hợp khí thu được gồm: CO và CO2
Ta có: \(\left\{{}\begin{matrix}n_{CO}+n_{CO_2}=\dfrac{4,958}{24,79}=0,2\\28n_{CO}+44n_{CO_2}=19.2.0,2\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{CO}=0,075\left(mol\right)\\n_{CO_2}=0,125\left(mol\right)\end{matrix}\right.\)
PT: \(C+\dfrac{1}{2}O_2\underrightarrow{t^o}CO\)
\(C+O_2\underrightarrow{t^o}CO_2\)
Theo PT: \(n_C=n_{CO}+n_{CO_2}=0,2\left(mol\right)\)
⇒ mC = 0,2.12 = 2,4 (g)

1 tấn = 1000 kg
a, Ta có: \(n_{CaCO_3}=\dfrac{1000}{100}=10\left(kmol\right)\)
PT: \(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
______10______10_____10 (kmol)
⇒ mCaO = 10.56 = 560 (kg)
mCO2 = 10.44 = 440 (kg)
b, 504 (g) = 0,504 (kg)
\(\Rightarrow H\%=\dfrac{0,504}{560}.100\%=0,09\%\)

a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, Ta có: \(n_{H_2}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{ZnCl_2}=n_{H_2}=0,3\left(mol\right)\)
\(n_{HCl}=2n_{H_2}=0,6\left(mol\right)\)
⇒ mZn = 0,3.65 = 19,5 (g)
mHCl = 0,6.36,5 = 21,9 (g)
c, mZnCl2 = 0,3.136 = 40,8 (g)

a) CuO + H₂SO₄ -> CuSO₄ + H₂O
0,04 0,04 0,04 0,04
b) số mol của CuO là: \(n_{CuO}=\dfrac{m}{M_{CuO}}=\dfrac{3,2}{80}=0,04\left(mol\right)\)
khối lượng chất tan H₂SO₄ là:
\(C\%=\dfrac{m_{ct}}{m_{dd}}\cdot100\%\Rightarrow m_{ct}=\dfrac{C\%\cdot mdd}{100\%}=\dfrac{20\%\cdot200}{100\%}=40\left(g\right)\)
số mol chất tan H₂SO₄ là:
\(n_{H_2SO_4}=\dfrac{m_{ct}}{M}=\dfrac{40}{98}=0,4\left(mol\right)\)
lập tỉ lệ: \(\dfrac{n_{CuO}}{1}=\dfrac{0,04}{1}< \dfrac{n_{H_2SO_4}}{1}=\dfrac{0,4}{1}\left(\text{H2SO4 dư tính theo CuO}\right)\)
b) vì H₂SO₄ dư nên sau phản ứng vẫn còn dung dịch H₂SO₄
\(n_{H_2SO_4}=n_{\text{ban đầu}}-n_{\text{phản ứng}}=0,4-0,04=0,36\left(mol\right)\)
khối lượng dung dịch sau phản ứng là:
\(m_{\text{dd sau phản ứng}}=m_{CuO}+m_{H_2SO_4}=3,2+200=203,2\left(g\right)\)
nồng độ phần trăm H₂SO₄ dư sau phản ứng là:
\(C\%_{H_2SO_4\text{dư}}=\dfrac{0,36\cdot98}{203,2}\cdot100\%=17,362\%\)
nồng độ phần trăm CuSO₄ sau phản ứng là:
\(C\%_{CúSO_4}=\dfrac{0,04\cdot160}{203,2}\cdot100\%\approx3,15\%\)
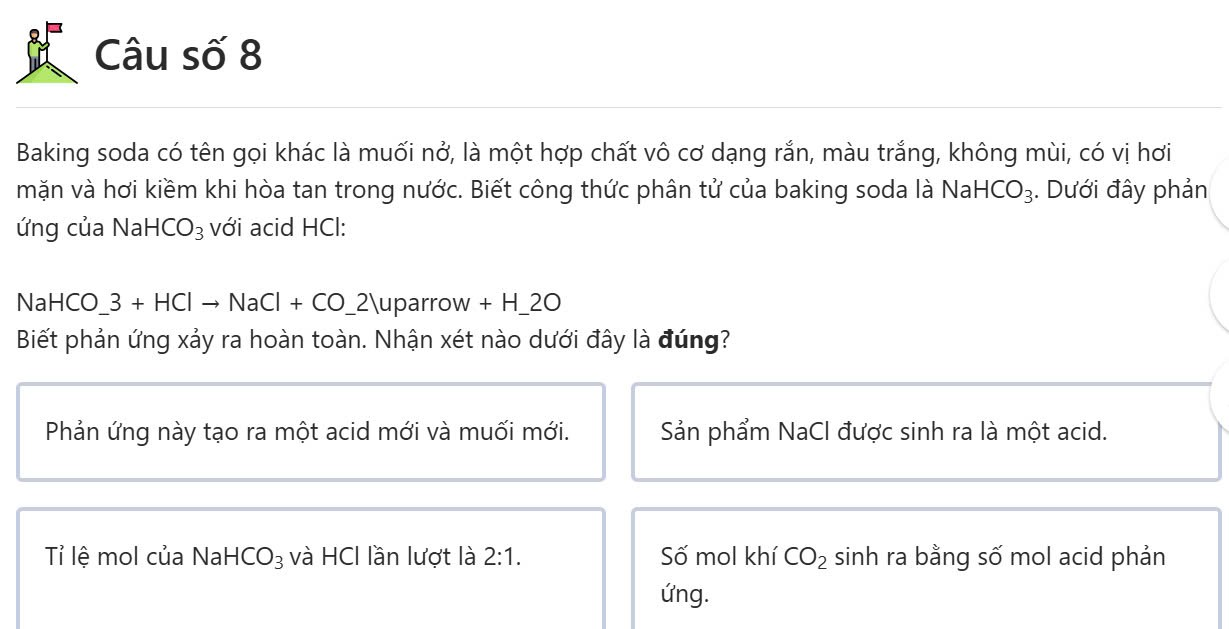
Đáp án: Số mol khí CO2 sinh ra bằng số mol acid phản ứng.