Đốt cháy hoàn toàn 6.72 lít hỗn hợp khí axitilen, metan cần dùng 15.68 lít khí oxi. Phần trăm thể tích mỗi khí trong hỗn hợp là (bt là khí đều ở ĐKTC) ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



a)
P1: \(n_{CO_2}=\dfrac{0,48}{24}=0,02\left(mol\right)\)
PTHH: 2CH3COOH + K2CO3 --> 2CH3COOK + CO2 + H2O
0,04<------0,02<----------------------0,02
=> \(m_{K_2CO_3}=0,02.138=2,76\left(g\right)\)
=> \(m=\dfrac{2,76.100}{6,9}=40\left(g\right)\)
mCH3COOH = 0,04.60 = 2,4 (g)
\(\%m_{CH_3COOH}=\dfrac{2,4}{3,78}.100\%=63,492\%\)
\(\%m_{C_2H_5OH}=\dfrac{3,78-2,4}{3,78}.100\%=36,508\%\)
\(n_{C_2H_5OH}=\dfrac{3,78-2,4}{46}=0,03\left(mol\right)\)
=> \(n_{CH_3COOH}:n_{C_2H_5OH}=0,04:0,03=4:3\)
b)
P2: Gọi \(\left\{{}\begin{matrix}n_{CH_3COOH}=4a\left(mol\right)\\n_{C_2H_5OH}=3a\left(mol\right)\end{matrix}\right.\)
PTHH: CH3COOH + C2H5OH --to,H+--> CH3COOC2H5 + H2O
Xét tỉ lệ: \(\dfrac{4a}{1}>\dfrac{3a}{1}\) => Hiệu suất tính theo C2H5OH
\(n_{C_2H_5OH\left(pư\right)}=\dfrac{3a.75}{100}=2,25a\left(mol\right)\)
PTHH: CH3COOH + C2H5OH --to,H+--> CH3COOC2H5 + H2O
2,25a-------------->2,25a
=> 2,25a = \(\dfrac{7,92}{88}=0,09\)
=> a = 0,04 (mol)
=> P2 \(\left\{{}\begin{matrix}n_{CH_3COOH}=0,16\left(mol\right)\\n_{C_2H_5OH}=0,12\left(mol\right)\end{matrix}\right.\)
X chứa \(\left\{{}\begin{matrix}CH_3COOH:0,2\left(mol\right)\\C_2H_5OH:0,15\left(mol\right)\end{matrix}\right.\)
=> a = 0,2.60 + 0,15.46 = 18,9 (g)

TL:
Nguyên tử là đơn vị cơ bản của vật chất chứa một hạt nhân ở trung tâm bao quanh bởi đám mây điện tích âm các electron.
HT

nZn = 13/65 = 0,2 (mol)
nHCl = 14,6/36,5 = 0,4 (mol)
PTHH: Zn + 2HCl -> ZnCl2 + H2
LTL: 0,2 = 0,4/2 => phản ứng đủ
nH2 = nZnCl2 = 0,2 (mol)
VH2 = 0,2 . 22,4 = 4,48 (l)
mZnCl2 = 0,1 . 136 = 27,2 (g)
mH2 = 0,2 . 2 = 0,4 (g)
\(n_{Zn}=\frac{13}{65}=0,2\left(mol\right)\)
\(n_{HCl}=\frac{14,6}{36,5}=0,4\left(mol\right)\)
\(PTHH:Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
tỉ số: \(\frac{0,2}{1}=\frac{0,4}{2}\Rightarrow\) PTHH này ko có chất dư (sau khi pứ kết thúc)
a) \(n_{H_2}=n_{Zn}=0,2\left(mol\right)\)
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
\(n_{ZnCl_2}=n_{Zn}=0,2\left(mol\right)\)
\(m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
XONG!

a. PTHH:
+ Lần thí nghiệm 1: 2NaOH + H2SO4 → Na2SO4 + 2H2O (1)
Vì quỳ tím hóa xanh, chứng tỏ NaOH dư. Thêm HCl:
HCl + NaOH → NaCl + H2O (2)
+ Lần thí nghiệm 2: phản ứng (1) xảy ra, sau đó quỳ hóa đỏ chứng tỏ H2SO4 dư. Thêm NaOH:
2NaOH + H2SO4 → Na2SO4 + 2H2O (3)
+ Đặt x, y lần lượt là nồng độ mol/l của dung dịch A và dd B: Từ (1),(2),(3) ta có:
0,3y - 2.0,2x = 0,05 (I)
0,3x - \(\dfrac{0,2y}{2}\) = 0,1 (II)
Giải hệ (I,II) ta được: x = 0,7 mol/l , y = 1,1 mol/l
b, Vì dung dịch E tạo kết tủa với AlCl3 , chứng tỏ NaOH còn dư.
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl (4)
2Al(OH)3 → Al2O3 + 3H2O (5)
Na2SO4 + BaCl2 → BaSO4 + 2NaCl (6)
Ta có n(BaCl2) = 0,1.0,15 = 0,015 mol
n(BaSO4) = 3,262 : 233= 0,014 mol < 0,015 mol
⇒ n(H2SO4) = n(Na2SO4) = n(BaSO4) = 0,014 mol . Vậy VA = 0,014 : 0,7 = 0,02 lít
n(Al2O3) = 3,262 : 102 = 0,032 mol và n(AlCl3) = 0,1.1 = 0,1 mol.
+ Xét 2 trường hợp có thể xảy ra:
- Trường hợp 1: Sau phản ứng với H2SO4,NaOH dư nhưng thiếu so vời AlCl3 (ở pư (4): n(NaOH) pư trung hoà axit = 2.0,014 = 0,028 mol
nNaOH pư (4) = 3n(Al(OH)3) = 6n(Al2O3) = 6.0,032 = 0,192 mol.
Tổng số mol NaOH bằng 0,028 + 0,192 = 0,22 mol
Thể tích dung dịch NaOH 1,1 mol/l là \(\dfrac{0,22}{1,1}\)= 0,2 lít . Tỉ lệ VB : VA = 0,2 : 0,02 = 10
- Trường hợp 2: Sau (4) NaOH vẫn dư và hoà tan một phần Al(OH)3:
Al(OH)3 + NaOH → NaAlO2 + 2H2O (7)
Tổng số mol NaOH pư (3,4,7) là: 0,028 + 3.0,1 + 0,1 - 2.0,032 = 0,364 mol
Thể tích dung dịch NaOH 1,1 mol/l là \(\dfrac{0,364}{1,1}\)= 0,33 lít
⇒ Tỉ lệ VB : VA = 0,33 : 0,02 = 16,5

A: CaCO3
B: CO2
C: NaHCO3
D: Na2CO3
E: HCl
F: CaCl2
PTHH:
\(CaCO_3\left(A\right)\underrightarrow{t^o}CaO+CO_2\left(B\right)\)
\(CO_2\left(B\right)+NaOH\rightarrow NaHCO_3\left(C\right)\)
\(CO_2\left(B\right)+2NaOH\rightarrow Na_2CO_3\left(D\right)+H_2O\)
\(NaHCO_3\left(C\right)+HCl\left(E\right)\rightarrow NaCl\left(H\right)+CO_2+H_2O\)
\(Na_2CO_3\left(D\right)+CaCl_2\left(F\right)\rightarrow2NaCl\left(H\right)+CaCO_3\downarrow\)
\(NaHCO_3\left(C\right)+NaOH\rightarrow Na_2CO_3\left(D\right)+H_2O\)
\(Na_2CO_3\left(D\right)+HCl\rightarrow NaCl+NaHCO_3\left(E\right)\)

a, PTHH:
2Cu + O2 -> (t°) 2CuO (1)
CuO + H2 -> (t°) Cu + H2O (2)
2Na + 2H2O -> 2NaOH + H2 (3)
2H2 + O2 -> (t°) 2H2O (4)
b, A: CuO: đồng (II) oxit
B: Cu: đồng
C: H2O: nước
D: H2: hiđro
F: O2: oxi
c, nCu = 12,8/64 = 0,2 (mol)
Theo (1): nCuO = nCu = 0,2 (mol)
Theo (2): nH2O = nCuO = 0,2 (mol)
Theo (3): nH2 = nH2O/2 = 0,2/2 = 0,1 (mol)
Theo (4): nH2O = nH2 = 0,1 (mol)
mH2O = 0,1 . 18 = 1,8 (g)

\(n_{hh}=\dfrac{11,2}{22,4}=0,5mol\)
\(\left\{{}\begin{matrix}n_{C_2H_4}=x\left(mol\right)\\n_{C_2H_2}=y\left(mol\right)\end{matrix}\right.\Rightarrow x+y=0,5\left(1\right)\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
\(\Rightarrow x+2y=0,7\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,3\\y=0,2\end{matrix}\right.\)
\(\%V_{C_2H_4}=\dfrac{0,3\cdot22,4}{11,2}\cdot100\%=60\%\)
\(\%V_{C_2H_2}=100\%-60\%=40\%\)
 Giups mình vs
Giups mình vs
 giúp mình vs
giúp mình vs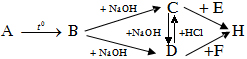
PTHH:\(2C_2H_2+5O_2\underrightarrow{t^o}4CO_2+2H_2O\)
x 5/2x
\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
y 2y
Gọi số mol của của \(C_2H_2\)là x; số mol của \(CH_4\)là y
Tổng số mol của hổn hợp là:
6,72:22,4=0,3(mol)
\(\rightarrow x+y=0,3\left(1\right)\)
Tổng số mol của Oxi là:
15,68:22,4=0,7(mol)
\(\rightarrow2,5x+2y=0,7\left(2\right)\)
Từ (1) và (2) ta lập được hệ:
\(\hept{\begin{cases}x+y=0,3\\2,5x+2y=0,7\end{cases}\Rightarrow\hept{\begin{cases}x=0,2\\y=0,1\end{cases}}}\)
\(V_{C_2H_2}=0,2.22,4=4,48\left(l\right)\)
\(\%V_{C_2H_2}=\frac{4,48}{6,72}.100\approx66,7\%\)
\(\%V_{CH_4}=100\%-66,7\%=33,3\%\)
nhh khí = 6,72/22,4 = 0,3 (mol)
Gọi nC2H2 = a (mol); nCH4 = b (mol)
=> a + b = 0,3 (1)
nO2 = 15,68/22,4 = 0,7 (mol)
PTHH: 2C2H2 + 5O2 -> (t°) 4CO2 + 2H2O
Mol: a ---> 2,5a
CH4 + 2O2 -> (t°) CO2 + 2H2O
Mol: b ---> 2b
=> 2,5a + 2b = 0,7 (2)
(1)(2) => a = 0,2 (mol); b = 0,1 (mol)
%VC2H2 = 0,2/0,3 = 66,66%
%VCH4 = 100% - 66,66% = 33,34%