Nhỏ dd iốt lê mặt cắt củ khoai lang thấy xuất hiện màu xanh tím là do khoai lang có chứa chất nào sau đây
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Hiện tượng vật lí: là hiện tượng chất biến đổi mà vẫn giữ nguyên là chất ban đầu
Hiện tượng hóa học: là hiện tượng chất này biến đổi thành chất khác

Dùng Bacl2 nếu kết tủa là Fe2(SO4)2 để phân biệt ra 2 nhóm
sau đó ở nhóm 2 cho từng chất tác dụng với nhau nếu có hiện tượng Cu tan tạo khí không màu hóa nâu trong không khí thì là CuCl2 và AgNO3 còn lại là NaCl
+ Mẫu thử nào thấy có kết tủa màu xanh thẫm trong dung dịch là Cu(OH)2 nên chất ban đầu là CuCl2
CuCl2+2NaOH−−−>Cu(OH)2↓+2NaCl����2+2����−−−>��(��)2↓+2����
+ Mẫu thử xuất hiện kết tủa trắng là Mg(OH)2 nên chất ban đầu là MgCk2
MgCl2+2NaOH−−−>Mg(OH)2↓+2NaCl����2+2����−−−>��(��)2↓+2����
+ Mẫu thử xuất hiện kết tủa nâu đỏ là Fe(OH)3 nên chất ban đầu là Fe2(SO4)3
Fe2(SO4)3+6NaOH−−−>2Fe(OH)3+3Na2SO4��2(��4)3+6����−−−>2��(��)3+3��2��4
+ Mẫu thử không có hiện tượng gì là NaOH

A. Số mol Ba(OH)2 = ��=34.2171=0,2���Mm=17134.2=0,2mol
Ba(OH)2 + Na2SO4 → BaSO4 + 2NaOH
PT: 1mol 1mol
ĐB: 0,2mol 0,2mol
Khối lượng BaSO4: mBaSO4= n.M = 0,2×233 = 46,6 g
B. Khối lượng Na2SO4 phản ứng:
mNa2SO4 = n. M = 0,2 . 142 = 28,4g
Nồng độ phần trăm của dd Na2SO4: C%= 46,6200.100%=23,3%20046,6.100%=23,3%
Bạ
A. Số mol Ba(OH)2 =m/M ��=34.2171=0,2���
=
34,2/171=0,2mol
Ba(OH)2 + Na2SO4 → BaSO4 + 2NaOH
PT: 1mol 1mol
ĐB: 0,2mol 0,2mol
Khối lượng BaSO4: mBaSO4= n.M = 0,2×233 = 46,6 g
n chưa trả lời câu hỏi này. Trả lời câu hỏi này
B. Khối lượng Na2SO4 phản ứng:
mNa2SO4 = n. M = 0,2 . 142 = 28,4g
Nồng độ phần trăm của dd Na2SO4: C%=46,6/200 46,6200.100%=23,3%
.100%=23,3%

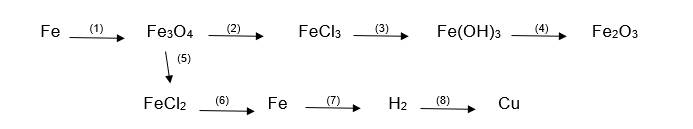
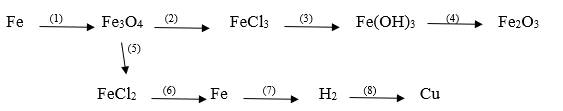
(1) \(3Fe+2O_2\xrightarrow[]{t^\circ}Fe_3O_4\)
(2) \(Fe_3O_4+8HCl\xrightarrow[]{}FeCl_2+2FeCl_3+4H_2O\)
(3) \(FeCl_3+3LiOH\xrightarrow[]{}Fe\left(OH\right)_3\downarrow+3LiCl\)
(4) \(2Fe\left(OH\right)_3\xrightarrow[]{t^\circ}Fe_2O_3+3H_2O\)
(5) \(Fe_3O_4+8HCl\xrightarrow[]{}FeCl_2+2FeCl_3+4H_2O\)
(6) \(FeCl_2\xrightarrow[]{đpdd}Fe+Cl_2\uparrow\)
(7) \(Fe+2HCl\xrightarrow[]{}FeCl_2+H_2\uparrow\)
(8) \(H_2+CuO\xrightarrow[]{t^\circ}Cu+H_2O\uparrow\)
(1) 3��+2�2→�∘��3�43Fe+2O2t∘Fe3O4
(2) ��3�4+8���→����2+2����3+4�2�Fe3O4+8HClFeCl2+2FeCl3+4H2O
(3) ����3+3����→��(��)3↓+3����FeCl3+3LiOHFe(OH)3↓+3LiCl
(4) 2��(��)3→�∘��2�3+3�2�2Fe(OH)3t∘Fe2O3+3H2O
(5) ��3�4+8���→����2+2����3+4�2�Fe3O4+8HClFeCl2+2FeCl3+4H2O
(6) ����2→đ�����+��2↑FeCl2đpddFe+Cl2↑
(7) ��+2���→����2+�2↑Fe+2HClFeCl2+H2↑
(8) �2+���→�∘��+�2�↑H2+CuOt∘Cu+H2O↑

(1) \(3Fe+2O_2\xrightarrow[]{t^\circ}Fe_3O_4\)
(2) \(Fe_3O_4+8HCl\xrightarrow[]{}FeCl_2+2FeCl_3+4H_2O\)
(3) \(FeCl_3+3LiOH\xrightarrow[]{}Fe\left(OH\right)_3\downarrow+3LiCl\)
(4) \(2Fe\left(OH\right)_3\xrightarrow[]{t^\circ}Fe_2O_3+3H_2O\)
(5) \(Fe_3O_4+8HCl\xrightarrow[]{}FeCl_2+2FeCl_3+4H_2O\)
(6) \(FeCl_2\xrightarrow[]{đpdd}Fe+Cl_2\uparrow\)
(7) \(Fe+2HCl\xrightarrow[]{}FeCl_2+H_2\uparrow\)
(8) \(H_2+CuO\xrightarrow[]{t^\circ}Cu+H_2O\uparrow\)
Chất tinh bột