Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Đề kiểm tra cuối học kì 1 (đề số 1) SVIP
Yêu cầu đăng nhập!
Bạn chưa đăng nhập. Hãy đăng nhập để làm bài thi tại đây!
Sử dụng thông tin sau cho Câu 1 và Câu 2: Một miếng kim loại có khối lượng 500 g được nung nóng từ 20 oC lên 100 oC. Biết nhiệt dung riêng của kim loại này là 380 J/kg.K, của nước là 4200 J/kg.K.
Nhiệt lượng cần thiết để làm nóng miếng kim loại từ 20 oC lên 100 oC là
Sau khi miếng kim loại đã nóng đến 100 oC, nó được ngâm vào một bể nước 2 lít ở nhiệt độ 30 oC. Nhiệt độ cân bằng nhiệt lúc này là
Sử dụng thông tin sau cho Câu 1 và Câu 2: Một bình chứa khí lí tưởng có thể tích 2 m3 với áp suất 2.105 Pa và nhiệt độ 300 K.
Số mol khí trong bình xấp xỉ là
Nếu nhiệt độ của khí trong bình tăng lên 450 K thì áp suất trong bình lúc này là bao nhiêu? Coi thể tích khí không đổi.
Sử dụng thông tin sau cho Câu 1 và Câu 2: Một nhà máy điện hơi nước nhận nhiệt từ một lò nung với tốc độ 280 GJ/h. Tổn thất nhiệt cho không khí xung quanh từ hơi nước khi nó đi qua các đường ống và các thành phần khác được ước tính là khoảng 8 GJ/h. Biết nhiệt lượng có ích được chuyển về nước làm mát với tốc độ 145 GJ/h.
Sản lượng điện sản xuất ra là bao nhiêu GJ/h?
Trả lời: .
Hiệu suất nhiệt của nhà máy điện này là bao nhiêu % (làm tròn kết quả đến chữ số hàng phần mười)?
Trả lời: .
Sử dụng thông tin sau cho Câu 1 và Câu 2: Ở độ cao 10 km so với mặt đất thì áp suất không khí là 30,6 kPa, còn nhiệt độ là 230 K. Coi không khí như một chất khí thuần nhất có khối lượng mol là 28,8 g/mol. Tại độ cao đó:
Khối lượng riêng của không khí là bao nhiêu kg/m3 (làm tròn kết quả đến chữ số hàng phần trăm)?
Trả lời: .
Mật độ phân tử của không khí là X.1024 phân tử/m3. Tìm giá trị của X (làm tròn kết quả đến chữ số hàng phần mười).
Trả lời: .
Sử dụng thông tin sau cho Câu 1 và Câu 2: Một bình chứa 120 g khí H 2 ở nhiệt độ 27 oC và áp suất 100 kPa. Cho khối lượng mol của H2 là 2 g, hằng số khí R=8,31 J.mol/K.
Thể tích của bình chứa là bao nhiêu m3 (làm tròn kết quả đến chữ số hàng phần mười)?
Trả lời: .
Tốc độ bình phương trung bình của phân tử H2 là Y.10-23 m2/s2. Tìm giá trị Y (làm tròn kết quả đến chữ số hàng phần mười).
Trả lời: .
Mô hình động học phân tử chất khí đã thuyết phục được nhiều nhà vật lí về sự tồn tại của các phân tử trước khi người ta có thể quan sát được chúng.
(Nhấp vào ô màu vàng để chọn đúng / sai)| a) Chất khí được cấu tạo từ các phân tử có kích thước rất lớn so với khoảng cách giữa chúng. |
|
| b) Lực liên kết giữa các phân tử ở thể khí rất yếu so với ở thể lỏng và thể rắn. |
|
| c) Các phân tử khí chuyển động hỗn loạn, không ngừng. |
|
| d) Các phân tử khí không thể gây áp suất lên thành bình. |
|
Định luật Boyle được nhà vật lí và hóa học người Ireland là Robert Boyle (1627 - 1691) tìm ra bằng thực nghiệm năm 1662 khi ông nghiên cứu về quá trình biến đổi trạng thái của một khối lượng khí xác định.
(Nhấp vào ô màu vàng để chọn đúng / sai)| a) Quá trình đẳng nhiệt là quá trình biến đổi trạng thái của một khối lượng khí xác định khi nhiệt độ giữ không đổi. |
|
| b) Định luật Boyle phù hợp với quá trình đẳng nhiệt. |
|
| c) Khi nhiệt độ của một khối lượng khí xác định giữ không đổi thì áp suất gây ra bởi khí tỉ lệ thuận với thể tích của nó. |
|
| d) Đồ thị biểu diễn định luật Boyle là một nhánh của đường parabol. |
|
Một lượng khí lí tưởng được đựng trong một xi lanh có pit-tông chuyển động được. Áp suất của khí là 0,7 atm và nhiệt độ là 47 oC.
(Nhấp vào ô màu vàng để chọn đúng / sai)| a) Với khí lí tưởng, va chạm giữa các phân tử khí là va chạm mềm. |
|
| b) Thể tích của khí trong xi lanh là không đổi trong mọi quá trình biến đổi trạng thái. |
|
| c) Khi áp suất trong xi lanh tăng đến 8 atm còn thể tích khí trong xi lanh giảm 5 lần thì nhiệt độ khí là 731,4 K. |
|
| d) Khi giữ pit-tông cố định, tăng nhiệt độ khí trong xi lanh tới 273 oC thì áp suất khí trong xi lanh là 1,19 atm. |
|
Một bình đựng một khối lượng khí. Cho hằng số Boltzmann k=1,38.10−23 J/K.
(Nhấp vào ô màu vàng để chọn đúng / sai)| a) Động năng trung bình của các phân tử khí chỉ phụ thuộc vào nhiệt độ khối khí. |
|
| b) Khi nhiệt độ khối khí tăng thì động năng của mỗi phân tử khí đều tăng. |
|
| c) Động năng trung bình của mỗi phân tử khí ở 27 oC là 24,84.10-23 J. |
|
| d) Biết thành phần chính của không khí là N2 (khối lượng mol là 28) và O2 (khối lượng mol 32). Khi đó tốc độ bình phương trung bình (v2) của các phân tử N2 lớn hơn tốc độ bình phương trung bình của các phân tử O2. |
|
Từ hình ảnh về quỹ đạo chuyển động Brown của hạt khói trong không khí dưới đây, có thể thấy các phân tử khí chuyển động

Một mẫu vật chất có khối lượng m, chứa N phân tử thì số mol n của mẫu vật đó được xác định theo biểu thức nào dưới đây?
Các thông số trạng thái của một lượng khí không bao gồm đại lượng nào dưới đây của lượng khí đó?
Trong hệ tọa độ (V, T), đường biểu điễn nào sau đây là đường đẳng áp?
Hệ thức nào dưới đây không phù hợp với phương trình trạng thái của khí lí tưởng?
Đại lượng Nm là tổng khối lượng của các phân tử khí, tức là khối lượng của một lượng khí xác định. Ở nhiệt độ phòng, mật độ không khí xấp xỉ 1,3 kg/m3 ở áp suất 1,00.105 Pa. Giá trị của v2 là
Mối quan hệ giữa hằng số Boltzmann k và hằng số khí lí tưởng R là
Động năng trung bình của phân tử được xác định bằng hệ thức nào dưới đây?
Tính chất của chất khí nào dưới đây không chứng tỏ lực liên kết giữa các phân tử ở thể khí rất yếu so với ở thể lỏng và thể rắn?
Vì sao chất khí luôn chiếm toàn bộ thể tích của bình chứa?
Đồ thị nào sau đây biểu diễn đúng định luật Boyle?
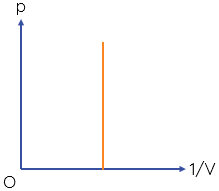
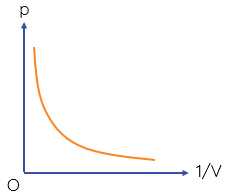
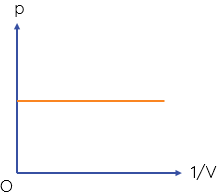
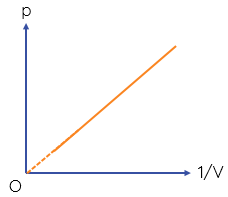
Người ta thực hiện nén đẳng áp một lượng khí xác định sao cho thể tích khí giảm đi 2 lần. Nhiệt độ tuyệt đối của khối khí khi đó sẽ
Phát biểu nào sau đây không phù hợp với bản chất của mối quan hệ giữa động năng trung bình của phân tử và nhiệt độ?
Căn bậc hai của trung bình bình phương tốc độ phân tử của một lượng khí lí tưởng là v=v2. Nếu nhiệt độ của lượng khí tăng gấp đôi thì giá trị này là
