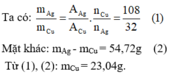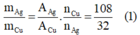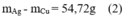Hai bình điện phân mắc nối tiếp với nhau trong một mạch điện , bình 1 chứa dung dịch CuSO4 có điện cực bằng đồng . Bình 2 cứa dung dịch AgNO3 có điện cực bằng bạc. Trong cùng một khoảng thời gian nếu lớp bạc bám vào Catốt của bình thứ 2 là M2=41.04 gam thì khối lượng Cu bám vào Catôt là bao nhiêu ?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Bài này cần phải chú ý tới giả thiết là hai bình điện phân này được mắc nối tiếp nhau, do vậy cường độ dòng điện qua hai bình là như nhau, thời gian điện phân bằng nhau. Ta có
m 2 = 1 F . A 2 n 2 I . t m 1 = 1 F . A 1 n 1 I . t ⇒ m 1 m 2 = A 1 n 1 . n 2 A 2 = 64.1 2.108 ⇒ m 1 = 12,16 g

Nếu cường độ dòng điện trong mạch bằng 0,5A thì khối lượng đồng:
\(m_{Cu}=\dfrac{1}{F}\cdot\dfrac{A}{n}\cdot I\cdot t\)
\(\Rightarrow0,64\cdot10^{-3}=\dfrac{1}{96494}\cdot\dfrac{64}{2}\cdot0,5\cdot t\)
\(\Rightarrow t=1,93s\)
thiếu nhiều quá ko có cách trình bày rõ ràng( thiếu khối lượng Ag)

Đáp án: A
Khối lượng m 1 bạc bám vào bình thứ nhất và khối lượng m 2 đồng bám vào bình thứ hai lần lượt là:
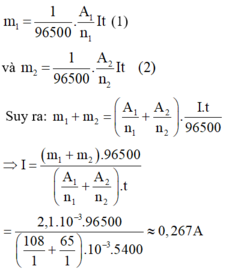
Thay I vào (1) và (2) ta có: m 1 = 1,62g; m 2 = 0,48g.